名校
解题方法
1 . 锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇
②在较高温度及酸性催化条件下,葡萄糖能发生如图反应: 时
时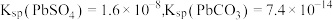
(1)已知 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为_______ 。
(2)“还原酸浸”过程中主要反应的离子方程式为_______ ,该过程中实际葡萄糖加入量远大于理论需要量,其原因是_______ 。
(3)整个流程中可循环利用的物质是_______ (填名称)。获得 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是_______ 。
(4)书写相关反应的离子方程式,并通过计算说明 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因_______ 。
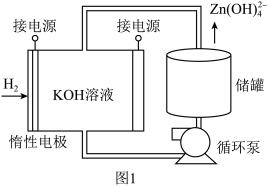
(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为_______ 。 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
① 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释_______ 。
② 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的_______ 位置(填“顶点”“面心”“棱心”或“晶胞内”)。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: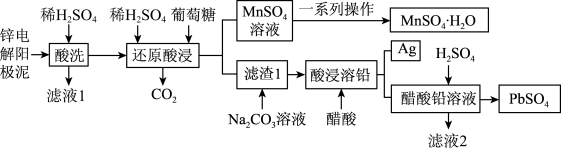
 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇②在较高温度及酸性催化条件下,葡萄糖能发生如图反应:
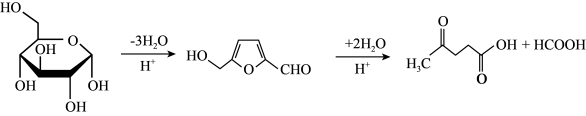
 时
时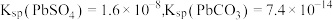
(1)已知
 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为(2)“还原酸浸”过程中主要反应的离子方程式为
(3)整个流程中可循环利用的物质是
 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是(4)书写相关反应的离子方程式,并通过计算说明
 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为
 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。①
 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释②
 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的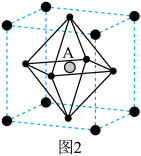
您最近一年使用:0次
7日内更新
|
94次组卷
|
2卷引用:福建省福州延安中学2024届高三下学期高考第一次模拟化学试题
解题方法
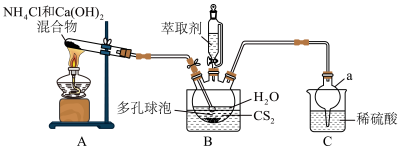
2 . 硫脲 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
(1)仪器a的名称为__________ 。
(2)从结构角度分析,硫脲可溶于水的原因是__________ 。
(3)多孔球泡的作用是__________ 。
(4)B中反应完全的标志是__________ 。
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为__________ (填标号)。
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:
取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为__________ 。
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成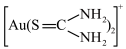 ,反应的离子方程式为
,反应的离子方程式为_______ 。溶解金的过程伴随着溶液变红的现象,原因可能为硫脲发生异构化生成__________ (填化学式)。
 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
(1)仪器a的名称为
(2)从结构角度分析,硫脲可溶于水的原因是
(3)多孔球泡的作用是
(4)B中反应完全的标志是
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:

取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成
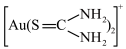 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
7日内更新
|
150次组卷
|
3卷引用:福建省厦门市国祺中学2023-2024学年高三下学期第二次模拟化学试题
名校
3 . 氮是自然界重要元素之一,氮及其化合物的性质以及氮的循环利用对解决环境和能源问题都具有重要意义。
已知:1 mol物质中的化学键断裂时所需能量如下表。
(1)恒温下,将1 mol空气 和
和 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容密闭容器中,假设体系中只存在如下两个反应:
的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容密闭容器中,假设体系中只存在如下两个反应:
ⅰ.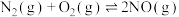


ⅱ.

 kJ⋅mol
kJ⋅mol
①
___________ kJ⋅mol 。
。
②以下操作可以降低上述平衡体系中NO浓度的有___________ (填标号)。
A.升高温度 B.移除 C.降低
C.降低 浓度
浓度
③若上述平衡体系中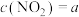 mol⋅L
mol⋅L :
: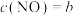 mol⋅L
mol⋅L ,则
,则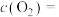
___________ mol⋅L 用含a、b、V的计算式表示)。
用含a、b、V的计算式表示)。
(2) 也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图1(其中
也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图1(其中 和NaCl略去)。NaClO氧化
和NaCl略去)。NaClO氧化 的化学反应程式为
的化学反应程式为___________ 。 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图2所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图2所示,则除氨气过程中最佳的 值约为
值约为___________ 。
(4)室温下,用水稀释0.1 mol⋅L 氨水,溶液中随着水量的增加而减小的是___________。
氨水,溶液中随着水量的增加而减小的是___________。
(5)工业上以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和
和 生成
生成 ;ⅱ.
;ⅱ. 分解生成尿素。
分解生成尿素。
结合反应过程中能量变化图3,下列说法正确的是___________ 。
b.ⅰ为放热反应,ⅱ为吸热反应
c.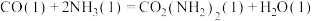

已知:1 mol物质中的化学键断裂时所需能量如下表。
| 物质 |  |  |  |
能量/kJ·mol | 945 | 498 | 631 |
(1)恒温下,将1 mol空气
 和
和 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容密闭容器中,假设体系中只存在如下两个反应:
的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容密闭容器中,假设体系中只存在如下两个反应:ⅰ.
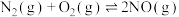


ⅱ.


 kJ⋅mol
kJ⋅mol
①

 。
。②以下操作可以降低上述平衡体系中NO浓度的有
A.升高温度 B.移除
 C.降低
C.降低 浓度
浓度③若上述平衡体系中
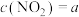 mol⋅L
mol⋅L :
: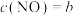 mol⋅L
mol⋅L ,则
,则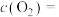
 用含a、b、V的计算式表示)。
用含a、b、V的计算式表示)。(2)
 也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图1(其中
也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图1(其中 和NaCl略去)。NaClO氧化
和NaCl略去)。NaClO氧化 的化学反应程式为
的化学反应程式为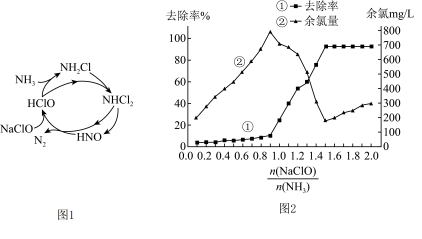
 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图2所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图2所示,则除氨气过程中最佳的 值约为
值约为(4)室温下,用水稀释0.1 mol⋅L
 氨水,溶液中随着水量的增加而减小的是___________。
氨水,溶液中随着水量的增加而减小的是___________。A.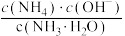 | B. |
C. | D. |
(5)工业上以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:ⅰ.
 和
和 生成
生成 ;ⅱ.
;ⅱ. 分解生成尿素。
分解生成尿素。结合反应过程中能量变化图3,下列说法正确的是
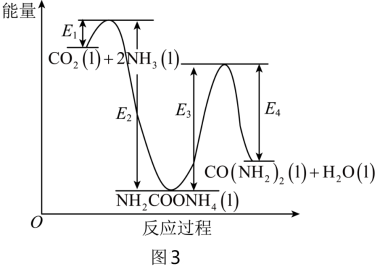
b.ⅰ为放热反应,ⅱ为吸热反应
c.
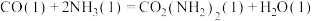

您最近一年使用:0次
2024-05-23更新
|
182次组卷
|
2卷引用:福建省福州第一中学2024届高三下学期质量检测化学试题
名校
4 .  作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(
作为一种新型锂电池正极材料受到广泛关注。由菱锰矿( ,含有少量Si、Fe、Ni、Al等元素)制备
,含有少量Si、Fe、Ni、Al等元素)制备 的流程如下:
的流程如下: ,
,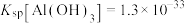 ,
, 。
。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为___________ 。
(2)加入少量 的作用是
的作用是___________ 。
(3)溶矿反应完成后,反应器中溶液 ,此时
,此时
___________  ;用石灰乳调节至
;用石灰乳调节至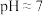 ,除去的金属离子是
,除去的金属离子是___________ 。
(4)加入少量 溶液除去
溶液除去 ,生成的沉淀有
,生成的沉淀有___________ 。
(5)在电解槽中,发生电解反应的离子方程式为___________ 。
(6)一种锰的氧化物晶胞结构如图所示。___________ 。
②已知该晶胞参数为a nm,阿伏加德罗常数为 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积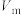 为
为___________  (列出计算式)。
(列出计算式)。
 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(
作为一种新型锂电池正极材料受到广泛关注。由菱锰矿( ,含有少量Si、Fe、Ni、Al等元素)制备
,含有少量Si、Fe、Ni、Al等元素)制备 的流程如下:
的流程如下:
 ,
,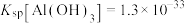 ,
, 。
。回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量
 的作用是
的作用是(3)溶矿反应完成后,反应器中溶液
 ,此时
,此时
 ;用石灰乳调节至
;用石灰乳调节至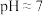 ,除去的金属离子是
,除去的金属离子是(4)加入少量
 溶液除去
溶液除去 ,生成的沉淀有
,生成的沉淀有(5)在电解槽中,发生电解反应的离子方程式为
(6)一种锰的氧化物晶胞结构如图所示。
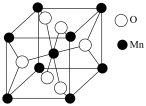
②已知该晶胞参数为a nm,阿伏加德罗常数为
 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积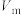 为
为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
5 . 中和渣是有色金属冶炼过程中产生的危险废渣。从中和渣(主要含有 和少量
和少量 、
、 、
、 、
、 的氢氧化物)中回收铜、锌等金属的工艺流程如下图:
的氢氧化物)中回收铜、锌等金属的工艺流程如下图: ,几种物质的
,几种物质的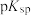 如下表
如下表
②当金属离子浓度小于 时,视为沉淀完全
时,视为沉淀完全
回答下列问题:
(1)“中性浸出”时,采用“中性”的目的是________ 。
(2)“高温高酸浸出”时,“浸渣2”的主要成分为________ 。
(3)“萃铜”时发生反应 ,
,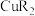 的结构简式如图所示:
的结构简式如图所示: 的价层电子排布图
的价层电子排布图________ 。
②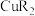 水溶性差的原因是
水溶性差的原因是________ (选填序号)。
a.形成分子内氢键 b.分子结构较稳定 c.亲油基团起主导作用
③萃取剂HR的结构简式为________ 。
(4)“氧化沉淀”时,试剂X用以调节溶液的pH。
①加入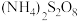 溶液时生成
溶液时生成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为________ 。
②沉淀后溶液的pH需不低于________ 。
(5)该流程中,可以循环使用的物质有________ 。
(6)某黄铜合金晶胞结构如图,其中A、B的原子坐标均可为 。与Zn原子距离最近且相等的Cu原子有
。与Zn原子距离最近且相等的Cu原子有________ 个,C的原子坐标为________ 。
 和少量
和少量 、
、 、
、 、
、 的氢氧化物)中回收铜、锌等金属的工艺流程如下图:
的氢氧化物)中回收铜、锌等金属的工艺流程如下图: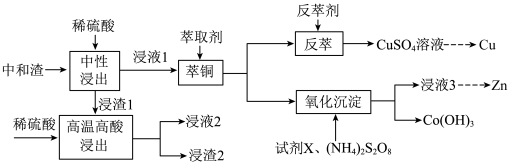
 ,几种物质的
,几种物质的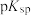 如下表
如下表物质 |
|
|
|
|
|
| 37.4 | 14.6 | 43.7 | 16.9 | 19.6 |
 时,视为沉淀完全
时,视为沉淀完全回答下列问题:
(1)“中性浸出”时,采用“中性”的目的是
(2)“高温高酸浸出”时,“浸渣2”的主要成分为
(3)“萃铜”时发生反应
 ,
,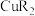 的结构简式如图所示:
的结构简式如图所示: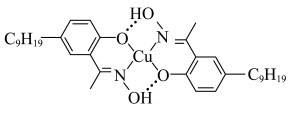
 的价层电子排布图
的价层电子排布图②
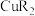 水溶性差的原因是
水溶性差的原因是a.形成分子内氢键 b.分子结构较稳定 c.亲油基团起主导作用
③萃取剂HR的结构简式为
(4)“氧化沉淀”时,试剂X用以调节溶液的pH。
①加入
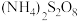 溶液时生成
溶液时生成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为②沉淀后溶液的pH需不低于
(5)该流程中,可以循环使用的物质有
(6)某黄铜合金晶胞结构如图,其中A、B的原子坐标均可为
 。与Zn原子距离最近且相等的Cu原子有
。与Zn原子距离最近且相等的Cu原子有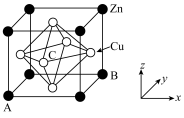
您最近一年使用:0次
6 . 钌(Ru)是地球上丰度最小的元素,钌的产品广泛应用于电子、航空航天、化工等领域。从某种失效的钌催化剂(主要成分为Ru、ZnO、 、有机物等)中回收钌的工艺流程如下:
、有机物等)中回收钌的工艺流程如下: 的沸点为40℃,温度高于108℃分解。②氧化性:
的沸点为40℃,温度高于108℃分解。②氧化性: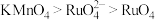
(1)“煅烧”的目的是___________ 。
(2)“氧化”过程需在650℃下熔融反应5小时。
①单质Ru被氧化为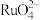 的化学方程式为
的化学方程式为___________ 。
② 固体过量会导致钌的回收率降低,原因是
固体过量会导致钌的回收率降低,原因是___________ 。
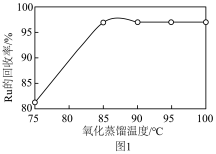
(3)“氧化蒸馏”时,测得钌的回收率随温度变化曲线如图1所示。工业上保证钌回收率较高的情况下,选择在95℃进行氧化蒸馏的原因是___________ 。___________ 。
(5)钌多活性位点催化剂(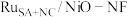 )可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
)可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。___________ 。
②催化剂的活性位点在催化过程中的主要作用是___________ 。
③分析图2-a推测 的“吸附解离”主要发生在
的“吸附解离”主要发生在___________ (填“钌原子”、“钌团簇”或“NiO”)位点上,若有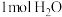 参与该过程,则变化的能量为
参与该过程,则变化的能量为___________ kJ(保留1位小数:已知: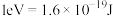 )。
)。
④分析图2-b并说明 的脱附主要发生在NiO表面的原因
的脱附主要发生在NiO表面的原因___________ 。
 、有机物等)中回收钌的工艺流程如下:
、有机物等)中回收钌的工艺流程如下: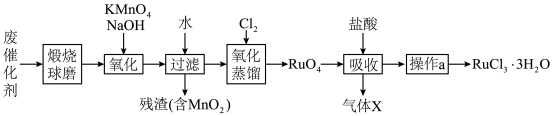
 的沸点为40℃,温度高于108℃分解。②氧化性:
的沸点为40℃,温度高于108℃分解。②氧化性: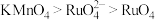
(1)“煅烧”的目的是
(2)“氧化”过程需在650℃下熔融反应5小时。
①单质Ru被氧化为
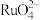 的化学方程式为
的化学方程式为②
 固体过量会导致钌的回收率降低,原因是
固体过量会导致钌的回收率降低,原因是(3)“氧化蒸馏”时,测得钌的回收率随温度变化曲线如图1所示。工业上保证钌回收率较高的情况下,选择在95℃进行氧化蒸馏的原因是
(5)钌多活性位点催化剂(
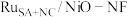 )可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
)可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
②催化剂的活性位点在催化过程中的主要作用是
③分析图2-a推测
 的“吸附解离”主要发生在
的“吸附解离”主要发生在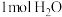 参与该过程,则变化的能量为
参与该过程,则变化的能量为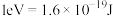 )。
)。④分析图2-b并说明
 的脱附主要发生在NiO表面的原因
的脱附主要发生在NiO表面的原因
您最近一年使用:0次
7 . 锆( )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: 、
、 、
、 ;
;
② 时,
时, ,
, ;
;
③“还原”前后相关物质沸点如下:
回答下列问题:
(1) 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是___________ 。
(2) 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式___________ 。
(3)“沉淀”后,废液中 ,则废液中
,则废液中 为
为___________  。
。
(4)“沸腾氯化”时, 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为___________ 。
(5)①气态 通常以二聚体
通常以二聚体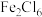 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为___________ 。 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为___________ 。
②“还原”的主要目的是___________ 。
(6)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:___________ ,继续摇动锥形瓶,观察溶液颜色变化。
②已知 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为___________  。
。
 )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: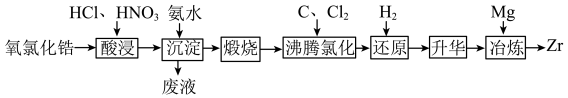
 、
、 、
、 ;
;②
 时,
时, ,
, ;
;③“还原”前后相关物质沸点如下:
| 物质 |  |  |  |  |  |
| 沸点 | 331 | 315 | 1300 | 700 | 1150 |
(1)
 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是(2)
 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式(3)“沉淀”后,废液中
 ,则废液中
,则废液中 为
为 。
。(4)“沸腾氯化”时,
 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为(5)①气态
 通常以二聚体
通常以二聚体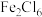 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为②“还原”的主要目的是
(6)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:

②已知
 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为 。
。
您最近一年使用:0次
2024·福建·模拟预测
解题方法
8 . 双氰胺( )为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮
)为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮 为原料制备双氰胺的流程如下:
为原料制备双氰胺的流程如下:


(1)已知:氰基是吸电子基团。氰氨
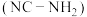 的碱性
的碱性(2)写出步骤Ⅰ的化学反应方程式:
(3)步骤Ⅱ中调节溶液pH为9.1,pH不能过低的原因:
(4)步骤Ⅲ中蒸发浓缩时,常采用真空蒸发浓缩,目的是
(5)凯氏定氮法是测定有机物中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐。
已知:
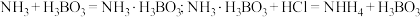

②仪器清洗后,g中加入硼酸
 和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭
和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭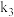 ,d中保留少量水。打开
,d中保留少量水。打开 ,加热b,使水蒸气进入e。d中保留少量水的目的是
,加热b,使水蒸气进入e。d中保留少量水的目的是③取双氰胺样品m克进行测定,滴定g中吸收液时消耗浓度为
 的盐酸VmL,则样品中氮的质量分数为
的盐酸VmL,则样品中氮的质量分数为
您最近一年使用:0次
名校
解题方法
9 . 钴镍渣是湿法炼锌净化渣之一,其中含有较多的Zn(Ⅱ)、Cd(Ⅱ)和少量Co(Ⅱ)、Fe(Ⅱ)、Ni(Ⅱ)的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为+2价)。利用以下工艺流程回收金属并制备碱式碳酸锌:
(1)“溶浸”中,可以加快化学反应速率的措施有________ (任写一种)。
(2)向“浸取液”中加入Zn粉,发生反应的离子方程式为________ 。
(3)过二硫酸根具有极强的氧化性,原因是________ 。
(4)“氧化、沉钴”时,加入 溶液并调节溶液pH至5.0~5.2,反应生成
溶液并调节溶液pH至5.0~5.2,反应生成 沉淀的离子方程式为
沉淀的离子方程式为________ 。
(5)研究加入 溶液时温度和时间对金属脱除率的影响,所得曲线如下图所示:
溶液时温度和时间对金属脱除率的影响,所得曲线如下图所示:________ 。金属脱除是指溶液中的二价金属离子被氧化后形成氢氧化物沉淀除去, 滤渣中还含有
滤渣中还含有________ (填化学式)。
(6)向 溶液中加入适量的
溶液中加入适量的 溶液,反应生成
溶液,反应生成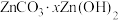 沉淀的化学方程式为
沉淀的化学方程式为________ 。
(7)锌的某些硫化物具有独特的光电效应,被研究应用于荧光材料、电磁学等领域。如图为锌的某种硫化物晶体的晶胞结构。 的价层电子排布图为
的价层电子排布图为________ 。
②该硫化物晶体的密度ρ=________  (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。

已知:过二硫酸根( )的结构式为
)的结构式为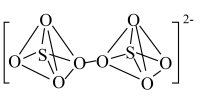 ,
, 的还原产物为
的还原产物为 。
。
(1)“溶浸”中,可以加快化学反应速率的措施有
(2)向“浸取液”中加入Zn粉,发生反应的离子方程式为
(3)过二硫酸根具有极强的氧化性,原因是
(4)“氧化、沉钴”时,加入
 溶液并调节溶液pH至5.0~5.2,反应生成
溶液并调节溶液pH至5.0~5.2,反应生成 沉淀的离子方程式为
沉淀的离子方程式为(5)研究加入
 溶液时温度和时间对金属脱除率的影响,所得曲线如下图所示:
溶液时温度和时间对金属脱除率的影响,所得曲线如下图所示:
 滤渣中还含有
滤渣中还含有(6)向
 溶液中加入适量的
溶液中加入适量的 溶液,反应生成
溶液,反应生成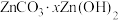 沉淀的化学方程式为
沉淀的化学方程式为(7)锌的某些硫化物具有独特的光电效应,被研究应用于荧光材料、电磁学等领域。如图为锌的某种硫化物晶体的晶胞结构。
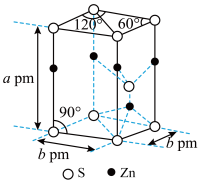
 的价层电子排布图为
的价层电子排布图为②该硫化物晶体的密度ρ=
 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-04-16更新
|
456次组卷
|
2卷引用:福建省南平市2024届高三联考(一模)化学试题
名校
解题方法
10 . 连二亚硫酸钠( )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ. 的制备
的制备 时选用上图所示装置中的
时选用上图所示装置中的________ (填标号)。选用以下试剂中的________ (填标号)。
A.铜粉 B. 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
Ⅱ. 的制备
的制备
制用如图所示实验装置(加热、搅拌及夹持装置省略)制备 ,实验步骤如下:
,实验步骤如下: 一段时间;
一段时间;
ii.然后持续通入 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;
iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入 的目的是
的目的是________ (答出两点)。
(3)装置d中发生的主要反应的化学方程式为________ 。
(4)步骤iv中“洗涤”时,洗涤剂为________ (填“水”或“乙醇”),进一步提纯 的方法为
的方法为________ 。
Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用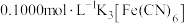 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
(5)滴定过程中发生反应的离子方程式为________ 。
(6)产品中 的质量分数为
的质量分数为________ 。
(7)下列情况会造成测定结果偏小的是________ (填标号)。
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用 标准液润洗酸式滴定管
标准液润洗酸式滴定管
C.滴定终点时俯视读数
 )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ.
 的制备
的制备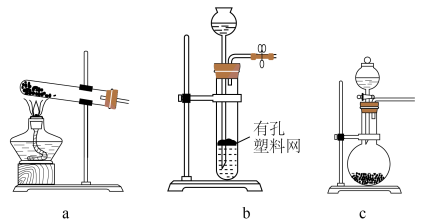
 时选用上图所示装置中的
时选用上图所示装置中的A.铜粉 B.
 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸Ⅱ.
 的制备
的制备制用如图所示实验装置(加热、搅拌及夹持装置省略)制备
 ,实验步骤如下:
,实验步骤如下: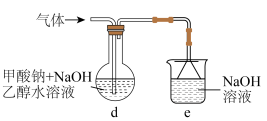
 一段时间;
一段时间;ii.然后持续通入
 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入
 的目的是
的目的是(3)装置d中发生的主要反应的化学方程式为
(4)步骤iv中“洗涤”时,洗涤剂为
 的方法为
的方法为Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量
 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用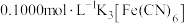 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。(5)滴定过程中发生反应的离子方程式为
(6)产品中
 的质量分数为
的质量分数为(7)下列情况会造成测定结果偏小的是
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用
 标准液润洗酸式滴定管
标准液润洗酸式滴定管C.滴定终点时俯视读数
您最近一年使用:0次
2024-04-16更新
|
325次组卷
|
2卷引用:福建省南平市2024届高三联考(一模)化学试题







