1 . 完成下列问题
(1)①硫酸钡的化学式_______ ;
②乙醇的结构简式_______ 。
(2)氯化铁溶液腐蚀覆铜板的离子方程式为_______ 。
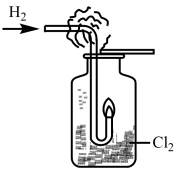
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:_______ 。
(1)①硫酸钡的化学式
②乙醇的结构简式
(2)氯化铁溶液腐蚀覆铜板的离子方程式为
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:

您最近一年使用:0次
解题方法
2 . 实验室用MnO2和浓盐酸反应制取Cl2,并进行Cl2性质的探究,发生装置如图①。

回答下列问题:
(1)仪器甲的名称是_______ 。
(2)制得的气体除去HCl杂质后,为得到干燥的Cl2,应通过_______ 装置(填“②”、“③”或“④”)。

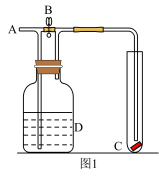
(3)如图1,若在A处通入未干燥的氯气,当关闭B处弹簧夹时,C处的红布条看不到明显现象,当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是_______。
(4)如图2能证明氯水具有漂白性的是_______ (填“a”、“b”、“c”或“d”),其现象为_______ 。


回答下列问题:
(1)仪器甲的名称是
(2)制得的气体除去HCl杂质后,为得到干燥的Cl2,应通过

(3)如图1,若在A处通入未干燥的氯气,当关闭B处弹簧夹时,C处的红布条看不到明显现象,当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是_______。

| A.饱和食盐水 | B.NaOH溶液 | C.H2O | D.浓硫酸 |

您最近一年使用:0次
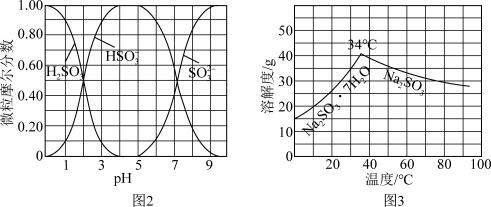
3 . 以Cl2、NaOH、CO(NH2)2 (尿素)和SO2为原料可制备N2H4∙H2O (水合肼)和无水Na2SO3,NaHSO3水溶液中含硫微粒随 的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
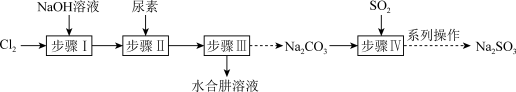
已知:
①Cl2+2OH-=Cl-+ClO-+H2O是放热反应,超过40℃发生副反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ用Cl2通入NaOH溶液制备NaClO溶液,Cl2需要缓慢通入的原因:_________________
(2)步骤Ⅱ合成N2H4∙H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应,使用冷凝管和迅速升温的目的分别是:__________

(3)关于实验操作下列说法正确的是______________。
(4)请补充完整由NaHSO3溶液制备较纯的无水Na2SO3的实验方案:
边搅拌边向NaHSO3溶液中滴加NaOH溶液→_______ →_______ →_______ 用少量无水乙醇洗涤、干燥,包装。
a.调节 至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
e.蒸发浓缩至有晶膜产生,冷却结晶 f.调节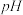 至7
至7
(5)①经某学习小组测定,Na2SO3中含有NaCl杂质,试分析杂质产生的原因:________
②产品的纯度是产品质量的重要指标,该小组同学利用cmol/L的KMnO4测定产品中Na2SO3的含量,装置如图,当酸性KMnO4与Na2SO3恰好完全反应时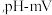 计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化
计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化 ):
):
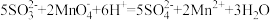
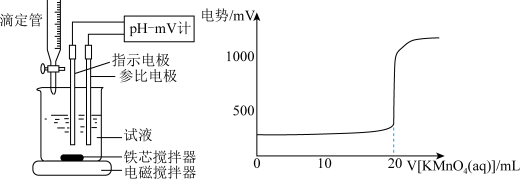
具体流程如下:称量ag样品,加入煮沸后冷却的蒸馏水溶解,配制为250mL的溶液,用碱式滴定管取25.00mL样品溶液于烧杯中,用cmol/L的KMnO4滴定,滴定曲线如图。则样品中Na2SO3纯度的表达式为:________________
 的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:

已知:
①Cl2+2OH-=Cl-+ClO-+H2O是放热反应,超过40℃发生副反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ用Cl2通入NaOH溶液制备NaClO溶液,Cl2需要缓慢通入的原因:
(2)步骤Ⅱ合成N2H4∙H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应,使用冷凝管和迅速升温的目的分别是:

(3)关于实验操作下列说法正确的是______________。
| A.步骤Ⅱ中通过滴液漏斗滴加NaClO溶液 |
| B.步骤Ⅲ为了得到较高浓度的水合肼,可以向水合肼溶液中加入NaOH,减压蒸馏 |
| C.步骤Ⅳ中边搅拌边向Na2CO3溶液中通入SO2至pH约为4时,即可以停止通入SO2 |
| D.为了快速得到无水Na2CO3,可以将产品烘干 |
边搅拌边向NaHSO3溶液中滴加NaOH溶液→
a.调节
 至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出e.蒸发浓缩至有晶膜产生,冷却结晶 f.调节
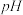 至7
至7(5)①经某学习小组测定,Na2SO3中含有NaCl杂质,试分析杂质产生的原因:
②产品的纯度是产品质量的重要指标,该小组同学利用cmol/L的KMnO4测定产品中Na2SO3的含量,装置如图,当酸性KMnO4与Na2SO3恰好完全反应时
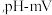 计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化
计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化 ):
):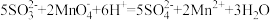

具体流程如下:称量ag样品,加入煮沸后冷却的蒸馏水溶解,配制为250mL的溶液,用碱式滴定管取25.00mL样品溶液于烧杯中,用cmol/L的KMnO4滴定,滴定曲线如图。则样品中Na2SO3纯度的表达式为:
您最近一年使用:0次
解题方法
4 . 某工厂废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
已知:还原性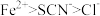
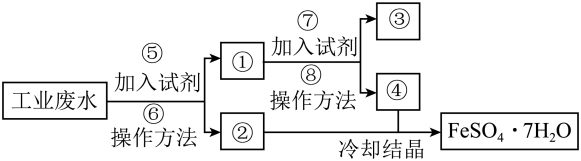
(1)溶液④中溶质的成分为_______ (用化学式表示),操作方法⑥为_______ 。
(2)若取2mL溶液④加入试管中,然后滴入氢氧化钠溶液,产生的现象为_______ ;此过程中属于氧化还原反应的化学方程式是_______ 。
(3)检验溶液②中的金属阳离子时要控制氧化剂用量,若氧化剂过量可能产生的现象是_______ ,请说明产生现象的原因:_______ 。
(4)产品取样研究:取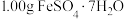 产品加水溶解,滴加
产品加水溶解,滴加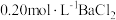 溶液至不再产生沉淀,共消耗
溶液至不再产生沉淀,共消耗 溶液20.00mL,产品的质量分数是
溶液20.00mL,产品的质量分数是_______ ,引起误差的可能原因是_______ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:已知:还原性
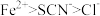

(1)溶液④中溶质的成分为
(2)若取2mL溶液④加入试管中,然后滴入氢氧化钠溶液,产生的现象为
(3)检验溶液②中的金属阳离子时要控制氧化剂用量,若氧化剂过量可能产生的现象是
(4)产品取样研究:取
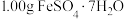 产品加水溶解,滴加
产品加水溶解,滴加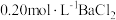 溶液至不再产生沉淀,共消耗
溶液至不再产生沉淀,共消耗 溶液20.00mL,产品的质量分数是
溶液20.00mL,产品的质量分数是
您最近一年使用:0次
解题方法
5 . 为提纯下列物质(括号内为杂质),所用的除杂试剂正确的是
| 序号 | 不纯物 | 除杂试剂 |
| A | CH4(C2H4) | 酸性 溶液 溶液 |
| B | Cl2(HCl) | 饱和 溶液 溶液 |
| C | 乙酸乙酯(乙酸) | 饱和 溶液 溶液 |
| D | SO2(SO3) | 硝酸钡溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-28更新
|
201次组卷
|
2卷引用:浙江省强基联盟2021-2022学年高一下学期5月份联考化学试题
名校
解题方法
6 . 当25℃时,向20.00mL某浓度新制氯水中滴入 的NaOH溶液,滴定曲线如图所示,已知次氯酸的电离常数为Ka=2.5×10-8。下列说法正确的是
的NaOH溶液,滴定曲线如图所示,已知次氯酸的电离常数为Ka=2.5×10-8。下列说法正确的是

 的NaOH溶液,滴定曲线如图所示,已知次氯酸的电离常数为Ka=2.5×10-8。下列说法正确的是
的NaOH溶液,滴定曲线如图所示,已知次氯酸的电离常数为Ka=2.5×10-8。下列说法正确的是
| A.甲到乙发生的非氧化还原反应主要为:HClO+OH-=H2O+ClO- |
| B.甲到丁的过程中,水的电离程度一直增大 |
| C.丙点溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(HClO)>c(H+) |
D.氯水中存在平衡:Cl2+H2O HCl+HClO,其平衡常数K的数量级为10-4 HCl+HClO,其平衡常数K的数量级为10-4 |
您最近一年使用:0次
2022-05-28更新
|
518次组卷
|
5卷引用:浙江省杭州第二中学等三校2021-2022学年高三下学期5月份模拟检测化学试题
浙江省杭州第二中学等三校2021-2022学年高三下学期5月份模拟检测化学试题浙江省杭州二中、温州中学、金华一中2021-2022学年高三下学期模拟化学试题(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
7 . 下列实验对应的离子方程式不正确的是
A.铬酸钾溶液中滴入浓盐酸: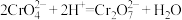 |
B.过量铁粉与稀硝酸反应: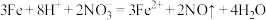 |
C.用 溶液吸收少量 溶液吸收少量 : : |
D.澄清石灰水中通入过量的二氧化碳: |
您最近一年使用:0次
8 . 回答下列问题
(1)写出乙醛的结构简式_______
(2)用电子式表示CO2的形成过程_______
(3)写出氯气与水反应的离子方程式_______
(4)写出铝片溶于氢氧化钠溶液发生的化学方程式_______
(1)写出乙醛的结构简式
(2)用电子式表示CO2的形成过程
(3)写出氯气与水反应的离子方程式
(4)写出铝片溶于氢氧化钠溶液发生的化学方程式
您最近一年使用:0次
解题方法
9 . 对于下列实验,能正确描述其反应的离子方程式是
A.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
| B.CuCl溶于氨水:Cu++2NH3•H2O=[Cu(NH3)2]++2H2O |
C.用铝粉和NaOH溶液反应制取少量H2:Al+2OH-=AlO +H2↑ +H2↑ |
| D.同浓度同体积NH4HSO3溶液与NaOH溶液混合:H++OH-=H2O |
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的值,下列说法不正确的是
A.将22.4L (标准状况下)通入水中,所得溶液中: (标准状况下)通入水中,所得溶液中: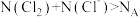 |
B.11.2L的甲烷和22.4L的 (均为标准状况)在光照下充分反应后分子数为1.5NA (均为标准状况)在光照下充分反应后分子数为1.5NA |
C.向常温常压下密闭容器投入2molNO与 ,使其充分反应,产物的分子数小于2NA ,使其充分反应,产物的分子数小于2NA |
D.31g (分子结构: (分子结构: )中的共价键数目为1.5NA )中的共价键数目为1.5NA |
您最近一年使用:0次



