名校
解题方法
1 . 如图为铁及其化合物的“价一类”二维图。

(1)填写二维图缺失的化学式②_______ 。
(2)利用以下试剂研究 性质,进行了如下预测:
性质,进行了如下预测:
a. b.
b. c.
c. d.
d. e.
e.
从物质类别上看, 属于盐,可能与
属于盐,可能与_______ 发生反应(填序号);从化合价角度看,体现 氧化性,可能与
氧化性,可能与_______ 反应(填序号)。
(3) 具有较强的还原性,容易被一些氧化剂氧化为
具有较强的还原性,容易被一些氧化剂氧化为 。
。
①向 溶液中加入
溶液中加入 溶液,无明显现象,再加入氯水,溶液变血红色。
溶液,无明显现象,再加入氯水,溶液变血红色。 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
②配制含 的溶液时,为防止
的溶液时,为防止 被氧化,应采取的措施是
被氧化,应采取的措施是_______ 。
(4)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成 胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为 ,每生成
,每生成 该气体,
该气体, 转移的电子数目为
转移的电子数目为_______ 。

(1)填写二维图缺失的化学式②
(2)利用以下试剂研究
 性质,进行了如下预测:
性质,进行了如下预测:a.
 b.
b. c.
c. d.
d. e.
e.
从物质类别上看,
 属于盐,可能与
属于盐,可能与 氧化性,可能与
氧化性,可能与(3)
 具有较强的还原性,容易被一些氧化剂氧化为
具有较强的还原性,容易被一些氧化剂氧化为 。
。①向
 溶液中加入
溶液中加入 溶液,无明显现象,再加入氯水,溶液变血红色。
溶液,无明显现象,再加入氯水,溶液变血红色。 与
与 反应的离子方程式为
反应的离子方程式为②配制含
 的溶液时,为防止
的溶液时,为防止 被氧化,应采取的措施是
被氧化,应采取的措施是(4)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成
 胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为 ,每生成
,每生成 该气体,
该气体, 转移的电子数目为
转移的电子数目为
您最近一年使用:0次
名校
2 . 铁在地壳中含量丰富,也是重要的人体微量元素之一
Ⅰ.如图所示装置可用来制取和观察 在空气中被氧化时颜色的变化。实验时必须使用铁屑和
在空气中被氧化时颜色的变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。填写下列空白:
的硫酸,其他试剂任选。填写下列空白:

(1)B中盛一定量的NaOH溶液,A中应预先加入的试剂是_______ 。实验开始时先将止水夹E打开,C中收集到气体的主要成分是_______ 。
(2)关闭止水夹E,A中压强增大,把 溶液压入B瓶中进行反应。生成沉淀的离子方程式为
溶液压入B瓶中进行反应。生成沉淀的离子方程式为_______ 。
(3)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:_______ 。
Ⅱ.验证菠菜中铁元素的存在。
(4)①取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以_______ (填离子符号)形式存在。
②另取新鲜菠菜洗净、烘干,放入坩埚中灼烧成灰烬。冷却后将灰烬移入烧杯中,加入 溶液至没有气体产生,加蒸馏水稀释,充分搅拌后过滤。取少量滤液于试管中,加入KSCN溶液,溶液变为
溶液至没有气体产生,加蒸馏水稀释,充分搅拌后过滤。取少量滤液于试管中,加入KSCN溶液,溶液变为_______ 色,由此推断滤液中有 。实验中加入
。实验中加入 溶液的目的为
溶液的目的为_______ 。
(5)为了防止缺铁性贫血,一些食品中允许添加含铁物质。某种麦片含有微量的还原铁粉,铁粉在胃酸的作用下会溶解。铁与盐酸反应的离子方程式为_______ 。
Ⅰ.如图所示装置可用来制取和观察
 在空气中被氧化时颜色的变化。实验时必须使用铁屑和
在空气中被氧化时颜色的变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。填写下列空白:
的硫酸,其他试剂任选。填写下列空白:
(1)B中盛一定量的NaOH溶液,A中应预先加入的试剂是
(2)关闭止水夹E,A中压强增大,把
 溶液压入B瓶中进行反应。生成沉淀的离子方程式为
溶液压入B瓶中进行反应。生成沉淀的离子方程式为(3)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:
Ⅱ.验证菠菜中铁元素的存在。
(4)①取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以
②另取新鲜菠菜洗净、烘干,放入坩埚中灼烧成灰烬。冷却后将灰烬移入烧杯中,加入
 溶液至没有气体产生,加蒸馏水稀释,充分搅拌后过滤。取少量滤液于试管中,加入KSCN溶液,溶液变为
溶液至没有气体产生,加蒸馏水稀释,充分搅拌后过滤。取少量滤液于试管中,加入KSCN溶液,溶液变为 。实验中加入
。实验中加入 溶液的目的为
溶液的目的为(5)为了防止缺铁性贫血,一些食品中允许添加含铁物质。某种麦片含有微量的还原铁粉,铁粉在胃酸的作用下会溶解。铁与盐酸反应的离子方程式为
您最近一年使用:0次
名校
3 . 下列各组物质反应后,滴入KSCN溶液,显红色的是
①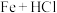 ;②
;② 溶液
溶液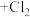 ;③
;③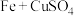 溶液;④
溶液;④ 稀
稀
①
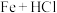 ;②
;② 溶液
溶液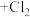 ;③
;③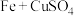 溶液;④
溶液;④ 稀
稀
| A.②④ | B.①② | C.③④ | D.①④ |
您最近一年使用:0次
2022-12-07更新
|
181次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高一上学期第二次月考化学试题
名校
解题方法
4 . 为除去括号内的杂质,所选用的试剂或方法错误的是
A. 溶液(NaHCO3):加入适量 溶液(NaHCO3):加入适量 |
B. 粉末(Na2O):将混合物放在氧气中加热 粉末(Na2O):将混合物放在氧气中加热 |
C. 溶液 (FeCl3):加入适量铜粉 溶液 (FeCl3):加入适量铜粉 |
| D.Fe2O3(NaCl):加入足量水,过滤 |
您最近一年使用:0次
2022-12-07更新
|
173次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高一上学期第二次月考化学试题
5 . 打印机墨粉中的Fe3O4含量是衡量墨粉质量优劣的重要指标之一,为测定墨粉中Fe3O4的含量,进行了如下实验:

已知:①墨粉中除了Fe3O4晶体粉粒外,其余成分均不溶于水且不与酸反应,
②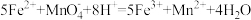 。下列有关说法正确的是
。下列有关说法正确的是

已知:①墨粉中除了Fe3O4晶体粉粒外,其余成分均不溶于水且不与酸反应,
②
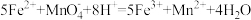 。下列有关说法正确的是
。下列有关说法正确的是| A.试剂是Zn粉,且要缓慢加入至观察到较多气泡产生时停止加入Zn粉 |
B.用 溶液能检验溶液②只含有Fe2+ 溶液能检验溶液②只含有Fe2+ |
| C.若溶解过滤后没有洗涤,则Fe3O4含量测定结果偏大 |
D.墨粉中的Fe3O4的含量为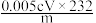 |
您最近一年使用:0次
名校
解题方法
6 . 无水FeCl3常作为有机反应的催化剂。某研究小组设计了如图流程,以废铁屑(含有少量碳和SiO2杂质)为原料制备无水FeCl3(s)。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易与水反应生成一种强酸和一种酸性氧化物。
)熔点-101℃,沸点76℃,易与水反应生成一种强酸和一种酸性氧化物。

回答问题:
(1)操作①的名称是_______ ,用到的玻璃仪器有烧杯、玻璃棒和_______ 。
(2)操作①得到的固体为_______ 。
(3)为避免引入新的杂质,试剂B可以选用_______(填编号)。
(4)取少量D晶体,溶于浓盐酸配成溶液,并滴加KSCN溶液,现象是_______ 。
(5)反应D→E的化学方程式为_______ 。
(6)由D转化成E的过程中可能产生少量亚铁盐,则还原剂可能是_______ ,并设计实验验证是该还原剂将Fe3+还原_______ 。
已知:氯化亚砜(
 )熔点-101℃,沸点76℃,易与水反应生成一种强酸和一种酸性氧化物。
)熔点-101℃,沸点76℃,易与水反应生成一种强酸和一种酸性氧化物。
回答问题:
(1)操作①的名称是
(2)操作①得到的固体为
(3)为避免引入新的杂质,试剂B可以选用_______(填编号)。
| A.KMnO4溶液 | B.Cl2水 | C.稀HNO3溶液 | D.H2O2溶液 |
(5)反应D→E的化学方程式为
(6)由D转化成E的过程中可能产生少量亚铁盐,则还原剂可能是
您最近一年使用:0次
2022-09-07更新
|
387次组卷
|
2卷引用:福建省龙岩市上杭县第一中学2022-2023学年高三上学期12月月考化学试题
解题方法
7 . 下列离子方程式书写正确的是
A.碳酸钙与稀盐酸: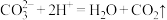 |
B. 溶液中加入足量的 溶液中加入足量的 : :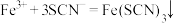 |
C.金属 与水反应: 与水反应: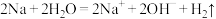 |
D.氢氧化钡溶液与稀硫酸混合: |
您最近一年使用:0次
名校
解题方法
8 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入
和空气的混合气体通入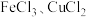 和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是
和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是

 和空气的混合气体通入
和空气的混合气体通入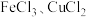 和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是
和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是
A.历程①发生反应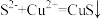 |
| B.历程②中CuS作氧化剂 |
C.历程③中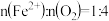 |
D.若要吸收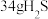 ,则至少要通入标准状况下56L空气(空气中氧气体积按20%计) ,则至少要通入标准状况下56L空气(空气中氧气体积按20%计) |
您最近一年使用:0次
2022-08-27更新
|
713次组卷
|
11卷引用:福建省龙岩第一中学2022-2023学年高三上学期第二次月考化学试题
福建省龙岩第一中学2022-2023学年高三上学期第二次月考化学试题河南省平顶山市、安阳市部分学校2022-2023学年高三上学期开学考试化学试题湖南省三湘创新发展联合2022-2023学年高三上学期起点调研考试化学试题广东省百校2023届高三上学期8月月考化学试题河南省洛阳市洛宁县第一高级中学2022-2023学年高三上学期开学考试化学试题河北省深州市中学2022-2023学年高三上学期第二次月考化学试题辽宁省渤海大学附属高级中学2022-2023学年高三上学期第二次月考化学试题湖南省邵东市第一中学2022-2023学年高三上学期第二次月考化学试题辽宁省鞍山市第一中学2022-2023学年高三上学期第二次模拟考试化学试题湖南省株洲市攸县第三中学2022-2023学年高三上学期第二次月考化学试题河南省安阳市第一中学2023届高三上学期10月月考化学试题
9 . 硫酸亚铁在印染、医药、化肥等多个行业有广泛应用。某学习小组对硫酸亚铁晶体 的热分解产物进行探究。回答下列问题:
的热分解产物进行探究。回答下列问题:
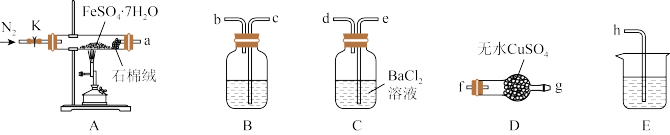
(1)装置A中石棉绒的作用为__________ 。
(2)按气流方向,上述装置合理的连接顺序为a→f、g→_____ →h(填装置口小写字母)。
(3)该小组同学按上述顺序连接各装置并进行实验,请为他们补全表格:
(4)硫酸亚铁晶体分解的化学方程式为_________ 。
(5)设计实验证明A中得到的红色粉末不含+2价铁元素:_______ (简述实验操作及现象)。
 的热分解产物进行探究。回答下列问题:
的热分解产物进行探究。回答下列问题:
(1)装置A中石棉绒的作用为
(2)按气流方向,上述装置合理的连接顺序为a→f、g→
(3)该小组同学按上述顺序连接各装置并进行实验,请为他们补全表格:
| 装置编号 | 填装试剂 | 实验现象 | 实验结论 |
| A | FeSO4·7H2O | 绿色固体逐渐变为红色粉末 | — |
| B | ① | ② | 分解产物中含有SO2 |
| C | BaCl2溶液 | 产生白色沉淀 | ③ |
| D | 无水CuSO4粉末 | 白色固体逐渐变为蓝色 | 分解产物中含有水蒸气 |
| E | ④ | — | — |
(5)设计实验证明A中得到的红色粉末不含+2价铁元素:
您最近一年使用:0次
2022-08-13更新
|
166次组卷
|
2卷引用:福建省龙岩北大附属实验学校2022-2023学年高三上学期第一次月考(平衡班)化学试题
名校
解题方法
10 . 印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显_______ (填“红色”或“蓝色”、“紫色”),证明废液含有FeCl3。
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是_______ (填化学式)。
(3)操作Ⅰ是_______ ,该操作需用到的玻璃仪器有烧杯、普通漏斗和_______ 。
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为_______ 。
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生_______ (填“是”、“否”)。

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是
(3)操作Ⅰ是
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生
您最近一年使用:0次



