解题方法
1 . 以锌灰(含ZnO及少量PbO、CuO、Fe2O3、SiO2)和Fe2(SO4)3为原料制备的ZnFe2O4脱硫剂,可用于脱除煤气中的H2S。脱硫剂的制备过程可表示为
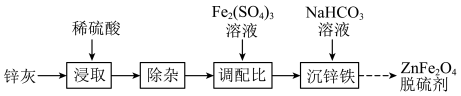
(1)“浸取”时需不断通入高温水蒸气,其目的是___________ 。
(2)“除杂”包括:向浸取后的滤液中加足量锌粉、过滤、加H2O2氧化等步骤。过滤所得滤渣的成分为(填化学式)___________ 。
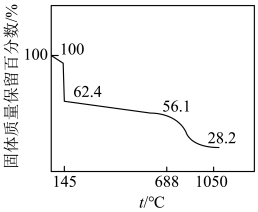
(3)ZnSO4溶液经结晶可得ZnSO4∙7H2O固体。加热该固体,固体质量保留百分数与温度的关系如图所示。温度从688℃升高到1050℃时,分解生成的产物中有两种气体(只有一种是氧化物),该过程中发生反应的化学方程式为___________ 。
(4)400℃时,将一定比例H2、H2S的混合气体以一定流速通过装有ZnFe2O4脱硫剂的硫化反应器进行硫化。已知:硫化过程中ZnFe2O4反应后生成ZnS和FeS,该过程中发生的化学反应方程式为______________________ 。
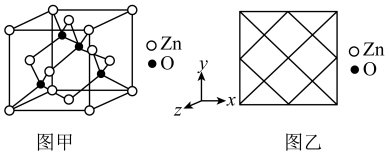
(5)①氧化锌晶体的一种晶胞是如图甲所示的立方晶胞,其中与Zn原子距离最近的O原子数目有___________ 个,请在图乙中画出该晶胞沿y轴方向的平面投影图___________ 。
②Zn2+能形成多种配离子,已知Zn2+形成的一种配离子[Zn(NH3)2(H2O)2]2+只有一种空间结构,则[Zn(NH3)4]2+的空间结构为___________ 。

(1)“浸取”时需不断通入高温水蒸气,其目的是
(2)“除杂”包括:向浸取后的滤液中加足量锌粉、过滤、加H2O2氧化等步骤。过滤所得滤渣的成分为(填化学式)
(3)ZnSO4溶液经结晶可得ZnSO4∙7H2O固体。加热该固体,固体质量保留百分数与温度的关系如图所示。温度从688℃升高到1050℃时,分解生成的产物中有两种气体(只有一种是氧化物),该过程中发生反应的化学方程式为

(4)400℃时,将一定比例H2、H2S的混合气体以一定流速通过装有ZnFe2O4脱硫剂的硫化反应器进行硫化。已知:硫化过程中ZnFe2O4反应后生成ZnS和FeS,该过程中发生的化学反应方程式为
(5)①氧化锌晶体的一种晶胞是如图甲所示的立方晶胞,其中与Zn原子距离最近的O原子数目有

②Zn2+能形成多种配离子,已知Zn2+形成的一种配离子[Zn(NH3)2(H2O)2]2+只有一种空间结构,则[Zn(NH3)4]2+的空间结构为
您最近一年使用:0次
解题方法
2 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向[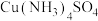 ]溶液中加入乙醇,析出深蓝色固体 ]溶液中加入乙醇,析出深蓝色固体 | [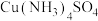 ]与乙醇反应生成了难溶于水的物质 ]与乙醇反应生成了难溶于水的物质 |
| B | 向 溶液中滴加几滴KSCN溶液,振荡,无明显现象,再滴加几滴新制氯水,溶液变红 溶液中滴加几滴KSCN溶液,振荡,无明显现象,再滴加几滴新制氯水,溶液变红 | 一定是 将 将 氧化为 氧化为 |
| C | 向蔗糖溶液中加入稀硫酸,加热。待溶液冷却后向其中加入少量新制 ,加热未产生砖红色沉淀 ,加热未产生砖红色沉淀 | 蔗糖没有发生水解 |
| D | 向溴水中加入植物油,振荡后静置,水层颜色变浅,油层呈无色 |  与植物油发生了反应 与植物油发生了反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某学习小组欲探究氯气与铁的反应及产物中铁元素的价态,设计并实施了以下实验.
已知: 的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
Ⅰ.氯气与铁的反应
按下图连接装置并进行制备实验.
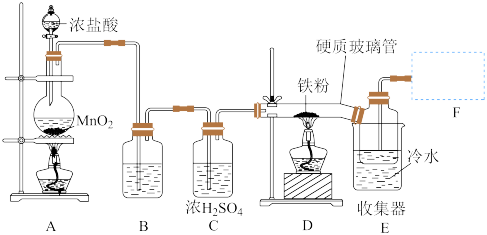
(1)按上图连接好装置,在进行______ 操作后,在各仪器中装入对应的试剂;开始反应时,应先点燃______ 装置的酒精灯(填“A”或“D”)。
(2)写出A中反应的离子方程式______ 。
(3)装置B的作用是______ .F应连接的装置是______ (选择其中一个装置,填相应的字母)。
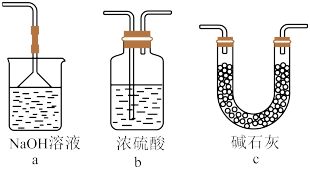
Ⅱ.产物中铁元素价态探究
反应结束后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,该小组设计了以下实验探究产物中铁元素的价态.
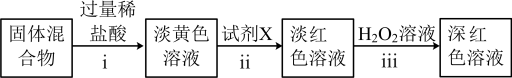
(4)步骤ⅱ添加的试剂X为______ 。
(5)步骤ⅲ中所发生的离子反应方程式为______ 。
(6)通过以上实验及现象,该小组同学认为氯气与铁的反应产物中包含+2和+3价的两种铁盐.实验结论是否正确?请进行判断并说明理由______ 。
已知:
 的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.Ⅰ.氯气与铁的反应
按下图连接装置并进行制备实验.

(1)按上图连接好装置,在进行
(2)写出A中反应的离子方程式
(3)装置B的作用是

Ⅱ.产物中铁元素价态探究
反应结束后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,该小组设计了以下实验探究产物中铁元素的价态.

(4)步骤ⅱ添加的试剂X为
(5)步骤ⅲ中所发生的离子反应方程式为
(6)通过以上实验及现象,该小组同学认为氯气与铁的反应产物中包含+2和+3价的两种铁盐.实验结论是否正确?请进行判断并说明理由
您最近一年使用:0次
名校
4 . 下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
| 物质(括号内为杂质) | 除杂试剂 | |
| A | FeCl2溶液(FeCl3) | Fe粉 |
| B | FeCl3溶液(FeCl2) | 氯水 |
| C | Cl2(HCl) | 饱和食盐水、浓H2SO4 |
| D | SO2(SO3) | 饱和小苏打溶液、无水CaCl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 在硫酸铁溶液中同时加入铁粉和铜粉,充分反应后不会出现的结果是
| A.铁铜均有 | B.铁铜均无 | C.有铜无铁 | D.有铁无铜 |
您最近一年使用:0次
2024-02-04更新
|
125次组卷
|
10卷引用:福建省连城县第一中学2021-2022学年高一上学期第二次月考化学试题
福建省连城县第一中学2021-2022学年高一上学期第二次月考化学试题山东省泰安市新泰市第一中学北校2020-2021学年高一上学期第二次考试化学试题浙江省金华市金华十校2020-2021学年高一上学期调研考试化学试题(已下线)【浙江新东方】双师134河南省郑州市第四十七高级中学2021-2022学年高一上学期第二次月考化学试题2019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题山东省枣庄市2022-2023学年高一上学期期末考试化学试题山东省枣庄市薛城区2022-2023学年高一上学期学科素养诊断化学试题河南省实验中学2023-2024学年高一上学期月考 化学试卷山东省济南市2023-2024学年高一上学期1月期末考试化学试题
名校
6 . 铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是___________。
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,___________ 。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有___________ (填化学性质)。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:___________
______Fe(OH)3+_______ClO-+_______=_______FeO +_______Cl-+_______
+_______Cl-+_______
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是___________ ,操作I用到的玻璃仪器有烧杯、玻璃棒和___________ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________ 。
③上述流程中操作Ⅲ包括:蒸发浓缩、___________ 、过滤、洗涤。
(1)所含铁元素只有还原性的物质是___________。
| A.Fe | B.FeCl2 | C.FeCl3 | D.Fe2O3 |
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO
 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:______Fe(OH)3+_______ClO-+_______=_______FeO
 +_______Cl-+_______
+_______Cl-+_______(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作Ⅲ包括:蒸发浓缩、
您最近一年使用:0次
名校
解题方法
7 . 室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向苯酚钠溶液中通入CO2,观察现象 | 探究碳酸和苯酚的酸性强弱 |
| B | 用pH计分别测定等体积的CH3COOH溶液和ClCH2COOH溶液的pH | 探究键的极性对羧酸酸性的影响 |
| C | 向圆底烧瓶中加入2.0gNaOH、15mL无水乙醇、碎瓷片和5mL1-溴丁烷,微热,将产生的气体通入酸性KMnO4溶液,观察现象 | 探究1-溴丁烷的消去产物 |
| D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,观察溶液颜色变化 | 探究H2O2与Fe3+氧化性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列方程式正确的是
A. 与NaOH溶液反应: 与NaOH溶液反应: |
B.KSCN溶液检验 : : |
C. 在高温条件下与 在高温条件下与 反应: 反应: |
D.红热的铁丝伸入充满氯气的集气瓶中: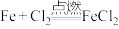 |
您最近一年使用:0次
名校
9 . 某实验小组为了探究铁及其化合物的有关性质设计了如下实验:

现象Ⅱ:生成白色沉淀,3min后沉淀基本变为红褐色
现象Ⅲ:生成白色沉淀,3min后沉淀颜色几乎不变
(1)实验I中的现象为_______ ,该现象说明 具有
具有_______ 性,确定滤液A中不含 操作及现象为
操作及现象为_______ 。
(2)用化学方程式表示“现象Ⅱ”中沉淀由白色变为红褐色的原因_______ 。
(3)探究“现象Ⅲ”中白色沉淀的组成:
①查阅资料发现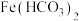 在水中不存在,由此对沉淀的组成作如下假设:
在水中不存在,由此对沉淀的组成作如下假设:
假设a:依据 溶液呈碱性,推测沉淀可能为
溶液呈碱性,推测沉淀可能为_______ ;(填化学式)
假设b:依据 溶液中存在的微粒,推测沉淀还可能为
溶液中存在的微粒,推测沉淀还可能为_______ ;(填化学式)
②验证上述假设的实验过程及现象如下,说明假设_______ 正确。(填“a”或“b”)
ⅰ.将白色沉淀进行充分洗涤后加入稀硫酸,沉淀完全溶解并产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液不变红;
ⅲ.向ⅱ所得溶液中再滴入少量新制氯水,溶液立即变为红色。
③实验小组发现,若将白色沉淀在空气中久置,最终也会变为红褐色。
(4)为探究溶液酸碱性对 还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
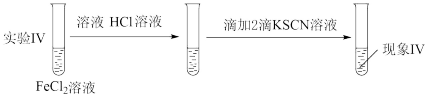
现象Ⅳ:溶液略显红色,3min后溶液颜色没有明显变深
根据实验Ⅰ~Ⅳ,避免 被空气氧化的措施有
被空气氧化的措施有_______ 。(写两条)

现象Ⅱ:生成白色沉淀,3min后沉淀基本变为红褐色
现象Ⅲ:生成白色沉淀,3min后沉淀颜色几乎不变
(1)实验I中的现象为
 具有
具有 操作及现象为
操作及现象为(2)用化学方程式表示“现象Ⅱ”中沉淀由白色变为红褐色的原因
(3)探究“现象Ⅲ”中白色沉淀的组成:
①查阅资料发现
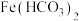 在水中不存在,由此对沉淀的组成作如下假设:
在水中不存在,由此对沉淀的组成作如下假设:假设a:依据
 溶液呈碱性,推测沉淀可能为
溶液呈碱性,推测沉淀可能为假设b:依据
 溶液中存在的微粒,推测沉淀还可能为
溶液中存在的微粒,推测沉淀还可能为②验证上述假设的实验过程及现象如下,说明假设
ⅰ.将白色沉淀进行充分洗涤后加入稀硫酸,沉淀完全溶解并产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液不变红;
ⅲ.向ⅱ所得溶液中再滴入少量新制氯水,溶液立即变为红色。
③实验小组发现,若将白色沉淀在空气中久置,最终也会变为红褐色。
(4)为探究溶液酸碱性对
 还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
现象Ⅳ:溶液略显红色,3min后溶液颜色没有明显变深
根据实验Ⅰ~Ⅳ,避免
 被空气氧化的措施有
被空气氧化的措施有
您最近一年使用:0次
2023-02-16更新
|
263次组卷
|
2卷引用:福建省龙岩市2022-2023学年高一上学期期末教学质量检测化学试题
名校
10 . 氧化亚铜( )主要用于制造船底防污漆、杀虫剂等。一价铜在酸性溶液中可歧化为二价铜离子和铜单质。用黄铜矿(主要成分为
)主要用于制造船底防污漆、杀虫剂等。一价铜在酸性溶液中可歧化为二价铜离子和铜单质。用黄铜矿(主要成分为 )制备氧化亚铜的流程如下图:
)制备氧化亚铜的流程如下图:
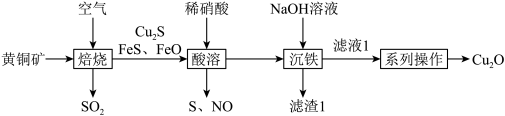
下列说法正确的是
 )主要用于制造船底防污漆、杀虫剂等。一价铜在酸性溶液中可歧化为二价铜离子和铜单质。用黄铜矿(主要成分为
)主要用于制造船底防污漆、杀虫剂等。一价铜在酸性溶液中可歧化为二价铜离子和铜单质。用黄铜矿(主要成分为 )制备氧化亚铜的流程如下图:
)制备氧化亚铜的流程如下图:
下列说法正确的是
A.“焙烧”反应产生的气体会污染环境,可通入 溶液除去 溶液除去 |
B.酸溶时,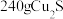 与足量稀硝酸充分反应,产生NO体积为44.8L 与足量稀硝酸充分反应,产生NO体积为44.8L |
C.可用KSCN溶液检验滤液Ⅰ中是否含有 |
D. 和稀硫酸反应时,稀硫酸是氧化剂 和稀硫酸反应时,稀硫酸是氧化剂 |
您最近一年使用:0次
2023-02-16更新
|
415次组卷
|
2卷引用:福建省龙岩市2022-2023学年高一上学期期末教学质量检测化学试题



