名校
解题方法
1 . 绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:___________ ;
(2)过程②对应的化学方程式是:___________ 。
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2 +I2=
+I2= +2I-)
+2I-)
iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是_________ ;
(4)醋酸铜产品中铜元素的质量分数是_______ 。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:
(2)过程②对应的化学方程式是:
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2
 +I2=
+I2= +2I-)
+2I-)iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是
(4)醋酸铜产品中铜元素的质量分数是
您最近一年使用:0次
解题方法
2 . 下列说法中,不正确的是
| A.玻璃钢是复合材料 | B.铜在空气中会生成铜锈 |
| C.金属钠着火时可使用煤油灭火 | D.铝是活泼金属,但在空气中耐腐蚀 |
您最近一年使用:0次
解题方法
3 . 铜是生产和生活中用量较多的金属。
(1)下列有关铜元素的说法中,不正确的是__________ (填字母)
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物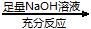 测定剩余固体的质量
测定剩余固体的质量
①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:___________ ,该方案中稀硝酸表现出来的性质是___________ (填字母)。
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是________________ 。请写出方案Ⅱ中发生反应的化学方程式:____________ ,该反应产生气体在标准状况下的体积为________ (铜铝混合物质量是m1g,反应后剩余固体的质量m2g,用含m1、m2的代数式表示)。
(1)下列有关铜元素的说法中,不正确的是
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物
 测定生成气体的体积
测定生成气体的体积方案Ⅱ:铜铝混合物
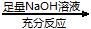 测定剩余固体的质量
测定剩余固体的质量①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是
您最近一年使用:0次
2020-01-02更新
|
126次组卷
|
2卷引用:河南省南阳市六校2019-2020学年高一下学期第一次联考试题 化学
名校
4 . 向Cu、Cu2O和CuO组成的混合物中,加入1L0.6 mol/L HNO3溶液恰好使其完全溶解,同时收集到2240 mL NO气体(标准状况)。下列说法中不正确的是
(已知:Cu2O+2H+=Cu+Cu2++H2O)
(已知:Cu2O+2H+=Cu+Cu2++H2O)
| A.上述体现酸性的硝酸与体现氧化性的硝酸其物质的量之比为5:1 |
| B.若混合物中含0.1molCu,使该混合物与稀硫酸充分反应,消耗硫酸的物质的量为0.1mol |
| C.Cu2O跟稀硝酸反应的离子方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O |
| D.若将上述混合物用足量的H2加热还原,所得到固体的质量为32g |
您最近一年使用:0次
2019-10-03更新
|
244次组卷
|
4卷引用:河南省南阳市第一中学2018届高三上学期第三次考试化学试题
名校
5 . 下列化学方程式中,不能正确表达反应颜色变化的原因的是
| A.铜久置空气中表面出现绿色固体:2Cu+O2+CO2+H2O═Cu2(OH)2CO3 |
B.某种火箭发射阶段有少量N2O4,逸出,产生红色气体:N2O4 2NO2 2NO2 |
C.FeSO4·7H2O在空气中久置变黄:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O Fe2O3+SO2↑+SO3↑+14H2O |
| D.SO2通入KMnO4溶液中,溶液紫色逐渐褪去:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4十2H2SO4 |
您最近一年使用:0次
2019-09-09更新
|
400次组卷
|
5卷引用:河南省南阳市第一中学2020届高三上学期第二次开学考试化学试题
河南省南阳市第一中学2020届高三上学期第二次开学考试化学试题山东省临沂市第一中学2020届高三10月月考化学试题2019年湖北省黄冈市高三11月新高考备考监测联考化学试题山东省新高考备考监测2020届高三10月联考化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题
6 . 废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:
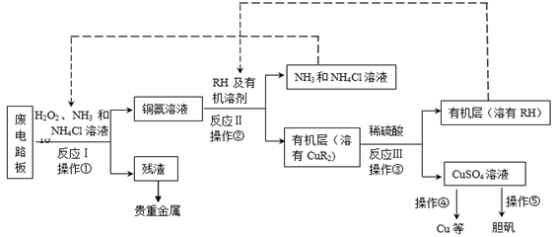
回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是_____ 。写出操作①的名称:_________ 。
(2)反应II是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:_______ 。操作②用到的主要仪器名称为_____ ,其目的是(填序号)_________ 。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和______ 。若操作③使用下图装置,图中存在的错误是_____ 。
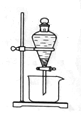
(4)操作④以石墨作电极电解CuSO4溶液。阴极析出铜,阳极产物是_______ 。操作⑤由硫酸铜溶液制胆矾的主要步骤是____________ 。
(5)流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是______ 。循环使用的NH4Cl在反应Ⅰ中的主要作用是________ 。

回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是
(2)反应II是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和

(4)操作④以石墨作电极电解CuSO4溶液。阴极析出铜,阳极产物是
(5)流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是
您最近一年使用:0次
2019-01-30更新
|
2999次组卷
|
6卷引用:河南省南阳市第一中学校2021届高三上期第五次考试化学试题
7 . 狐刚子在“炼石胆取精华法”中作如下叙述:“以士擊(即砖坯)垒作两个方头炉,一炉中著铜盘,使定,即密泥之,一炉中以炭烧石胆(CuSO4·5H2O)使作烟,以物扇之,其精华尽入铜盘。炉中却火待冷……”。狐刚子所取“精华”为
| A.H2O | B.SO2 | C.稀硫酸 | D.CuSO4溶液 |
您最近一年使用:0次
2017-12-13更新
|
237次组卷
|
2卷引用:河南省南阳市2018届高三第三次联考化学试题
名校
8 . 溴化亚铜可用作工业催化剂,是一种白色粉末,微溶于冷水,不溶于乙醇等有机溶剂,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:

步骤1.在如上图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去水中的________________ (写化学式)。
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为__________________ ;
②控制反应在60℃进行,实验中可采取的措施是____________________ ;
③说明反应已完成的现象是_____________________ 。
(3)步骤2过滤需要避光的原因是_____________________ 。
(4)步骤3中洗涤剂需“溶有SO2”的原因是____________________ 。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。
请补充实验步骤[须用到SO2(贮存在钢瓶中)、20%NaOH溶液]:
①_________________ 。
②___________________ 。
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④过滤,用乙醇洗涤2~3次。⑤放真空干燥箱中干燥。

步骤1.在如上图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去水中的
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为
②控制反应在60℃进行,实验中可采取的措施是
③说明反应已完成的现象是
(3)步骤2过滤需要避光的原因是
(4)步骤3中洗涤剂需“溶有SO2”的原因是
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。
请补充实验步骤[须用到SO2(贮存在钢瓶中)、20%NaOH溶液]:
①
②
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④过滤,用乙醇洗涤2~3次。⑤放真空干燥箱中干燥。
您最近一年使用:0次
2017-11-27更新
|
561次组卷
|
3卷引用:河南省南阳市第一中学2018届高三上学期第五次月考化学试题
名校
9 . CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配制 CuSO4 溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了,原因是______________________ ,最后,他向烧杯中加入了一定量的_______ 溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的 CuSO4溶液,进行以下实验探究。
①图一是根据反应 Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池。电解质溶液乙是_______ 溶液;Cu极的电极反应式是_________________ 。
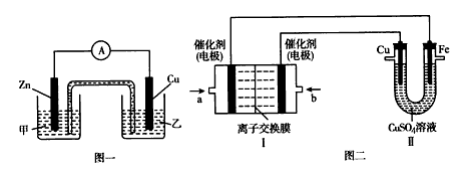
②图二中,I 是甲烷燃料电池(电解质溶液为 NaOH 溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是__________ (填“CH4”或“O2”), a 处电极上发生的电极反应式是____ ;铁为电解池的____ 极,当铜电极的质量减轻 3.2 g,则消耗的 CH4在标准状况下的体积为____ L。
(3)反应一段时间后,生成的 Na2CO3 溶液(溶质仅为 Na2CO3)中存在的关系正确的是____ 。
A. c(Na+)=c(HCO3-)=c(OH-)=c(H+) B. c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C. c(Na+)>c(CO32-)>c(H+)>c(OH-) D. c(Na+)>c(CO32-) >c(OH-)>c(HCO3-)
(1)某同学配制 CuSO4 溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了,原因是
(2)该同学利用制得的 CuSO4溶液,进行以下实验探究。
①图一是根据反应 Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池。电解质溶液乙是

②图二中,I 是甲烷燃料电池(电解质溶液为 NaOH 溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是
(3)反应一段时间后,生成的 Na2CO3 溶液(溶质仅为 Na2CO3)中存在的关系正确的是
A. c(Na+)=c(HCO3-)=c(OH-)=c(H+) B. c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C. c(Na+)>c(CO32-)>c(H+)>c(OH-) D. c(Na+)>c(CO32-) >c(OH-)>c(HCO3-)
您最近一年使用:0次
2017-02-26更新
|
557次组卷
|
2卷引用:2016-2017学年河南省南阳市第一中学高二下学期开学考试化学试卷
10 . 现有Si和Al2O3的固体混合物样品,加入NaOH溶液使混合物完全溶解,所得溶液中c(Na+) : c([Al(OH)4]-) : c(OH—) = 6:2:1,则原固体混合物中硅元素与氧元素的质量比为
| A.7:8 | B.3:1 | C.3:2 | D.7:16 |
您最近一年使用:0次



