名校
解题方法
1 . 雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO 2CO2(g)+N2(g) △H<O
2CO2(g)+N2(g) △H<O
①反应的速率时间图像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是(填对应字母)__________
B.b1<b2
C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号)__________
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g) N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:__________ .
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
①该反应是__________ 反应(填“吸热”或“放热”).
②T℃时,向1L密闭容器中投入l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O CO+3H2的平衡常数K=
CO+3H2的平衡常数K=__________ ;
(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。__________
②电解后溶液的pH=__________ (忽略氯气与氢氧化钠溶液反应)
③阳极产生气体的体积在标准状况下是__________ L。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO
 2CO2(g)+N2(g) △H<O
2CO2(g)+N2(g) △H<O①反应的速率时间图像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是(填对应字母)

B.b1<b2
C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号)
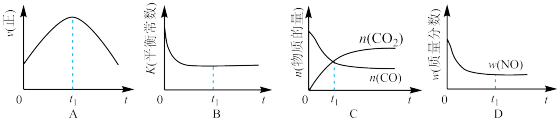
已知:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol2NO2(g)
 N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
②T℃时,向1L密闭容器中投入l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O
 CO+3H2的平衡常数K=
CO+3H2的平衡常数K=(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。
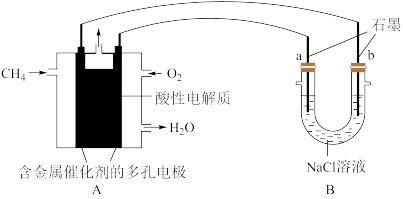
②电解后溶液的pH=
③阳极产生气体的体积在标准状况下是
您最近一年使用:0次
2017-02-17更新
|
377次组卷
|
7卷引用:2016届山西省祁县中学高三5月月考理综化学试卷
真题
名校
2 . 催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1 I
CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1 I
CO2(g)+H2(g) CO(g)+H2O(g) △H2 II
CO(g)+H2O(g) △H2 II
某实验室控制CO2和H2初始投料比为1︰2.2,在相同压强下,经过相同反应时间测得如下实验数据:
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1。
②H2O(l)=H2O(g) △H3=+44.0kJ•mol-1
请回答(不考虑温度对△H的影响):
(1)反应I的平衡常数表达式K=______ ;反应II的△H2=______ kJ•mol-1.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有__________ 。
A.使用催化剂Cat.1 B.使用催化剂Cat.2
C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大 CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___________________________ 。
(4)在如图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程-能量”示意图_________ 。

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在______ 极,该电极反应式是_________ 。
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1 I
CH3OH(g)+H2O(g) △H1=-53.7kJ•mol-1 ICO2(g)+H2(g)
 CO(g)+H2O(g) △H2 II
CO(g)+H2O(g) △H2 II某实验室控制CO2和H2初始投料比为1︰2.2,在相同压强下,经过相同反应时间测得如下实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
已知:①CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1。
②H2O(l)=H2O(g) △H3=+44.0kJ•mol-1
请回答(不考虑温度对△H的影响):
(1)反应I的平衡常数表达式K=
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有
A.使用催化剂Cat.1 B.使用催化剂Cat.2
C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大 CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是
(4)在如图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程-能量”示意图

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在
您最近一年使用:0次
2016-12-09更新
|
1469次组卷
|
6卷引用:2017届山西省重点中学协作体高三暑假第一次联考化学试卷
2017届山西省重点中学协作体高三暑假第一次联考化学试卷2016年全国普通高等学校招生统一考试化学(浙江卷精编版)广东省揭阳市第一中学2018届高三上学期第二次阶段考试化学试题陕西省西安市长安区第一中学2018届高三上学期第五次质量检测化学试题2016年全国普通高等学校招生统一考试化学(浙江卷参考版)(已下线)专题20.化学反应原理综合应用-十年(2012-2021)高考化学真题分项汇编(浙江专用)
名校
3 . 通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是
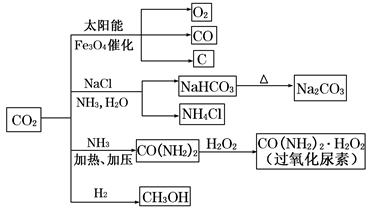

| A.CO2经催化分解为C、CO、O2的反应为放热反应 |
| B.除去Na2CO3固体中少量NaHCO3可用热分解的方法 |
| C.过氧化尿素和SO2都能使品红溶液褪色,其原理相同 |
| D.由CO2和H2合成甲醇,原子利用率达100% |
您最近一年使用:0次
2016-12-09更新
|
740次组卷
|
4卷引用:山西省运城市河津市河津中学2019届高三上学期9月月考化学试题
山西省运城市河津市河津中学2019届高三上学期9月月考化学试题2016届内蒙古巴彦淖尔市第一中学高三上期中考试理化学试卷湘赣皖十五校(长郡中学、南昌二中等)2020届高三下学期第一次联考模拟化学试题(已下线)第11讲 碳、硅及无机非金属材料(精讲)-2022年一轮复习讲练测
14-15高三上·河北石家庄·阶段练习
名校
4 . 下列图示与对应的叙述相符的是
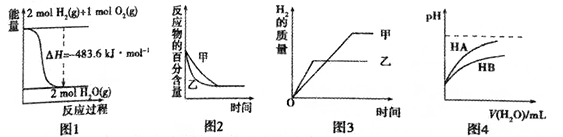

| A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ·mol-1 |
B.图2表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C.若图3表示等质量的钾、钠分别与足量水反应,则甲代表钠 |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH |
您最近一年使用:0次
2016-12-09更新
|
1332次组卷
|
13卷引用:山西省三区八校2017届高三第二次模拟考试理科综合化学试题
山西省三区八校2017届高三第二次模拟考试理科综合化学试题山西省孝义市2017届高三下学期考前热身训练理综化学试题(已下线)2015届河北省正定中学高三上学期第三次月考化学试卷【全国百强校】江苏省启东市启东中学2019届高三上学期第一次月考化学试题陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题河北省衡水市衡水中学2019届高三上学期期中考试化学试题河南省南阳市2018届高三上学期期末考试理综化学试题【市级联考】江西省宜春市2019届高三上学期期末统考理科综合化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题福建省漳州市龙海市第二中学2020届高三上学期第二次月考化学试题甘肃省天水市一中2020届高三上学期第四次考试化学试题辽宁省辽河油田第二高级中学2020届高三期末考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解平衡的影响因素及探究
10-11高二·山西·阶段练习
解题方法
5 . 工业上以黄铁矿为原料生产硫酸。
(1)写出燃烧黄铁矿的化学方程式______________________________ 。
(2)接触室中发生反应的化学方程式是_______________________________ 。
(3)判断下列说法正确的是(选填序号字母)________________ 。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)吸收塔中用浓硫酸吸收三氧化硫而不用水的原因是是_____________ 。
(5)吸收塔排出的尾气可以用两种方法处理:
方法①:先用氨水吸收,再用浓硫酸处理。用浓硫酸处理的主要目的是_______ ;
方法②:先用含一定水的亚硫酸钠吸收后再加热处理,也可达到与方法①相同的目的。为了实现节能减排,其所需能量可以由________ 提供。与方法①相比,方法②的优点是_________ 。
(6)SO2 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2 吸收Br2的离子方程式是__________________________ 。
(1)写出燃烧黄铁矿的化学方程式
(2)接触室中发生反应的化学方程式是
(3)判断下列说法正确的是(选填序号字母)
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)吸收塔中用浓硫酸吸收三氧化硫而不用水的原因是是
(5)吸收塔排出的尾气可以用两种方法处理:
方法①:先用氨水吸收,再用浓硫酸处理。用浓硫酸处理的主要目的是
方法②:先用含一定水的亚硫酸钠吸收后再加热处理,也可达到与方法①相同的目的。为了实现节能减排,其所需能量可以由
(6)SO2 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2 吸收Br2的离子方程式是
您最近一年使用:0次
9-10高三下·山西太原·阶段练习
6 . 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价):

| A.放出H2的质量是C>B>A |
| B.金属活动性顺序是A>B>C |
| C.反应速率最大的是A |
| D.相对原子质量是C>B>A |
您最近一年使用:0次
7 . 硫酸是一种重要的化工产品,2SO2+O2 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零 |
| C.如果反应前充入由18O原子组成的O2,反应达到平衡状态时,18O在所有物质中都存在 |
| D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
您最近一年使用:0次



