名校
1 . 下列说法或表示方法中正确的是
| A.同温同压下,H2(g)+Cl2(g) = 2HCl(g)在光照和点燃条件下的ΔH相同 |
| B.使用催化剂能降低反应的活化能,所以也能改变反应的ΔH。 |
| C.甲烷的燃烧热为-890.3KJ/mol,则其热化学方程式为CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) ΔH= - 890.3kJ/mol, |
| D.稀的强酸和稀的强碱溶液反应的热化学方程式均为:H+ +OH- = H2O ΔH= -57.3kJ·mol-1 |
您最近一年使用:0次
2021-10-13更新
|
304次组卷
|
6卷引用:福建省莆田九中2017-2018学年高二上学期第二次月考(12月)化学试题
2 . 通过以下反应可获得新型能源二甲醚( )。下列说法不正确的是
)。下列说法不正确的是
①
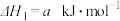
②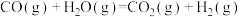
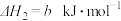
③
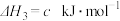
④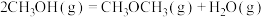
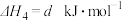
 )。下列说法不正确的是
)。下列说法不正确的是①

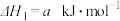
②
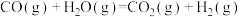
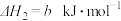
③

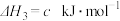
④
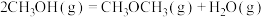
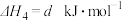
| A.反应①②为反应③提供原料气 |
B.反应③也是 资源化利用的方法之一 资源化利用的方法之一 |
C.反应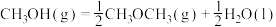 的 的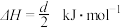 |
D.反应 的 的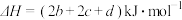 |
您最近一年使用:0次
2021-08-07更新
|
4572次组卷
|
90卷引用:福建省莆田九中2019-2020学年高二上学期期中考试化学试题
福建省莆田九中2019-2020学年高二上学期期中考试化学试题山东省济宁市2016-2017学年高二下学期期末考试化学试题湖南省长郡中学2017-2018学年高二上学期第一次模块检测化学试题1安徽师范大学附属中学2017-2018学年高二上学期10月月考化学试题河南省郑州市第一中学2017-2018学年高二上学期期中考试化学试题四川省遂宁市射洪县2017-2018学年高二上学期期末统考实验小班加试化学试题辽宁省实验中学2017-2018学年高二上学期期中考试化学试题河南省周口市中英文学校2018-2019学年高二上学期第一次月考化学试题(已下线)2018年10月21日 《每日一题》人教选修4-每周一测【全国百强校】四川省彭州中学2018-2019学年高二上学期10月月考化学试题【全国百强校】吉林省实验中学2018-2019学年高二上学期期中考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二(实验班)上学期期中考试化学试题【全国百强校】湖南省衡阳市第八中学2018-2019学年高二上学期六科联赛试题(12月)化学试题安徽省新城高升学校2018-2019学年高二上学期期中考试化学试题广东省-北京师范大学东莞石竹附属学校2019-2020学年高二10月月考化学试题江西省南昌市八一中学、洪都中学、十七中三校2019-2020学年高二10月联考化学试题河南省南阳市南阳一中2019-2020学年高二上期第三次月考化学试题江苏省苏北县2019-2020学年高二上学期学情调研化学(选择考)试题北京市2019—2020学年高二上学期期末考试模拟试题(选修4人教版 )云南省昆明市寻甸县民族中学2019-2020学年高二下学期第一次月考化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1章 综合检测高中必刷题高二选择性必修1第一章 化学反应的热效应 第一章素养检测(已下线)1.3.1+盖斯定律-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)1.3.2+反应热的计算-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)江苏省南通市海安县2020-2021学年高二上学期第一次月考化学试题浙江省富阳中学2020-2021学年高二上学期第一次月考化学试题河南省周口市中英文学校2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 过高考 3年真题强化闯关陕西省西安市长安区第一中学2020-2021学年高二上学期第一次教学质量检测化学试题江苏省泰州中学2020-2021学年高二上学期第一次月度质量检测化学试题湖南省邵阳市邵东创新实验学校2020-2021学年高二上学期期末考试化学(选考)试题选择性必修1 专题1 素养检测江苏省华东师范大学盐城实验中学2021-2022学年高二上学期第一次月考化学试题 江苏省扬州中学2021-2022学年高二上学期10月阶段检测化学试题安徽省蚌埠第三中学2021-2022学年高二上学期10月教学质量检测化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题辽宁省沈阳市东北育才双语学校2021-2022学年高二上学期期中考试化学试题(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期开学考试化学试题 江西省丰城市第九中学2021-2022学年高二上学期第二次月考(日新班)化学试题湖南省临湘市第五中学2021-2022学年高二上学期第三次月考化学试题广东省广州市第八十九中学2022-2023学年高二上学期期末考试化学试题河南省南阳市2023-2024学年高二上学期10月月考化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期第一次半月考化学试题江苏省苏州市工业园区三校20232024学年高二上学期10月联考化学试题四川省内江市第六中学20223-2024学年高二上学期第一次月考化学试题 广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷陕西省西安市蓝田县乡镇学校联考2023-2024学年高二上学期1月期末化学试题河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试化学(江苏卷精编版)江苏省海安高级中学2018届高三1月月考化学试题(已下线)二轮复习测试专项 专题07 化学反应与能量变化江苏省泰州中学2018届高三3月月度检测(二模模拟)化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题13 化学反应与能量类选择题解题方法和策略(已下线)《考前20天终极攻略》-5月24日 盖斯定律及反应热的有关计算(已下线)解密08 化学反应与热能(教师版)——备战2018年高考化学之高频考点解密【全国百强校】陕西省宝鸡中学2019届高三上学期11月模拟考试(二)化学试题福建省泉州市泉港区第一中学2019届高三上学期第二次月考化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点(已下线)2019年高考总复习巅峰冲刺-专题05 化学反应中的能量变化应试策略浙江省嘉兴市第一中学2020届高三上学期期中考试化学试题2019年秋高三化学复习强化练习—— 盖斯定律及其应用天津市海河中学2020届高三第二学期化学测试(二)试卷(已下线)专题九 化学能与热能(提分特训)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训北京市顺义牛栏山第一中学2020届高三下学期模拟考试化学试题河北省衡水中学2020届高三四月份质量监测理综化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题北京市顺义牛栏山第一中学2020届高三3月高考适应性测试化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分(已下线)【浙江新东方】42.浙江省杭州学军中学2021届高三上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高三上】【期中】【HD-LP423】【化学】(已下线)【浙江新东方】120(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)山西省实验中学2019届高三上学期第四次月考化学试题高中化学苏教2019版必修第二册-专题6 第二单元综合拔高练(已下线)【浙江新东方】高中化学20210513-015【2021】【高三下】(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题7 盖斯定律专练(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)陕西省延安市第一中学2021-2022学年高一下学期期中考试化学试题江苏省连云港市厉庄高级中学2022-2023学年高三上学期第一次质量检测化学试题(已下线)热点情景汇编-专题六 化学反应中的热能福建省泉州第一中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
3 . 二硫化钼(MoS2,其中Mo化合价为+4)是辉钼矿的主要成分,可用于制取钼的化合物、润滑添加剂、氢化反应和异构化反应的催化剂等,回答下列问题:
(1)已知:MoS2(s)=Mo(s)+S2(g)∆H1;
S2(g)+2O2(g)=2SO2(g)∆H2;
2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g)∆H3;
反应2Mo(s)+3O2(g)=2MoO3(s)的∆H=_______ (用含∆H1、∆H2、∆H3的代数式表示)。
(2)利用电解法可浸取辉钼矿得到Na2MoO4和Na2SO4溶液装置如图所示。

①阴极的电极反应式为_______ 。
②MoO 在电极
在电极_______ (填A或B)附近生成。
(3)用辉钼矿冶炼Mo的反应为:MoS2(s)+4H2(g)+2Na2CO3(s) Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)∆H
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)∆H
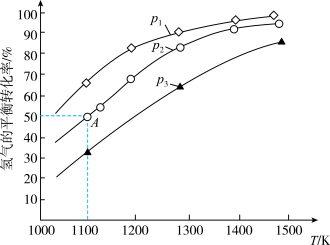
①该反应的∆H_______ 0(填“>”或“<”);p1、p2、p3按从小到大的顺序为_______ 。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若充入氦气,平衡_______ (填“向正反应方向”“向逆反应方向”或“不移动”)。
③在2L的恒温恒容密闭容器中加入0.1mol MoS2、0.2mol Na2CO3、0.4mol H2,在1100K时发生反应,达到平衡时恰好处于图中A点,则此温度下该反应的平衡常数为_______ 。
(1)已知:MoS2(s)=Mo(s)+S2(g)∆H1;
S2(g)+2O2(g)=2SO2(g)∆H2;
2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g)∆H3;
反应2Mo(s)+3O2(g)=2MoO3(s)的∆H=
(2)利用电解法可浸取辉钼矿得到Na2MoO4和Na2SO4溶液装置如图所示。

①阴极的电极反应式为
②MoO
 在电极
在电极(3)用辉钼矿冶炼Mo的反应为:MoS2(s)+4H2(g)+2Na2CO3(s)
 Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)∆H
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)∆H
①该反应的∆H
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若充入氦气,平衡
③在2L的恒温恒容密闭容器中加入0.1mol MoS2、0.2mol Na2CO3、0.4mol H2,在1100K时发生反应,达到平衡时恰好处于图中A点,则此温度下该反应的平衡常数为
您最近一年使用:0次
2021-06-15更新
|
231次组卷
|
2卷引用:福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题
4 . 下列科学家与其贡献匹配错误的是
| A.侯德榜——联合制碱 | B.盖斯——平衡移动原理 |
| C.徐光宪——稀土元素分离及应用 | D.门捷列夫——元素周期表 |
您最近一年使用:0次
2021-06-12更新
|
246次组卷
|
3卷引用:福建省莆田市锦江中学2023-2024学年高二上学期期末考试化学试题
名校
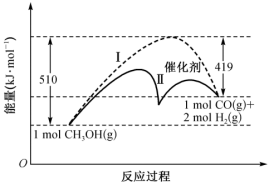
5 . 燃料气(CO、H2)是有机化工中的常见原料,工业上制取方法之一为高温下甲醇分解,反应原理为CH3OH(g) CO(g)+2H2(g) ∆H,能量变化情况如图。下列叙述正确的是
CO(g)+2H2(g) ∆H,能量变化情况如图。下列叙述正确的是
 CO(g)+2H2(g) ∆H,能量变化情况如图。下列叙述正确的是
CO(g)+2H2(g) ∆H,能量变化情况如图。下列叙述正确的是
| A.∆H为-91 kJ·mol-1 | B.I:正反应的活化能为419 kJ·mol-1 |
| C.II:催化剂增加了活化分子数 | D.其他条件相同时I比II先达到平衡 |
您最近一年使用:0次
2021-03-20更新
|
921次组卷
|
9卷引用:福建省莆田第一中学2022-2023学年高二上学期期末考试化学试题
福建省莆田第一中学2022-2023学年高二上学期期末考试化学试题安徽省江淮名校2020-2021学年高二下学期开学联考化学试题广东省梅州市2020-2021学年高二下学期期末考试化学试题广东省茂名市电白区2021-2022学年高二上学期期末考试(选择性)化学试题江西省上饶市铅山县第一中学2021-2022学年高二下学期开学考试化学试题 湖南省株洲市第一中学2022-2023学年高二上学期期末考试化学试题四川省仁寿第一中学校南校区2022—2023学年高二下学期3月月考化学试题湖南省娄底市新化县2023-2024学年高二上学期期末考试化学试题天津市塘沽一中2022届高三上学期毕业班开学调研考试化学试题
6 . 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol液态水消耗的能量是____________ kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________ ;
(3)在以甲醇为燃料、电解质为稀硫酸的燃料电池中,甲醇发生________ 反应(填“氧化”或“还原”),正极反应式为_________________________ ;
(4)二甲醚(CH3OCH3)是无色气体,可作为一种新型能源,由合成气(组成为H2、CO、和少量CO2)直接制备二甲醚,其中主要过程包括以下反应:
甲醇合成反应:①CO(g)+ 2H2(g)=CH3OH(g) ΔH1=-90.1kJ·mol‒1
水煤气变换反应:②CO(g) + H2O (g)=CO2(g)+H2(g) ΔH2=-41.1kJ·mol‒1
二甲醚合成反应:③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5 kJ·mol‒1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为___________ ,二甲醚直接燃料电池具有启动快,效率高等优点,其能量密度高于甲醇直接燃料电池,若电解质为碱性,二甲醚燃料电池的负极反应式为______________________________ 。
(1)用太阳能分解10mol液态水消耗的能量是
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)在以甲醇为燃料、电解质为稀硫酸的燃料电池中,甲醇发生
(4)二甲醚(CH3OCH3)是无色气体,可作为一种新型能源,由合成气(组成为H2、CO、和少量CO2)直接制备二甲醚,其中主要过程包括以下反应:
甲醇合成反应:①CO(g)+ 2H2(g)=CH3OH(g) ΔH1=-90.1kJ·mol‒1
水煤气变换反应:②CO(g) + H2O (g)=CO2(g)+H2(g) ΔH2=-41.1kJ·mol‒1
二甲醚合成反应:③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5 kJ·mol‒1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为
您最近一年使用:0次
解题方法
7 . (1)已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为
C(金刚石·s)+O2(g)=CO2(g)ΔH1=-395.41kJ/mol-1,
C(石墨·s)+O2(g)=CO2(g)ΔH2=-393.51kJ/mol-1,则金刚石转化为石墨时的热化学方程式:____ ,由此看来更稳定的碳的同素异形体为_____ 。
(2)某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。
已知:N2(g)+2O2(g)=2NO2(g)△H=+67.2kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534kJ/mol
假如都在相同状态下,请写出发射火箭反应的热化学方程式:_______
C(金刚石·s)+O2(g)=CO2(g)ΔH1=-395.41kJ/mol-1,
C(石墨·s)+O2(g)=CO2(g)ΔH2=-393.51kJ/mol-1,则金刚石转化为石墨时的热化学方程式:
(2)某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。
已知:N2(g)+2O2(g)=2NO2(g)△H=+67.2kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534kJ/mol
假如都在相同状态下,请写出发射火箭反应的热化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因_______ 。
(2)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s) N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
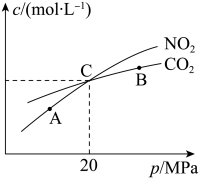
①A、B两点的浓度平衡常数关系:Kc(A)_______ Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是_______ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=_______ (写出计算结果,Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)亚硝酸的电离平衡常数Ka=5.1×10-4(298K)。它的性质和硝酸很类似。已知298K 时,H2CO3的Ka1=4.2×10-7;Ka2=5.61×10-11.向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO 、HCO
、HCO 和NO
和NO 的离子浓度由大到小是
的离子浓度由大到小是_______ 。
(4)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
① CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1
②CaSO4(s)+ 4CO(g) CaS(s)+ 4CO2(g) △H= -189.2kJ•mol-1
CaS(s)+ 4CO2(g) △H= -189.2kJ•mol-1
反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) △H=
CaS(s)+3CO2(g) △H=_______ kJ•mol-1;
(5)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=_______ mol·L-1;
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=_______ 时,Fe2+开始沉淀。【已知:KSP(FeS)=1.4×10-19】
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因
(2)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s)
 N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp=
(3)亚硝酸的电离平衡常数Ka=5.1×10-4(298K)。它的性质和硝酸很类似。已知298K 时,H2CO3的Ka1=4.2×10-7;Ka2=5.61×10-11.向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO
 、HCO
、HCO 和NO
和NO 的离子浓度由大到小是
的离子浓度由大到小是(4)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
① CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1②CaSO4(s)+ 4CO(g)
 CaS(s)+ 4CO2(g) △H= -189.2kJ•mol-1
CaS(s)+ 4CO2(g) △H= -189.2kJ•mol-1反应CaO(s)+3CO(g)+SO2(g)
 CaS(s)+3CO2(g) △H=
CaS(s)+3CO2(g) △H=(5)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=
您最近一年使用:0次
9 . 碘与氢气反应的热化学方程式是
①I2(g)+H2(g) 2HI(g) ΔH=-9.48kJ·mol-1
2HI(g) ΔH=-9.48kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH=26.48kJ·mol-1
2HI(g) ΔH=26.48kJ·mol-1
下列说法正确的是
①I2(g)+H2(g)
 2HI(g) ΔH=-9.48kJ·mol-1
2HI(g) ΔH=-9.48kJ·mol-1②I2(s)+H2(g)
 2HI(g) ΔH=26.48kJ·mol-1
2HI(g) ΔH=26.48kJ·mol-1下列说法正确的是
| A.①的产物比②的产物稳定 |
| B.1molI2(s)转化为1molI2(g)需要放出热量 |
| C.②的反应物总能量比①的反应物总能量低 |
| D.1molI2(g)中通入1molH2(g),发生反应时放热9.48kJ |
您最近一年使用:0次
解题方法
10 . 写出下列反应的热化学方程式:
(1)N2(g)和H2(g)反应生成1mol NH3(g),放出46.1kJ热量_____ 。
(2)46g C2H5OH(l)完全燃烧生成CO2(g)和H2O(l)放出1366.8 kJ热量_____ 。
(3)已知断裂1molH2(g)中的H-H键需要吸收436kJ的能量,断裂1molO2(g)中的共价键需要吸收498kJ的能量,生成H2O(g)中1molH-O键能放出463kJ的能量,试着写出O2(g)与H2(g)反应生成H2O(g)的热化学方程式________ 。.
(4)到目前为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);ΔH=-25kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g);ΔH=-47kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g);ΔH=+19kJ/mol
请写出CO还原FeO的热化学方程式______ 。
(1)N2(g)和H2(g)反应生成1mol NH3(g),放出46.1kJ热量
(2)46g C2H5OH(l)完全燃烧生成CO2(g)和H2O(l)放出1366.8 kJ热量
(3)已知断裂1molH2(g)中的H-H键需要吸收436kJ的能量,断裂1molO2(g)中的共价键需要吸收498kJ的能量,生成H2O(g)中1molH-O键能放出463kJ的能量,试着写出O2(g)与H2(g)反应生成H2O(g)的热化学方程式
(4)到目前为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);ΔH=-25kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g);ΔH=-47kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g);ΔH=+19kJ/mol
请写出CO还原FeO的热化学方程式
您最近一年使用:0次



