1 . 回答下列问题
(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。
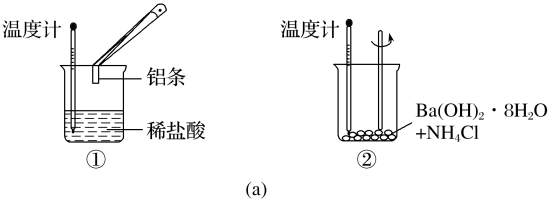
实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是___________ 热反应,Ba(OH)2·8H2O与NH4Cl的反应是___________ 热反应。
(2)我国发射宇宙飞船的 “神舟”系列火箭用偏二甲肼(C2H8N2)作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体,其反应的化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O。则该反应是___________ (填“放热”或“吸热”)反应,反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物的总能量,断开化学键吸收的总能量___________ (填“大于”、“小于”或“等于”)形成化学键放出的总能量。
(3)矿物能源是现代人类社会赖以生存的重要物质基础,目前,全球仍主要处于化石能源时期。下列不属于化石能源的是___________。
(4)沼气是有机废弃物(树叶、秸秆、草类及垃圾、粪便等)在隔绝空气的条件下发酵分解而成的气体,主要成分是甲烷。农村沼气池中发酵后的池底剩余物是很好的沤肥。下面有关叙述中,错误的是___________。
(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。

实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是
(2)我国发射宇宙飞船的 “神舟”系列火箭用偏二甲肼(C2H8N2)作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体,其反应的化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O。则该反应是
(3)矿物能源是现代人类社会赖以生存的重要物质基础,目前,全球仍主要处于化石能源时期。下列不属于化石能源的是___________。
| A.石油 | B.煤 | C.天然气 | D.生物质能 |
| A.沼气是一种清洁的能源 |
| B.使用沼气作能源可以保护森林 |
| C.使用沼气给农民的生活带来了不便 |
| D.使用沼气是对化学能的充分利用 |
您最近一年使用:0次
解题方法
2 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是___________ (填字母)。
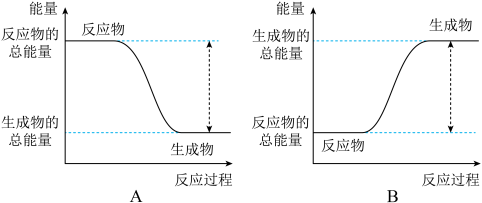
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量___________ kJ。
(3)将Z棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。
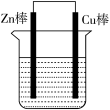
①若电解质溶液为稀硫酸,则Zn棒为原电池的___________ (填“正”或“负”)极,可观察到Cu棒上有气泡生成,写出Cu棒上的电极反应式___________ 。若反应过程中Zn棒减少的质量为3.25g,则生成的氢气在标准状况下的体积为___________ L。
②若电解质为硫酸铜溶液,则Cu棒上发生___________ (填“氧化”或“还原”)反应,Zn棒上发生的电极反应式为___________ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(3)将Z棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。

①若电解质溶液为稀硫酸,则Zn棒为原电池的
②若电解质为硫酸铜溶液,则Cu棒上发生
您最近一年使用:0次
2023-03-12更新
|
756次组卷
|
2卷引用:陕西省汉中市2020-2021学年高一下学期期中联考化学试卷
名校
3 . 古代诗词中蕴含着许多科学知识,下列叙述不正确的是
| A.“冰,水为之,而寒于水”说明等质量的水和冰相比,冰的能量更低 |
| B.“纷纷灿烂如星陨,赫赫喧虺似火攻”所描述的灿烂烟花是某些金属的焰色试验 |
| C.“千锤万凿出深山,烈火焚烧若等闲”描述的石灰石煅烧是吸热反应 |
| D.“煮豆燃豆萁,豆在釜中泣”,这里的变化只有化学能转化为热能 |
您最近一年使用:0次
2023-03-12更新
|
1396次组卷
|
12卷引用:陕西省汉中市2020-2021学年高一下学期期中联考化学试卷
陕西省汉中市2020-2021学年高一下学期期中联考化学试卷山东省新泰市第一中学2022-2023学年高一下学期第一次阶段性考试检测化学试题山西省太原市第四十八中学校2022-2023学年高一下学期3月月考化学试题山东省青岛第十九中学2022-2023学年高一4月月考化学试题浙江省台州市洪家中学2022-2023学年高一下学期期中考试化学试题甘肃省天水市第一中学2022-2023学年高一下学期5月期中考试化学试题吉林省长春汽车经济技术开发区第三中学2022-2023学年高一下学期期中考试化学试题四川省广安市岳池县第一中学2022-2023学年高一下学期第二次月考化学试题内蒙古第一机械制造(集团)有限公司第一中学2023-2024学年高二上学期9月月考化学试题山东省烟台市莱州市第一中学2023-2024学年高一下学期3月月考化学试题山西省太原市育英中学校2023-2024学年高一下学期3月月考化学试题阶段重点练(三)
名校
4 . 甲醛(HCHO)与 在羟基磷灰石(HAP)表面发生反应的能量—历程关系如图。下列说法错误的是
在羟基磷灰石(HAP)表面发生反应的能量—历程关系如图。下列说法错误的是
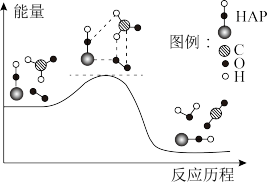
 在羟基磷灰石(HAP)表面发生反应的能量—历程关系如图。下列说法错误的是
在羟基磷灰石(HAP)表面发生反应的能量—历程关系如图。下列说法错误的是
| A.该反应为放热反应 |
| B.反应过程中,甲醛的C-H键断裂 |
C. 中的氧原子全部来自 中的氧原子全部来自 |
D.化学方程式为 |
您最近一年使用:0次
2023-02-25更新
|
1107次组卷
|
11卷引用:广东省深圳市2020-2021学年高一下学期期末调研考试化学试题
广东省深圳市2020-2021学年高一下学期期末调研考试化学试题广东省广州市执信中学2021-2022学年高一5月月考化学试题广东省广州市第六中学021-2022学年高一下学期期末考试化学试题广东省茂名市电白区2021-2022学年高一下学期期末(选择性)考试化学试题(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】福建省三明第一中学2022-2023学年高一下学期期中考试化学(选考)试题辽宁省名校联盟2022-2023学年高一下学期6月份联合考试化学试题 广东省佛山市第一中学2022-2023学年高一下学期5月月考化学试题广东广雅中学2023-2024学年高二上学期开学考化学试题四川省自贡市第一中学校2023-2024学年高二下学期开学考试化学试题河南省洛阳市强基联盟2023-2024学年高一下学期3月月考化学试题
5 . 已知充分燃烧a g乙炔气体生成44 g二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式是
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=2b kJ∙mol−1 |
B.C2H2(g)+  O2(g)=2CO2(g)+H2O(l);ΔH=−2b kJ∙mol−1 O2(g)=2CO2(g)+H2O(l);ΔH=−2b kJ∙mol−1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=4b kJ∙mol−1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=−b kJ∙mol−1 |
您最近一年使用:0次
名校
解题方法
6 . 实验室利用下列装置模拟工业生产制备少量硝酸。
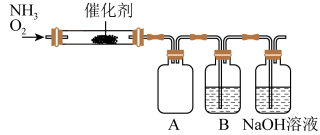
(1)实验结束时,两种反应气体中需要再持续通入_______ (填化学式)一段时间。
(2)B中反应的化学方程式为_______ 。
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是_______
(4)已知:①2H2(g)+O2(g)=2H2O(1) △H=-571.5kJ/mol
②N2(g)+2O2(g)=2NO2(g) △H=+68.0kJ/mol
③N2(g)+3H2(g)=2NH3(g) △H=-92.5kJ/mol
则:8NH3(g)+6NO2(g)=7N2(g)+12H2O(l) △H=_______ kJ/mol
(5)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。白烟是_______ (填化学式)。
②理论上使氨气完全转化为硝酸,则NH3与O2(相同条件下)的体积比应满足V(NH3):V(O2)_____ 。

(1)实验结束时,两种反应气体中需要再持续通入
(2)B中反应的化学方程式为
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是_______
A.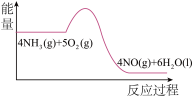 | B.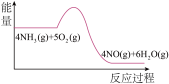 | C.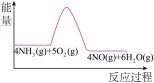 | D.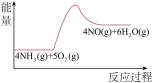 |
②N2(g)+2O2(g)=2NO2(g) △H=+68.0kJ/mol
③N2(g)+3H2(g)=2NH3(g) △H=-92.5kJ/mol
则:8NH3(g)+6NO2(g)=7N2(g)+12H2O(l) △H=
(5)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。白烟是
②理论上使氨气完全转化为硝酸,则NH3与O2(相同条件下)的体积比应满足V(NH3):V(O2)
您最近一年使用:0次
7 . 下列说法中错误的是
| A.燃烧一定有发光现象 | B.燃烧一定是氧化还原反应 |
| C.燃烧一定要有氧气参加 | D.燃烧一定要放出热量 |
您最近一年使用:0次
2023-01-13更新
|
228次组卷
|
47卷引用:北京市石景山区2020-2021学年高一上学期期末调研化学试卷题
北京市石景山区2020-2021学年高一上学期期末调研化学试卷题天津市和平区2020-2021学年高一上学期期末考试化学试题黑龙江省鹤岗市绥滨县第一中学2020-2021学年高一上学期期末考试化学(文)试题江苏省淮安市高中校协作体2020-2021学年高一下学期期中考试化学试题人教2019版必修第一册第二章第二节 氯及其化合物课后习题北京市第九中学2021-2022学年高一上学期期中考试化学试题新疆乌苏市第一中学2021-2022学年高一上学期期中考试化学试题天津市河东区三校2021-2022学年高一上学期期中考试化学试题黑龙江省密山市第四中学2021-2022学年高一上学期期中考试化学试题广西桂林市第十九中学2021-2022学年高一上学期期中质量检测化学试题北京市第十三中学2021-2022学年高一上学期期中考试化学试题(已下线)2011-2012学年吉林省长春外国语学校高一上学期期末考试文科化学试卷(已下线)2011-2012学年江苏省南通市小海中学高一上学期期末考试化学试卷(已下线)2011-2012学年河南省焦作市高一第一学期期末考试化学试卷(已下线)2012-2013学年河南省平顶山市高一上学期期末考试化学试卷2015-2016学年吉林省长春第十一高中高一上期末化学试卷2015-2016学年山西省临汾市曲沃中学高一上学期期末化学试卷2015-2016学年山西省曲沃中学高一上学期期末化学试卷2015-2016学年山西省晋城市高平市特立高中高二下期中文科化学试卷贵州省遵义市第四中学2015-2016学年高二上学期期中考试(文)化学试题黑龙江省牡丹江市第一高级中学2017-2018学年高二10月月考(文)化学试题吉林省长春外国语学校2017-2018学年高一上学期期末考试化学(文)试题云南省曲靖市宣威市第三中学2017-2018学年高二下学期3月月考化学试题【全国百强校】河北省武邑中学2017-2018学年高一下学期期末考试化学试题辽宁省阜新市第二高级中学2019-2020学年高一上学期第二次月考化学试题河北省石家庄市元氏县第四中学2020-2021学年高二上学期第一次月考化学试题北京市育才学校2020-2021高一上学期期中考试化学试题吉林省农安县伏龙泉镇中学2020-2021学年高一上学期期中考试化学试题吉林省长春市农安县2020-2021学年高一上学期期中考试化学试题辽宁省阜新市第二高级中学2020-2021学年高二上学期第二次月考化学试题辽宁省阜新市第二高级中学2020-2021学年高一上学期第二次月考化学试题北京市昌平区新学道临川学校2020-2021学年高一上学期12月月考化学试题(京津班)湖南省怀化市第五中学2019-2020学年高一下学期期中考试化学试题天津市河北区2021-2022学年高一上学期期末质量检测化学试题天津市河东区普通高中2022年高二学业水平合格考试模拟化学试题青海省西宁市大通回族土族自治县2021-2022学年高一上学期期末考试化学试题北京市铁路第二中学2022-2023学年高一上学期期中考试化学试题宁夏银川市第二中学2022-2023学年高一上学期期中考试化学试题北京教育学院附属中学2022-2023学年高一上学期期中练习化学试题天津市第四中学2022-2023学年高一上学期期末考试化学试题新疆疏勒县第一中学等3校2022-2023学年高一上学期1月期末考试化学试题宁夏吴忠市吴忠中学2023-2024学年高一上学期11月期中考试化学试题贵州省贵阳市2023-2024学年清镇市博雅实验学校高一第三次月考化学北京市铁路第二中学2023-2024学年高一上学期期中考试化学试题北京市第三中学2023-2024学年高一上学期期中考试化学试题北京市第一六一中学2023-2024学年高一上学期期中考试化学试题河南省商丘市柘城县德盛高级中学2023-2024学年高一上学期11月月考化学试题
8 . 下列反应属于吸热反应的是
| A.铝热反应 | B.木炭燃烧 | C.酸碱中和反应 | D.煅烧石灰石 |
您最近一年使用:0次
9 . 现有反应:
A.CaCO3 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
C.C+CO2 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O
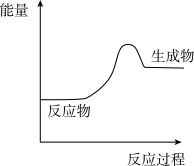
(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是_______ (填反应序号)。
(2)在常温下,上述四个反应中可用于设计原电池的是_______ (填反应序号),根据该原电池回答下列问题:
①负极发生_______ (填“氧化”或“还原”)反应;正极的电极反应式为_______ 。
②当导线中有1 mol电子通过时,理论上发生的变化是_______ (填序号)。
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
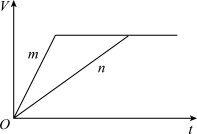
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。
反应速率变快的原因是_______(填序号)。
A.CaCO3
 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑C.C+CO2
 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是

(2)在常温下,上述四个反应中可用于设计原电池的是
①负极发生
②当导线中有1 mol电子通过时,理论上发生的变化是
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。

反应速率变快的原因是_______(填序号)。
| A.CuSO4作催化剂 |
B.加入硫酸铜溶液增大了c( ) ) |
| C.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池 |
| D.加入硫酸铜溶液增大了溶液体积 |
您最近一年使用:0次
名校
10 . 反应A+B→C分两步进行:①A+B→X(慢反应),②X→C(快反应),反应过程中能量变化如图所示,下列有关叙述正确的是
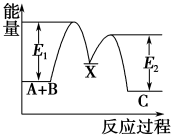
| A.反应A+B→C的ΔH>0 |
| B.X是反应A+B→C的催化剂 |
| C.反应A+B→C的快慢主要取决于反应① |
| D.E2表示反应X→C的活化能 |
您最近一年使用:0次
2022-12-28更新
|
196次组卷
|
5卷引用:宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题



