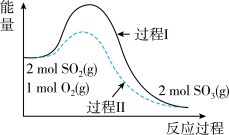
1 . 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
 2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
| A.该反应的△H>0 |
| B.反应物断键吸收的总能量小于生成物成键释放的总能量 |
| C.过程Ⅱ可能使用了催化剂,但不可以提高SO2的平衡转化率 |
| D.过程Ⅰ、Ⅱ达到平衡的时间不相同 |
您最近一年使用:0次
2 . 下列物质加入水中,显著放热的是
| A.生石灰 | B.固体Na2CO3 | C.无水乙醇 | D.固体硝酸铵 |
您最近一年使用:0次
解题方法
3 . 化学反应伴随着能量变化,下列说法正确的是
| A.需要加热的反应一定是吸热反应,不需要加热的反应一定是放热反应 |
B.单质硫燃烧热的热化学方程式:S(s)+ O2(g)=SO3(g) ΔH=a kJ·mol-1 O2(g)=SO3(g) ΔH=a kJ·mol-1 |
C.C(s,石墨) C(s,金刚石) ΔH=+1.9 kJ·mol-1,由此推断石墨比金刚石稳定 C(s,金刚石) ΔH=+1.9 kJ·mol-1,由此推断石墨比金刚石稳定 |
| D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
解题方法
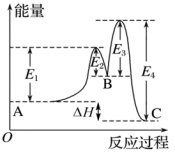
4 . 某反应由两步反应ABC构成,反应过程中的能量变化曲线如图所示(E1、E3表示两反应的活化能)。下列有关叙述正确的是

| A.两步反应均为放热反应 |
| B.整个反应的△H=E1-E2+E3-E4 |
| C.加入催化剂可以改变反应AC的焓变 |
| D.三种化合物中B最稳定 |
您最近一年使用:0次
5 . 下列说法正确的是
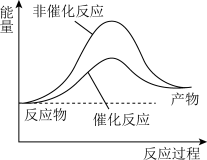

| A.如图可表示水分解过程中的能量变化 |
| B.若2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol,则碳的燃烧热ΔH为-110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
D.已知:Ⅰ. H2(g)+Cl2(g)=2HCl(g) ΔH=-a kJ/mol Ⅱ.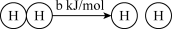 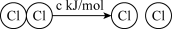 ,且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为(-a-b-c) ,且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为(-a-b-c) 。 。 |
您最近一年使用:0次
解题方法
6 . 回答下列问题
(1)下列反应中,属于放热反应的是__________ ,属于吸热反应的是________ 。
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有______________________ 。
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有____________ ;表示中和热的热化学方程式有_____________________ 。
(1)下列反应中,属于放热反应的是
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有
您最近一年使用:0次
7 . 下列过程既是氧化还原反应,又是吸热反应的是
| A.Na2O2溶于水 |
| B.Ba(OH)2·8H2O与NH4Cl(s)混合并搅拌 |
| C.灼热的炭与CO2反应 |
| D.铝热反应 |
您最近一年使用:0次
8 . 二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲醇是一种很有前景的方法。如下图所示为该反应在无催化剂及有催化剂时的能量变化。
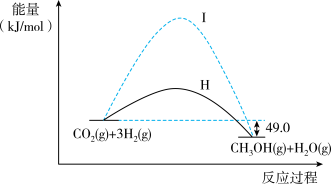
(1)从图可知,有催化剂存在的是过程_________ (填“Ⅰ”或“Ⅱ”)。
(2)写出图中CO2催化合成甲醇的热化学方程式:_________ 。
(3)若要提高反应速率,可以采取的措施有_________ 。
(4)若要提高上述可逆反应 中甲醇的平衡产率,可以采取的措施有_________ 。
(5)已知:1 mol液态甲醇完全气化需吸热37.4 kJ,1 mol液态水完全气化需吸热44.0 kJ,由CO2合成1 mol液态甲醇和1 mol液态水将_________ (填“吸收”或“放出”)_________ kJ热量。
(6)关于CO2催化合成甲醇的反应,下列说法中,合理的是_________ (填字母序号)。
a.该反应中所有原子都被用于合成甲醇
b.该反应可用于CO2的转化,有助于缓解温室效应
c.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量
d.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率

(1)从图可知,有催化剂存在的是过程
(2)写出图中CO2催化合成甲醇的热化学方程式:
(3)若要提高反应速率,可以采取的措施有
(4)若要提高上述
(5)已知:1 mol液态甲醇完全气化需吸热37.4 kJ,1 mol液态水完全气化需吸热44.0 kJ,由CO2合成1 mol液态甲醇和1 mol液态水将
(6)关于CO2催化合成甲醇的反应,下列说法中,合理的是
a.该反应中所有原子都被用于合成甲醇
b.该反应可用于CO2的转化,有助于缓解温室效应
c.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量
d.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率
您最近一年使用:0次
9 . 从能量变化看,有关H2在O2中燃烧的说法正确的是
| A.该反应是放热反应 | B.形成H-O键吸收能量 |
| C.断裂H-H键放出能量 | D.燃烧时化学能转化成电能 |
您最近一年使用:0次
10 . 科学家已获得了气态N4分子,其结构为正四面体形(如图所示)。已知断裂1molN-N键吸收193kJ能量,断裂1molN≡N键吸收946kJ能量,下列说法正确的是
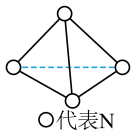

| A.N4属于一种新型的化合物 |
| B.N4(g)=4N(g)的过程中释放1158kJ能量 |
| C.56gN4转化为N2时要放出734kJ能量 |
| D.N4和N2互为同素异形体,N4转化为N2属于物理变化 |
您最近一年使用:0次



