1 .  和
和 联合重整能减少温室气体的排放,其主要反应为
联合重整能减少温室气体的排放,其主要反应为
①
②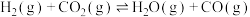
其他条件相同时,投料比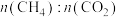 为1∶1.5,不同温度下反应的结果如图。
为1∶1.5,不同温度下反应的结果如图。

下列说法不正确的是
A.加压有利于增大 和 和 反应的速率但不利于提高二者的平衡转化率 反应的速率但不利于提高二者的平衡转化率 |
| B.550~600℃,升温更有利于反应①,反应①先达到平衡 |
C.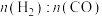 始终低于1.0,与反应②有关 始终低于1.0,与反应②有关 |
D.若不考虑其他副反应,体系中存在: |
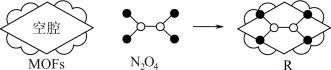
 可将其“固定”得到R(如图所示),实现从烟气中分离出
可将其“固定”得到R(如图所示),实现从烟气中分离出 并可制备
并可制备 。
。
已知反应

 。下列说法正确的是
。下列说法正确的是A.使用多孔超分子材料能降低反应 的活化能 的活化能 |
B.高温有利于从烟气中分离出 |
C.R在 中水洗,可制得 中水洗,可制得 同时实现MOFs再生 同时实现MOFs再生 |
D.该MOFs材料也可用于“固定”其他小分子,如NO、 等 等 |
汽车尾气中含有
 、
、 、
、 等大气污染物,可发生以下反应:
等大气污染物,可发生以下反应:Ⅰ.
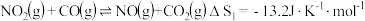
Ⅱ.

Ⅲ.
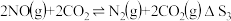
(1)
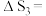
 忽略
忽略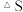 受温度的影响
受温度的影响 。
。(2)反应Ⅰ的平衡常数
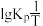 的关系如图
的关系如图 所示,则反应Ⅰ为
所示,则反应Ⅰ为 填“吸热”或“放热”
填“吸热”或“放热” 反应。温度为
反应。温度为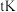 时,
时,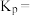
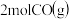 和
和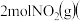 若只发生反应Ⅰ
若只发生反应Ⅰ ,测得起始压强为
,测得起始压强为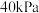 ,达到平衡时,
,达到平衡时, 的转化率为
的转化率为 的平衡分压为
的平衡分压为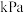 。
。
(3)将等物质的量的
 和
和 分别充入盛有催化剂
分别充入盛有催化剂 和
和 的体积相同的密闭容器中,进行反应Ⅲ,经过相同时间测量两容器中
的体积相同的密闭容器中,进行反应Ⅲ,经过相同时间测量两容器中 的含量,从而确定
的含量,从而确定 的转化率,结果如图
的转化率,结果如图 所示。试判断图像中
所示。试判断图像中 点是否一定处于平衡状态并分析原因:
点是否一定处于平衡状态并分析原因: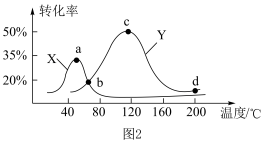
(4)间接电解法可对大气污染物
 进行无害化处理,工作原理如图
进行无害化处理,工作原理如图 所示,质子膜允许
所示,质子膜允许 和
和 通过。
通过。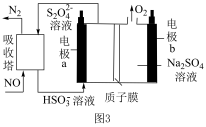
①电极
 的电极反应式为
的电极反应式为②工作时有
 通过质子膜时,理论上可处理标准状况下
通过质子膜时,理论上可处理标准状况下 的体积为
的体积为 。
。
4 . 近日,科学家开发新型催化剂实现一氧化二氮对C4馏分中2-丁烯的气相选择性氧化,反应原理如下:
反应l:CH3CH=CHCH3(g)+N2O(g)⇌CH3CH2COCH3(g)+N2(g) △H1
反应2:CH3CH=CHCH3(g)+2N2O(g)⇌2CH3CHO(g)+2N2(g) △H2<0
(1)几种共价键的键能数据如下表所示。
共价键 | C-H | C-C | C=C | C=O | N≡N | N=O | N=N |
键能/kJ·mol-1 | 413 | 347 | 614 | 745 | 945 | 607 | 418 |
已知N2O的结构与CO2相似,可表示为N=N=O。根据键能估算:△H1=
(2)某温度下,向恒压密闭容器中充入CH3CH=CHCH3(g)和N2O(g),发生上述反应1和反应2,测得平衡体系中N2的体积分数与起始投料比[
 ]的关系如图1所示,那么在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为
]的关系如图1所示,那么在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为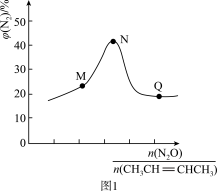
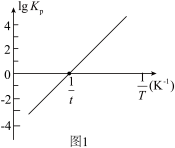
(3)已知:阿伦尼乌斯经验公式为Rlnk=-
 +C(R、C为常数,T为热力学温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,Rlnk与温度的倒数关系如图2所示,以此判断催化效果较高的催化剂是
+C(R、C为常数,T为热力学温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,Rlnk与温度的倒数关系如图2所示,以此判断催化效果较高的催化剂是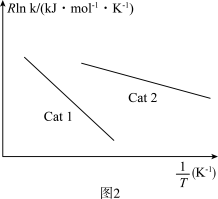
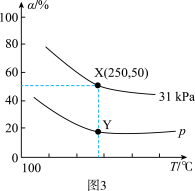
(4)在反应器中充入1mol2-丁烯和2molN2O(g),发生上述反应,测得2-丁烯的平衡转化率与温度、压强的关系如图3所示,X点时丁酮(CH3CH2COCH3)的选择性为
 。
。
已知:[CH3CH2COCH3的选择性= ]
]
①其他条件不变,升高温度,2-丁烯的平衡转化率降低的原因是
②p
③Y点反应1的压强平衡常数Kp为
(5)以熔融碳酸盐(如K2CO3)为电解质,丁烯(C4H8/空气燃料电池的能量转化率较高。电池总反应为C4H8+6O2=4CO2+4H2O,则负极的电极方程式为
选项 | 实验目的 | 方案设计 | 现象和结论 |
A | 探究温度对化学平衡的影响 | 加热盛有 溶液的试管 溶液的试管 | 加热,溶液变为绿色,冷却后变为蓝色,说明 转化为 转化为 的反应为吸热反应 的反应为吸热反应 |
B | 鉴别苏打和小苏打 | 在两支试管中分别取少量苏打和小苏打(各约 ),向两支试管分别滴入几滴水,用温度计插入其中测量温度 ),向两支试管分别滴入几滴水,用温度计插入其中测量温度 | 测量温度较高的是含小苏打的试管 |
C | 检验溴乙烷中含溴元素 | 加热溴乙烷与 的混合液,然后滴加 的混合液,然后滴加 溶液 溶液 | 有沉淀生成,说明溴乙烷中含溴元素 |
D | 探究 的氧化性 的氧化性 | 向溶有 的 的 溶液中滴入几滴 溶液中滴入几滴 溶液 溶液 | 有白色沉淀生成,说明 具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |

A.用图甲制备 消毒液 消毒液 |
B.用图乙以 标准溶液滴定未知浓度的盐酸 标准溶液滴定未知浓度的盐酸 |
C.用图丙由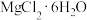 制备无水 制备无水 |
D.用图丁探究温度对 平衡移动的影响 平衡移动的影响 |
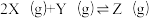
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是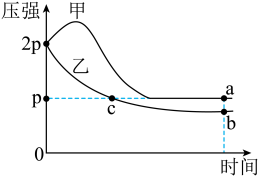
| A.△H>0 | B.气体的总物质的量:na>nc |
| C.a点平衡常数:K<12 | D.反应速率:Va正>Vb正 |
8 . 异丁烯( )是重要的化工原料,可由异丁醇(
)是重要的化工原料,可由异丁醇( )脱水制得。异丁醇催化脱水时发生如下反应:
)脱水制得。异丁醇催化脱水时发生如下反应:
反应1(主反应):

 (异丁烯,g)
(异丁烯,g)
反应2(副反应):2



 的混合气体(
的混合气体( 不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示。下列说法错误的是
不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示。下列说法错误的是
| A.反应1为消去反应,反应2为加成反应 |
| B.保持其他条件不变,升高温度,反应1和反应2平衡均向正反应方向移动 |
C.100MPa、200℃时,V(异丁醇) 起始比值越小,平衡时异丁烯的产率越高 起始比值越小,平衡时异丁烯的产率越高 |
D.100MPa、200℃时,若起始时将V(异丁醇) 改为V(异丁醇) 改为V(异丁醇) ,平衡时异丁烯的产率降低 ,平衡时异丁烯的产率降低 |
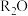 ,摩尔质量为Mg/mol)发生分解反应:
,摩尔质量为Mg/mol)发生分解反应: ,该反应平衡压强(
,该反应平衡压强(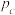 )与温度(
)与温度( )的关系如下表所示。
)的关系如下表所示。 温度下,向恒容容器中加入
温度下,向恒容容器中加入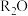 ,分解过程中反应速率
,分解过程中反应速率 与压强
与压强 的关系为
的关系为 ,
, 为速率常数(恒温为常数),当固体质量减少8%时,逆反应速率最大。下列说法正确的是
为速率常数(恒温为常数),当固体质量减少8%时,逆反应速率最大。下列说法正确的是 /K /K | 391 | 433 | 453 |
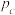 /kPa /kPa | 9 | 42 | 81 |
| A.该分解反应为放热反应 |
B.453K时反应的平衡常数 |
C. 温度下,向恒容容器中加入 温度下,向恒容容器中加入 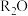 ,当 ,当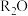 转化率为20%时, 转化率为20%时, 为 为 |
D.某温度下,1L恒容密闭容器中起始有 、 、 和 和 ,建立平衡状态Ⅰ后,恒温将体积变为2L,达平衡状态Ⅱ时,固体质量和起始固体质量相同,则建立平衡状态Ⅰ的过程中 ,建立平衡状态Ⅰ后,恒温将体积变为2L,达平衡状态Ⅱ时,固体质量和起始固体质量相同,则建立平衡状态Ⅰ的过程中 |
 基催化剂催化乙烷脱氢,但该催化剂对
基催化剂催化乙烷脱氢,但该催化剂对 键和
键和 键的断裂均有较高活性。方法二:乙烷催化氧化脱氢,反应历程如下图所示。下列说法正确的是
键的断裂均有较高活性。方法二:乙烷催化氧化脱氢,反应历程如下图所示。下列说法正确的是
A.方法一中可能形成碳单质沉积在 基催化剂表面使其失活,影响催化效率 基催化剂表面使其失活,影响催化效率 |
| B.方法二的反应历程中只涉及极性键的断裂和生成 |
| C.方法二中升高温度可提高反应的平衡产率 |
D.方法二中反应决速步骤的化学方程式为 |



