名校
解题方法
1 . 工业上利用锌焙砂(主要成分为 ,含有少量
,含有少量 、
、 、
、 等)生产高纯
等)生产高纯 的流程示意图如下。
的流程示意图如下。 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是_____ 。
②通过“浸出”步骤,锌焙砂中的 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(2)“浸出”时 转化为
转化为 。“除砷”步骤①中用
。“除砷”步骤①中用 作氧化剂。
作氧化剂。
i.指出 中
中 与
与 的化合价:
的化合价:_____ 。
ii.步骤①的离子方程式为_____ 。
(3)“除重金属”时加入 溶液。滤渣Ⅱ中含有的主要物质是
溶液。滤渣Ⅱ中含有的主要物质是_____ 和 。
。
(4)“蒸氨”时会出现白色固体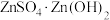 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:_____ 。
(5)“沉锌”步骤①中加入足量 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为_____ 。
(6)“煅烧”步骤中,不同温度下, 分解的失重曲线和产品
分解的失重曲线和产品 的比表面积变化情况如图甲、图乙所示。
的比表面积变化情况如图甲、图乙所示。
已知:i.固体失重质量分数=
ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品 的活性越高。
的活性越高。 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为_____ %(保留到小数点后一位)。
②根据图1和图2,获得高产率( 分解率
分解率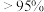 )、高活性(
)、高活性( 比表面积
比表面积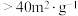 )产品
)产品 的最佳条件是
的最佳条件是_____ (填字母序号)。
a.恒温280℃,60~120min
b.恒温300℃,240~300min
c.恒温350℃,240~300min
d.恒温550℃,60~120min
(7)该流程中可循环利用的物质有_____ 。
 ,含有少量
,含有少量 、
、 、
、 等)生产高纯
等)生产高纯 的流程示意图如下。
的流程示意图如下。
已知: 结构如图所示
结构如图所示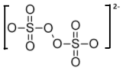
 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。①“浸出”前,锌焙砂预先粉碎的目的是
②通过“浸出”步骤,锌焙砂中的
 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为(2)“浸出”时
 转化为
转化为 。“除砷”步骤①中用
。“除砷”步骤①中用 作氧化剂。
作氧化剂。i.指出
 中
中 与
与 的化合价:
的化合价:ii.步骤①的离子方程式为
(3)“除重金属”时加入
 溶液。滤渣Ⅱ中含有的主要物质是
溶液。滤渣Ⅱ中含有的主要物质是 。
。(4)“蒸氨”时会出现白色固体
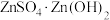 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:(5)“沉锌”步骤①中加入足量
 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为(6)“煅烧”步骤中,不同温度下,
 分解的失重曲线和产品
分解的失重曲线和产品 的比表面积变化情况如图甲、图乙所示。
的比表面积变化情况如图甲、图乙所示。已知:i.固体失重质量分数=

ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品
 的活性越高。
的活性越高。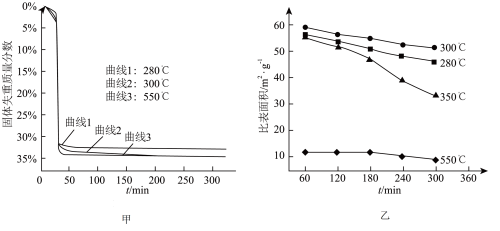
 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为②根据图1和图2,获得高产率(
 分解率
分解率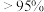 )、高活性(
)、高活性( 比表面积
比表面积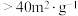 )产品
)产品 的最佳条件是
的最佳条件是a.恒温280℃,60~120min
b.恒温300℃,240~300min
c.恒温350℃,240~300min
d.恒温550℃,60~120min
(7)该流程中可循环利用的物质有
您最近一年使用:0次
名校
2 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。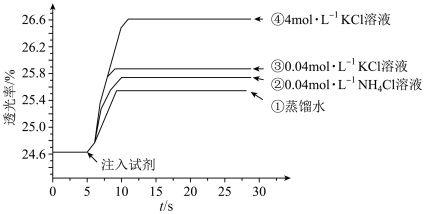
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近一年使用:0次
2023-11-21更新
|
363次组卷
|
7卷引用:北京市密云二中2023-2024学年高二上学期10月月考化学试卷
3 . 有机催化聚合反应有环境友好和储存容易等优点。一种有机催化聚合方法如下:

资料:KH是一种强碱。
下列说法中不正确的是

资料:KH是一种强碱。
下列说法中不正确的是
| A.反应①是取代反应 | B.KH可增大反应②中b的转化率 |
C.反应③中的另外一种产物可能是 | D. 为加聚反应 为加聚反应 |
您最近一年使用:0次
2023-05-07更新
|
213次组卷
|
2卷引用:北京市第五中学通州分校2023-2024学年高三上学期12月练习二化学试题
名校
4 . 碳酸二甲酯(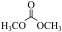 )是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
)是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
i.
ii.
(1)碳酸二甲酯分子中碳原子的杂化类型是___________ 。
(2)CuCl中,基态 的价电子排布式为
的价电子排布式为___________ ,CuCl在生产碳酸二甲酯的反应过程中所起的作用是___________ 。
(3)上述方法中,甲醇单位时间内的转化率较低。为分析原因,查阅如下资料。
i.甲醇单位时间内的转化率主要受 (+1价铜元素)浓度的影响。
(+1价铜元素)浓度的影响。
ii.CuCl在甲醇中溶解度较小,且其中的 易被氧化为难溶的CuO。
易被氧化为难溶的CuO。
iii.加入4-甲基咪唑(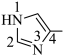 )可与
)可与 形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
请结合信息回答以下问题。
①4-甲基咪唑中,1~4号原子___________ (填“在”或“不在”)同一平面上,___________ (填“1”或“3”)号N原子更容易与 形成配位键。
形成配位键。
②加入4-甲基咪唑后,甲醇转化率提高,可能的原因是___________ (填序号)。
a. 配合物中的-NH结构可增大其在甲醇中的溶解度
配合物中的-NH结构可增大其在甲醇中的溶解度
b.通过形成配合物,避免 被氧化为难溶的CuO
被氧化为难溶的CuO
c.形成的 配合物能增大反应的限度
配合物能增大反应的限度
(4)配位原子提供孤电子对的能力是影响配体与 之间配位键强度的一个重要因素。若用某结构相似的含O配体与
之间配位键强度的一个重要因素。若用某结构相似的含O配体与 配位,所得配合物的稳定性比含N配体低,可能的原因是
配位,所得配合物的稳定性比含N配体低,可能的原因是___________ 。
 )是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
)是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。i.

ii.

(1)碳酸二甲酯分子中碳原子的杂化类型是
(2)CuCl中,基态
 的价电子排布式为
的价电子排布式为(3)上述方法中,甲醇单位时间内的转化率较低。为分析原因,查阅如下资料。
i.甲醇单位时间内的转化率主要受
 (+1价铜元素)浓度的影响。
(+1价铜元素)浓度的影响。ii.CuCl在甲醇中溶解度较小,且其中的
 易被氧化为难溶的CuO。
易被氧化为难溶的CuO。iii.加入4-甲基咪唑(
 )可与
)可与 形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。请结合信息回答以下问题。
①4-甲基咪唑中,1~4号原子
 形成配位键。
形成配位键。②加入4-甲基咪唑后,甲醇转化率提高,可能的原因是
a.
 配合物中的-NH结构可增大其在甲醇中的溶解度
配合物中的-NH结构可增大其在甲醇中的溶解度b.通过形成配合物,避免
 被氧化为难溶的CuO
被氧化为难溶的CuOc.形成的
 配合物能增大反应的限度
配合物能增大反应的限度(4)配位原子提供孤电子对的能力是影响配体与
 之间配位键强度的一个重要因素。若用某结构相似的含O配体与
之间配位键强度的一个重要因素。若用某结构相似的含O配体与 配位,所得配合物的稳定性比含N配体低,可能的原因是
配位,所得配合物的稳定性比含N配体低,可能的原因是
您最近一年使用:0次
名校
5 . 某同学进行如下实验:
①取少量稀盐酸放于试管中,投入光亮的铜片,无明显变化。
②向实验①的试管中通入足量的 ,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
③若将稀盐酸换成稀硫酸重复实验①和②,均无明显变化。
资料: 是白色固体,难溶于水,能溶于盐酸,
是白色固体,难溶于水,能溶于盐酸,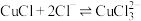 (棕色)
(棕色)
下列说法不正确 的是
①取少量稀盐酸放于试管中,投入光亮的铜片,无明显变化。
②向实验①的试管中通入足量的
 ,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。③若将稀盐酸换成稀硫酸重复实验①和②,均无明显变化。
资料:
 是白色固体,难溶于水,能溶于盐酸,
是白色固体,难溶于水,能溶于盐酸,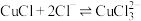 (棕色)
(棕色)下列说法
A.黑色固体不是 |
| B.将棕色溶液加水稀释,会产生白色沉淀 |
C.由实验①②能说明 增强了 增强了 的还原性 的还原性 |
D.上述过程中可能发生的反应: |
您最近一年使用:0次
2023-01-03更新
|
1022次组卷
|
7卷引用:北京师范大学附属实验中学2022-2023学年高二下学期3月月考化学试题
北京师范大学附属实验中学2022-2023学年高二下学期3月月考化学试题北京市第一七一中学2023-2024学年高三上学期10月考化学试题北京市海淀区2023届高三上学期期末考试化学试卷(已下线)北京市海淀区2022-2023学年高三上学期期末考试化学试卷(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(8-14)辽宁省东北育才学校2024届高三上学期高中学段联合考试化学试题湖北省襄阳市第五中学2023-2024学年高三上学期10月月考化学试题
名校
6 . 火法有色金属冶炼烟气制酸过程中会产生大量含砷污酸,采用硫化-石膏中和法处理含砷污酸可获得达标废水,同时实现变废为宝得到多级产品,工艺流程如下:
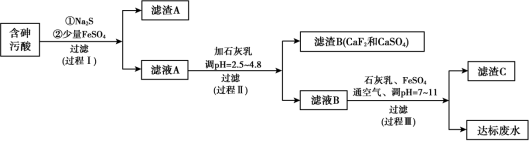
资料:
ⅰ. 常温下H2CO3的Ka1 = 4.4×10-7 ,Ka2 = 4.7×10-11;H2S的Ka1 = 1.3×10-7 ,Ka2 = 7.1×10-15;
ⅱ. 含砷污酸中砷的主要存在形式为亚砷酸(H3AsO3,弱酸),除砷外H+、Cu2+、F-、SO 含量均超标;
含量均超标;
ⅲ.室温下三价砷在水溶液中的存在形式与溶液pH的关系:
(1)工业上制备Na2S时,用NaOH溶液吸收H2S,不能以纯碱代替NaOH。结合方程式解释不能使用纯碱的原因___________ 。
(2)过程Ⅰ可除去含砷污酸中的Cu2+和部分砷,滤渣A 的主要成分为CuS和As2S3,生成As2S3的离子方程式是___________ 。
(3)过程Ⅰ会发生副反应As2S3(s)+3S2-(aq) 2AsS
2AsS (aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因
(aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因___________ 。
(4)过程Ⅲ中获得的滤渣C主要成分是FeAsO4, 该过程通入空气的作用是___________ 。
(5)利用反应AsO +2I-+2H+ =AsO
+2I-+2H+ =AsO +I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到
+I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到___________ 现象说明已到滴定终点,重复三次实验,记录用去Na2S2O3溶液体积为V mL,计算样品纯度为 ___________ (用字母表示)。
资料:2Na2S2O3+I2=Na2S4O6+2NaI;FeAsO4相对分子质量为195

资料:
ⅰ. 常温下H2CO3的Ka1 = 4.4×10-7 ,Ka2 = 4.7×10-11;H2S的Ka1 = 1.3×10-7 ,Ka2 = 7.1×10-15;
ⅱ. 含砷污酸中砷的主要存在形式为亚砷酸(H3AsO3,弱酸),除砷外H+、Cu2+、F-、SO
 含量均超标;
含量均超标;ⅲ.室温下三价砷在水溶液中的存在形式与溶液pH的关系:
| pH值 | pH<7 | pH=10~11 |
| 主要存在形式 | H3AsO3 | H2AsO |
(2)过程Ⅰ可除去含砷污酸中的Cu2+和部分砷,滤渣A 的主要成分为CuS和As2S3,生成As2S3的离子方程式是
(3)过程Ⅰ会发生副反应As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因
(aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因(4)过程Ⅲ中获得的滤渣C主要成分是FeAsO4, 该过程通入空气的作用是
(5)利用反应AsO
 +2I-+2H+ =AsO
+2I-+2H+ =AsO +I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到
+I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到资料:2Na2S2O3+I2=Na2S4O6+2NaI;FeAsO4相对分子质量为195
您最近一年使用:0次
2022-04-16更新
|
517次组卷
|
3卷引用:北京市第十二中学2022-2023学年高二下学期3月练习化学试题
北京市第十二中学2022-2023学年高二下学期3月练习化学试题北京市顺义区2021-2022学年高三下学期4月第二次统练化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)
名校
7 . 下列不能用勒夏特列原理解释的是
| A.FeCl3溶液配制时需将FeCl3固体溶于较浓盐酸中,再稀释到指定浓度 |
| B.硫酸工业中,SO2和O2化合成SO3(△H<0)过程采用高温、常压 |
| C.雪碧拧开瓶盖时看到液体内出现大量气泡并上浮 |
| D.NO2(红棕色)与N2O4(无色)转化达到平衡后,压缩体积到一半,颜色加深,但比两倍要浅 |
您最近一年使用:0次
2021-11-15更新
|
298次组卷
|
3卷引用:北京市第二中学2022-2023学年高二上学期11月月考化学试题
名校
8 . 下列实验操作或现象不能用平衡移动原理解释的是
A.卤化银沉淀的转化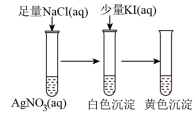 |
B.配制 溶液 溶液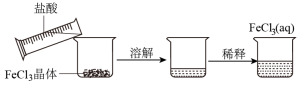 |
C.溶解淀粉在不同条件下水解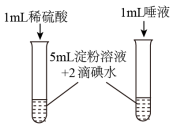 |
D.探究石灰石与稀盐酸在密闭环境下的反应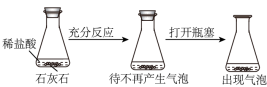 |
您最近一年使用:0次
2021-01-25更新
|
514次组卷
|
11卷引用:北京一零一中2021届高三上学期第三次统练化学试题
北京一零一中2021届高三上学期第三次统练化学试题北京市北京一零一中学2022-2023学年高三上学期统练7化学试题【区级联考】北京市东城区2019届高三下学期二模考试化学试题(已下线)2023-2024学年度第二学期高三化学零模试卷北京市师范大学附属实验中学2024届高三零模化学试题【校级联考】湖北省荆门市龙泉中学、钟祥一中、京山一中、沙洋中学四校2019届高三六月模拟考试化学试题【校级联考】辽宁省六校协作体2018-2019学年高二下学期期中考试化学试题广东省云浮市2019-2020学年高二上学期期末考试化学试题河南省新蔡县2020-2021学年高二上学期期末调研考试化学试题湖北省黄冈市2020-2021学年高二上学期期末调研考试化学试题2020届高三化学二轮冲刺新题专练——化学平衡移动及其影响因素
名校
解题方法
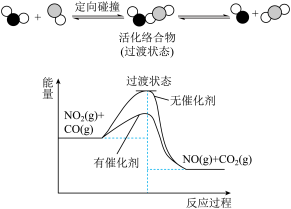
9 . 汽车尾气处理存在反应:NO2(g)+CO(g) NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( )
NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( )
 NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( )
NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( )
| A.升高温度,平衡正向移动 |
| B.该反应生成了具有非极性共价键的CO2 |
| C.反应物转化为活化络合物需要吸收能量 |
| D.使用催化剂可以有效提高反应物的平衡转化率 |
您最近一年使用:0次
2020-11-14更新
|
252次组卷
|
8卷引用:北京市第八中学 2020届高三下学期化学自主测试三
名校
解题方法
10 . 两个体积相同带活塞的容器,分别盛装一定量的NO2和Br2(g),都为一样的红棕色,迅速将两容器同时压缩到原来的一半(如图),假设气体不液化,则下列说法正确的是
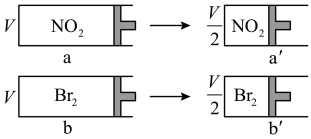

| A.a→a′过程中,颜色突然加深,然后逐渐变浅,最终颜色比原来的浅 |
| B.a′、b′的颜色一样深 |
| C.a′的压强比a的压强的2倍要小,b′的压强为b的压强的2倍 |
| D.a′中的c(NO2)一定比b′中的c(Br2)小 |
您最近一年使用:0次
2020-10-14更新
|
496次组卷
|
13卷引用:北京市第二中学2022-2023学年高二上学期10月月考化学试题
北京市第二中学2022-2023学年高二上学期10月月考化学试题安徽省定远重点中学2018-2019学年高二上学期第三次月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二10月月考化学试题云南省大姚县一中2020-2021学年高二下学期6月份考试化学试题黑龙江省哈尔滨市第六中学校2021-2022学年高二上学期10月阶段性总结化学试题广东省深圳市光明区高级中学2023-2024学年高二上学期10月月考化学试题北京市顺义区杨镇第一中学2023-2024学年高二上学期期中考试化学试题高二人教版选修4 第二章 章末基础排查(二)云南省马关县第二中学2019-2020学年高二上学期期末考试化学试题2020届福建高三化学总复习——--速率与平衡简答题吉林省四平市普通高中2021-2022学年高二上学期期中考试化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)陕西省咸阳市武功县2022-2023学年高二上学期期中考试化学试题



