名校
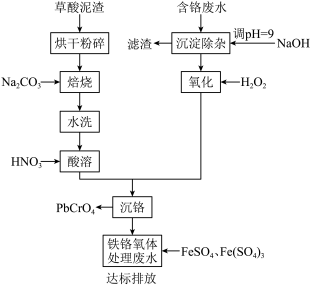
1 . 铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含Cr3+、Fe3+、Cu2+)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
回答下列问题
(1)草酸泥渣“粉碎”的目的是___________ ,“焙烧”时加入碳酸钠是为了将硫酸铅转化为PbO,同时放出CO2,该转化过程的化学方程式为___________ 。
(2)滤渣的主要成分为___________ 、___________ 。(填化学式)
(3)“沉淀除杂”所得滤液中含铬化合物主要为___________ 。(填化学式)
(4)“氧化”工序中发生反应的离子方程式为___________ 。
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因:___________ 。
(6)处理含 的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为___________ mol。

回答下列问题
(1)草酸泥渣“粉碎”的目的是
(2)滤渣的主要成分为
(3)“沉淀除杂”所得滤液中含铬化合物主要为
(4)“氧化”工序中发生反应的离子方程式为
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因:
(6)处理含
 的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
您最近一年使用:0次
2024-04-13更新
|
226次组卷
|
4卷引用:2024届江西省吉安市第一中学高三下学期一模化学试题
2024届江西省吉安市第一中学高三下学期一模化学试题(已下线)东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题东北三省四市2024届高三教研联合体高考模拟(一)化学试卷东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
名校
2 . 某学习小组欲利用 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取2 mL溶液X,加入5滴0.01 mol⋅L KSCN溶液,溶液红色
KSCN溶液,溶液红色_______ (填“变深”、“变浅”或“不变”,下同);取2 mL溶液X,插入经砂纸打磨过的铁丝,溶液红色_______ 。基于上述两个实验可以得到的结论是_______ 。
(2)取2 mL溶液X,加入5滴0.03 mol⋅L KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是_______ 或者不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.探究KCl对 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
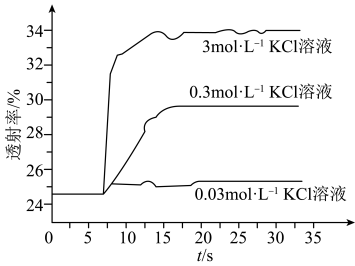
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响_______ 。二是_______ 。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:_______ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响
平衡体系产生的影响
资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。

上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是_______ 。盐效应影响较大的阳离子是_______ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:_______ 。
 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取2 mL溶液X,加入5滴0.01 mol⋅L
 KSCN溶液,溶液红色
KSCN溶液,溶液红色(2)取2 mL溶液X,加入5滴0.03 mol⋅L
 KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.探究KCl对
 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。猜想②:
 产生的影响。
产生的影响。猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响
平衡体系产生的影响资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L
 KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:
您最近一年使用:0次
2023-05-21更新
|
324次组卷
|
2卷引用:江西省萍乡中学、新余市第一中学2023-2024学年高二上学期10月创新班联考化学试题
名校
解题方法
3 . 某小组同学探究盐对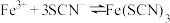 平衡体系的影响。
平衡体系的影响。
实验Ⅰ:探究KCl对 和
和 平衡体系的影响
平衡体系的影响
将等体积、低浓度的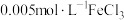 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和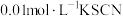 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
② 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。
(1)稀盐酸酸化 溶液的目的是
溶液的目的是___________ 。采用浓度较低的 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免___________ (填离子符号)的颜色对实验干扰。
(2)从实验结果来看,KCl溶液确实对 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向___________ (填“正”或“逆”)反应方向移动。
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。
(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
①上述实验可证明盐效应影响了 和
和 平衡体系的是
平衡体系的是___________ (填字母序号)。
a.1和2 b.1和3 c.1和4
②选择实验___________ (填序号)可得出结论: 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。
(4)取等体积的溶液a继续进行实验,结果如下表。
上述实验可证明副反应影响了 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:___________ 。
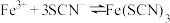 平衡体系的影响。
平衡体系的影响。实验Ⅰ:探究KCl对
 和
和 平衡体系的影响
平衡体系的影响将等体积、低浓度的
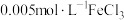 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和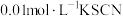 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②
 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。(1)稀盐酸酸化
 溶液的目的是
溶液的目的是 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免(2)从实验结果来看,KCl溶液确实对
 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使
 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。原因2:溶液中存在副反应
 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
| 序号 | 加入少量盐 | 溶液颜色 |
| 1 | 无 | 红色 |
| 2 | KCl | 变浅 |
| 3 |  | 略变浅 |
| 4 | NaCl | 变浅程度较大 |
 和
和 平衡体系的是
平衡体系的是a.1和2 b.1和3 c.1和4
②选择实验
 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。(4)取等体积的溶液a继续进行实验,结果如下表。
| 序号 | 加入溶液 | 溶液颜色 |
| 5 | 1mL浓盐酸 | 明显变浅,溶液偏黄 |
| 6 | 1mL去离子水 | 略变浅 |
 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:
您最近一年使用:0次
2023-04-20更新
|
117次组卷
|
4卷引用:江西省五校2022-2023学年高一下学期直升班联考化学试题
4 . 某小组同学探究盐对Fe3++3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响将已用稀盐酸酸化0.005mol·L-1FeCl3溶液(无色)和0.01mol·L-1KSCN溶液等体积混合,静置至体系达平衡,得红色溶液X。各取2mL溶液X放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
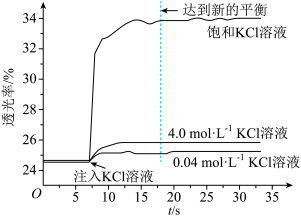
已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②Cl、 与Fe3+均能发生络合反应:Fe3++4C1-
与Fe3+均能发生络合反应:Fe3++4C1- [FeCl4]-(黄色)、Fe3++2
[FeCl4]-(黄色)、Fe3++2
 [Fe(SO4)2]-(无色)。
[Fe(SO4)2]-(无色)。
(1)稀盐酸酸化FeCl3溶液的目的是___________ 。(用离子方程式表示)。采用浓度较低的FeCl3溶液制备Fe3+和SCN-的平衡体系,是为了避免___________ (填离子符号)的颜色对实验干扰。
(2)从实验结果来看,KCl溶液确实对Fe3+和SCN-平衡体系有影响,且随着KCl浓度增大,Fe3++3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正反应”或“逆反应”)方向移动。
实验II:探究盐对Fe3+和SCN-平衡体系产生影响的原因
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使Fe3+和SCN-平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应Fe3++4C1- [FeCl4]-,离子浓度发生变化,导致Fe3+和SCN-平衡状态发生变化。
[FeCl4]-,离子浓度发生变化,导致Fe3+和SCN-平衡状态发生变化。
(3)基于以上分析,该组同学取2mL红色溶液X,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
基于以上实验现象可得出结论:K+的盐效应弱于Na+的盐效应。简述获得结论的依据:______ 。
(4)取2mL溶液X继续进行实验,结果如下表。
上述实验③和实验④可证明副反应影响了Fe3+和SCN-平衡体系,结合实验现象及化学用语分析副反应对Fe3+和SCN-平衡体系有影响的原因:___________ 。
实验III:探究现象a中溶液变为浅黄色的的原因
(5)由实验④、实验⑤和实验⑥可知,溶液变为浅黄色与___________ (填微粒的化学式)无关。
(6)为了进一步确认现象a中使溶液呈浅黄色的微粒只有Fe(SCN)3,补充完整实验⑦的操作___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响将已用稀盐酸酸化0.005mol·L-1FeCl3溶液(无色)和0.01mol·L-1KSCN溶液等体积混合,静置至体系达平衡,得红色溶液X。各取2mL溶液X放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②Cl、
 与Fe3+均能发生络合反应:Fe3++4C1-
与Fe3+均能发生络合反应:Fe3++4C1- [FeCl4]-(黄色)、Fe3++2
[FeCl4]-(黄色)、Fe3++2
 [Fe(SO4)2]-(无色)。
[Fe(SO4)2]-(无色)。(1)稀盐酸酸化FeCl3溶液的目的是
(2)从实验结果来看,KCl溶液确实对Fe3+和SCN-平衡体系有影响,且随着KCl浓度增大,Fe3++3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向实验II:探究盐对Fe3+和SCN-平衡体系产生影响的原因
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使Fe3+和SCN-平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应Fe3++4C1-
 [FeCl4]-,离子浓度发生变化,导致Fe3+和SCN-平衡状态发生变化。
[FeCl4]-,离子浓度发生变化,导致Fe3+和SCN-平衡状态发生变化。(3)基于以上分析,该组同学取2mL红色溶液X,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
| 序号 | 加入少量盐 | 溶液颜色 |
| ① | KCl | 变浅 |
| ② | NaCl | 变浅程度较大 |
(4)取2mL溶液X继续进行实验,结果如下表。
| 序号 | 加入溶液 | 溶液颜色 |
| ③ | 1mL蒸馏水 | 略变浅 |
| ④ | 1mL3mol·L-1盐酸 | 明显变浅,溶液偏黄 |
| ⑤ | 1mL1.5mol·L-1硫酸 | 现象a:溶液变为浅黄色 |
实验III:探究现象a中溶液变为浅黄色的的原因
| 序号 | 实验操作 | 溶液颜色 |
| ⑥ | 取1mL0.0025mol:L-1Fe2(SO4)3溶液(无色),加入1mL0.01mol·L-1KSCN溶液,再加入1mL1.5mol·L-1硫酸 | 溶液先变红,加入硫酸后变为浅黄色 |
| ⑦ | 取1mL0.005mol·L-1FeCl3溶液(无色) | 溶液为无色 |
(6)为了进一步确认现象a中使溶液呈浅黄色的微粒只有Fe(SCN)3,补充完整实验⑦的操作
您最近一年使用:0次
名校
解题方法
5 . 以辉铋矿(主要成分为Bi2S3,含有FeS2、SiO2杂质)和软锰矿(主要成分为MnO2)为原料制备超细氧化铋的工艺流程如图:
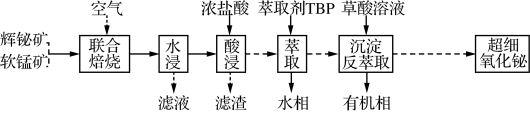
已知:Bi3+易与Cl-形成BiCl ,BiCl
,BiCl 易发生水解,其反应的离子方程式为BiCl
易发生水解,其反应的离子方程式为BiCl +H2O
+H2O BiOCl↓+5Cl-+2H+。
BiOCl↓+5Cl-+2H+。
(1)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4。该反应的化学方程式为_____ 。
(2)“酸浸”时需及时补充浓盐酸调节浸取液的pH。
①一般控制浸取液pH小于1.4,其目的是______ 。
②为提高酸浸时金属元素的浸出率,除适当增加浓盐酸用量、加快搅拌速度外,还可采取的措施有_____ 。
(3)铋离子能被有机萃取剂(简称TBP)萃取,其萃取原理可表示为BiCl (水层)+2TBP(有机层)
(水层)+2TBP(有机层) BiCl3•2TBP(有机层)+3Cl-(水层)。
BiCl3•2TBP(有机层)+3Cl-(水层)。
①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图1所示。c(Cl-)最佳为1.0mol•L-1的可能原因是______ 。

②萃取后分液所得水相中的主要阳离子为_____ (填化学式)。
(4)“沉淀反萃取”时生成草酸铋[Bi2(C2O4)3•7H2O]晶体。为得到含Cl-较少的草酸铋晶体,“萃取”后有机相与草酸溶液的混合方式为_____ 。
(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3•7H2O的质量的比值随温度变化的关系如图2所示。400℃时制得超细氧化铋,其化学式为_____ 。(写出计算过程,M[Bi2(C2O4)3•7H2O]=808g•mol-1)


已知:Bi3+易与Cl-形成BiCl
 ,BiCl
,BiCl 易发生水解,其反应的离子方程式为BiCl
易发生水解,其反应的离子方程式为BiCl +H2O
+H2O BiOCl↓+5Cl-+2H+。
BiOCl↓+5Cl-+2H+。(1)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4。该反应的化学方程式为
(2)“酸浸”时需及时补充浓盐酸调节浸取液的pH。
①一般控制浸取液pH小于1.4,其目的是
②为提高酸浸时金属元素的浸出率,除适当增加浓盐酸用量、加快搅拌速度外,还可采取的措施有
(3)铋离子能被有机萃取剂(简称TBP)萃取,其萃取原理可表示为BiCl
 (水层)+2TBP(有机层)
(水层)+2TBP(有机层) BiCl3•2TBP(有机层)+3Cl-(水层)。
BiCl3•2TBP(有机层)+3Cl-(水层)。①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图1所示。c(Cl-)最佳为1.0mol•L-1的可能原因是

②萃取后分液所得水相中的主要阳离子为
(4)“沉淀反萃取”时生成草酸铋[Bi2(C2O4)3•7H2O]晶体。为得到含Cl-较少的草酸铋晶体,“萃取”后有机相与草酸溶液的混合方式为
(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3•7H2O的质量的比值随温度变化的关系如图2所示。400℃时制得超细氧化铋,其化学式为

您最近一年使用:0次
2023-03-14更新
|
581次组卷
|
3卷引用:江西省吉安市第三中学2023届高三一模考试化学试题
解题方法
6 . 碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制备CuI,并设计实验探究其性质。已知:碘化亚铜(CuI)是白色固体,难溶于水,易与KI形成K[CuI2]实验装置如图1所示。
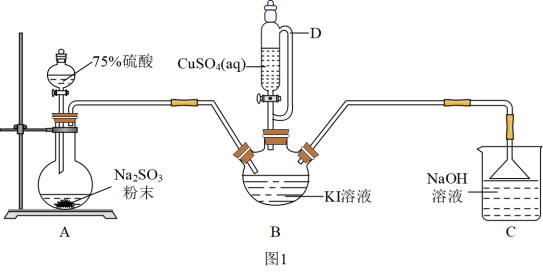
(1)仪器D的名称是________ 。
(2)实验完毕后,用图2所示装置分离CuI的突出优点是_______ 。
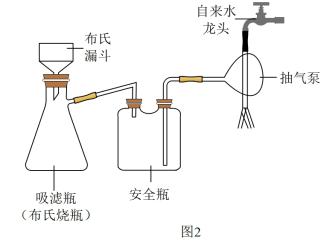
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:_______ 。
(4)装置B中发生反应的离子方程式是_______ 。
(5)小组同学设计下表方案对CuI的性质进行探究:
①在实验I中“加水,又生成白色沉淀”的原理是_______ 。
②根据实验II,CuI与NaOH溶液反应的化学方程式是_______ 。
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为_______ (用含a、b、V的代数式表示)。如果其他操作均正确,仅滴定前盛标准液的滴定管用蒸馏水洗净后没有用标准液润洗,测得结果_______ (填“偏高”“偏低”或“无影响”)。

(1)仪器D的名称是
(2)实验完毕后,用图2所示装置分离CuI的突出优点是

(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:
(4)装置B中发生反应的离子方程式是
(5)小组同学设计下表方案对CuI的性质进行探究:
| 实验 | 实验操作及现象 |
| Ⅰ | 取少量CuI放入试管中,加入KI溶液,白色固体溶解得到无色溶液;加水,又生成白色沉淀 |
| Ⅱ | 取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀。过滤,向所得上层清液中滴加淀粉溶液,无明显变化;将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液 |
②根据实验II,CuI与NaOH溶液反应的化学方程式是
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2
 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为
您最近一年使用:0次
解题方法
7 . 工业上合成氨的化学反应,在容积为10L的密闭容器中,通入40molN2和120molH2在一定条件下进行反应,4s后达到平衡状态,此时N2的浓度为2mol/L。通过计算回答下列问题:
(1)用N2表示的4s内化学反应的平均速率是___________ 。
(2)若生成17g氨气,放出46.2kJ热量,写出生成2摩尔氨反应的热化学方程式___________ 。
(3)若外界条件改变为降低温度,则平衡向___________ (填“正反应”或“逆反应”)方向移动,达到平衡后,N2的物质的量浓度___________ (填“大于、小于、等于”)2mol/L
(4)上述反应达到平衡后,在其它条件不变的情况下,通过增大容器体积减小压强,则NH3的合成率___________ (填“增大”“减少”或“不变”)。
(1)用N2表示的4s内化学反应的平均速率是
(2)若生成17g氨气,放出46.2kJ热量,写出生成2摩尔氨反应的热化学方程式
(3)若外界条件改变为降低温度,则平衡向
(4)上述反应达到平衡后,在其它条件不变的情况下,通过增大容器体积减小压强,则NH3的合成率
您最近一年使用:0次
名校
8 . 1776年,法国化学家LaVoisier首次确定硫元素。自然界天然的硫单质主要存在于火山区,发生反应如下(a、b均大于0):ⅰ.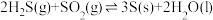
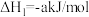 ;
;
ⅱ. 。回答下列问题:
。回答下列问题:
(1)根据上述信息, )
) 
_______ kJ/mol。推测a____ b或(填“>”“<”或“=”)。
(2)一定温度下,在恒容密闭容器中充入适量的 、
、 和
和 气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
(3)一定温度下,向2L密闭容器中充入 和
和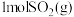 ,仅发生反应①,达到平衡后,测得
,仅发生反应①,达到平衡后,测得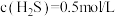 。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
_______ mol/L。
(4)在恒容密闭容器中充入一定量 和
和 气体,测得
气体,测得 的平衡转化率与温度、投料比
的平衡转化率与温度、投料比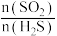 关系如图所示。
关系如图所示。
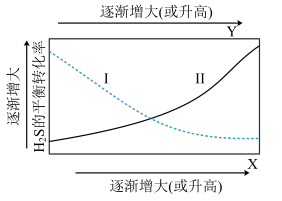
①代表 的平衡转化率随温度变化的曲线为
的平衡转化率随温度变化的曲线为_______ 。
②解释曲线Ⅱ变化趋势:_______ 。
(5)一定温度下,向密闭容器中充入 、
、 和
和 ,达到平衡时测得平衡体系中有
,达到平衡时测得平衡体系中有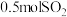 和
和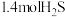 ,平衡时总压强为21kPa。该温度下,反应②的平衡常数
,平衡时总压强为21kPa。该温度下,反应②的平衡常数
_______ 。(不要求带单位,可用分数表示,提示:用分压计算的平衡常数为 ,分压等于总压×物质的量分数)。
,分压等于总压×物质的量分数)。
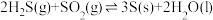
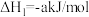 ;
;ⅱ.
 。回答下列问题:
。回答下列问题:(1)根据上述信息,
 )
) 
(2)一定温度下,在恒容密闭容器中充入适量的
 、
、 和
和 气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
气体,仅发生上述反应。下列叙述正确的是_______(填字母)。| A.混合气体密度不再随时间变化时达到平衡状态 |
| B.增大硫单质的质量,逆反应速率会增大 |
C.达到平衡后,适当升温, 的平衡转化率减小 的平衡转化率减小 |
| D.平衡后充入少量惰性气体(不反应),平衡向左移动 |
 和
和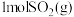 ,仅发生反应①,达到平衡后,测得
,仅发生反应①,达到平衡后,测得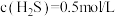 。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
(4)在恒容密闭容器中充入一定量
 和
和 气体,测得
气体,测得 的平衡转化率与温度、投料比
的平衡转化率与温度、投料比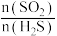 关系如图所示。
关系如图所示。
①代表
 的平衡转化率随温度变化的曲线为
的平衡转化率随温度变化的曲线为②解释曲线Ⅱ变化趋势:
(5)一定温度下,向密闭容器中充入
 、
、 和
和 ,达到平衡时测得平衡体系中有
,达到平衡时测得平衡体系中有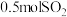 和
和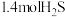 ,平衡时总压强为21kPa。该温度下,反应②的平衡常数
,平衡时总压强为21kPa。该温度下,反应②的平衡常数
 ,分压等于总压×物质的量分数)。
,分压等于总压×物质的量分数)。
您最近一年使用:0次
2022-12-15更新
|
356次组卷
|
3卷引用:江西省2022-2023学年高二上学期12月统一调研测试(联考)化学试题
解题方法
9 . 兴趣小组同学为探究影响化学反应速率及化学平衡的因素,设计以下实验:

(1)利用实验I探究锌与稀硫酸反应的速率,需要记录的实验数据有:___________ 。
(2)利用实验II探究浓度对化学平衡的影响。已知: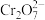 (橙色)
(橙色)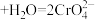 (黄色)
(黄色)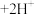 ,推测B试管中的实验现象为:
,推测B试管中的实验现象为:___________ ,用平衡移动原理解释其原因:___________ 。
(3)该小组同学继续用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,设计实验方案如表所示。请回答相关问题:
)溶液进行实验,设计实验方案如表所示。请回答相关问题:
①实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定___________ 来判断反应的快慢。
②实验a、b、c所加的 溶液均要过量。理由是
溶液均要过量。理由是___________ 。
③实验a和b是探究___________ 对化学反应速率的影响。实验b和c是探究___________ 对化学反应速率的影响。
④实验a和b起初反应均很慢,过了一会儿速率突然增大,可能原因是___________ 。

(1)利用实验I探究锌与稀硫酸反应的速率,需要记录的实验数据有:
(2)利用实验II探究浓度对化学平衡的影响。已知:
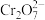 (橙色)
(橙色)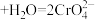 (黄色)
(黄色)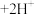 ,推测B试管中的实验现象为:
,推测B试管中的实验现象为:(3)该小组同学继续用酸性
 溶液和草酸(
溶液和草酸( )溶液进行实验,设计实验方案如表所示。请回答相关问题:
)溶液进行实验,设计实验方案如表所示。请回答相关问题:| 编号 | 温度℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度/( ) ) | 体积/mL | 浓度/( ) ) | 体积/mL | ||
| a | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| b | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| c | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定②实验a、b、c所加的
 溶液均要过量。理由是
溶液均要过量。理由是③实验a和b是探究
④实验a和b起初反应均很慢,过了一会儿速率突然增大,可能原因是
您最近一年使用:0次
名校
10 . 研究氮氧化物、碳氧化物的产生及利用有重要的化学意义。回答下列问题:
(1)汽车燃料中不含氮元素,汽车尾气中所含NO产生的原因是_______ 。
(2)将SrCO3放入密闭的真空容器中,发生反应SrCO3(s)⇌SrCO3(s)+CO2(g),反应达到平衡时c(CO2)为x mol/L,如反应温度不变,将反应体系的体积快速压缩为原来的一半,则c(CO2)的变化范围为_______ 。
(3)用CO2和H2在一定条件下可转化生成甲醇蒸气和水蒸气:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H
已知部分化学键键能如表所示:
①∆H=_______ kJ∙mol-1;
②一定条件下,在相同体积的恒容密闭容器中充入1.0mol CO2和3.0mol H2,相同时间段内测得CO2的转化率随温度变化如图所示:
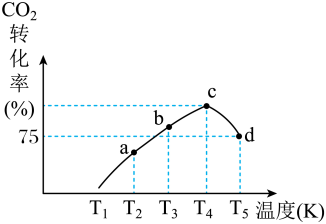
d点v正_______ v逆(填“>”“<”或“=”)。已知容器内的起始压强为160kPa,则图中d点对应温度下反应的平衡常数Kp=_______ kPa-2(KP为以分压表示的平衡常数,分压=总压×物质的量分数)
(1)汽车燃料中不含氮元素,汽车尾气中所含NO产生的原因是
(2)将SrCO3放入密闭的真空容器中,发生反应SrCO3(s)⇌SrCO3(s)+CO2(g),反应达到平衡时c(CO2)为x mol/L,如反应温度不变,将反应体系的体积快速压缩为原来的一半,则c(CO2)的变化范围为
(3)用CO2和H2在一定条件下可转化生成甲醇蒸气和水蒸气:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H
已知部分化学键键能如表所示:
| 化学键 | H-H | C=O | C-O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 745 | 351 | 463 | 413 |
②一定条件下,在相同体积的恒容密闭容器中充入1.0mol CO2和3.0mol H2,相同时间段内测得CO2的转化率随温度变化如图所示:

d点v正
您最近一年使用:0次



