名校
1 . 一定温度下,恒容密闭容器中,某可逆反应达到平衡,其平衡常数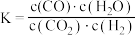 ,升高温度,
,升高温度, 减小,下列说法正确的是
减小,下列说法正确的是
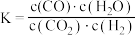 ,升高温度,
,升高温度, 减小,下列说法正确的是
减小,下列说法正确的是A.该反应的 |
| B.升高温度,K值减小 |
| C.升高温度,逆反应速率减小 |
D.该反应为 |
您最近一年使用:0次
2 .  时,向
时,向 密闭容器中充入
密闭容器中充入 和
和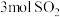 发生反应:
发生反应: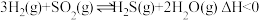 。部分物质的物质的量
。部分物质的物质的量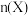 随时间t变化如图实线所示。下列说法正确的是
随时间t变化如图实线所示。下列说法正确的是
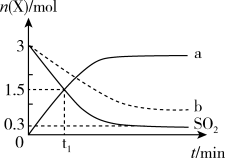
 时,向
时,向 密闭容器中充入
密闭容器中充入 和
和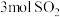 发生反应:
发生反应: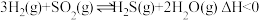 。部分物质的物质的量
。部分物质的物质的量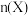 随时间t变化如图实线所示。下列说法正确的是
随时间t变化如图实线所示。下列说法正确的是
A.该反应的平衡常数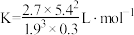 |
B. 时, 时, |
C.曲线a代表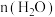 随时间变化的曲线 随时间变化的曲线 |
D.若该反应在 时进行,则虚线b可表示 时进行,则虚线b可表示 的变化 的变化 |
您最近一年使用:0次
2022-07-10更新
|
1413次组卷
|
11卷引用:内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题
内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题广东省深圳市2022届高三下学期第二次调研考化学试题(已下线)化学-2022年高考考前押题密卷(重庆卷)福建省漳平第一中学、永安一中 2022届高考前高三毕业班联考化学试题(已下线)2022年广东卷高考真题变式题(11-16)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)湖南省株洲市茶陵县第一中学2022届高三下学期期中考试化学试题(已下线)2022年北京高考真题变式题1-14安徽省舒城晓天中学2022-2023学年高二上学期期中考试化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)广东省潮州市2022-2023学年高三下学期第二次模拟考试化学试题
名校
解题方法
3 . 在160℃、200℃条件下,分别向两个容积为2L的刚性容器中充入2molCO和2mol ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是

 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是
A.ac段 的平均反应速率为 的平均反应速率为 |
| B.逆反应速率:c=d>b |
| C.160℃时,该反应的平衡常数K=9 |
| D.当容器中混合气体的密度不随时间变化时,该反应达到平衡状态 |
您最近一年使用:0次
2022-07-01更新
|
214次组卷
|
6卷引用:内蒙古包钢第一中学2022-2023学年高二上学期月考化学试题
名校
解题方法
4 . 反应 在1000K时
在1000K时 ,当总压为101kPa,气体组成是
,当总压为101kPa,气体组成是 ,
, ,
, 时,上述反应
时,上述反应
 在1000K时
在1000K时 ,当总压为101kPa,气体组成是
,当总压为101kPa,气体组成是 ,
, ,
, 时,上述反应
时,上述反应| A.正向移动 | B.逆向移动 | C.达到平衡 | D.不一定 |
您最近一年使用:0次
名校
5 . 已知下列反应的平衡常数:①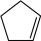 (g)=
(g)=
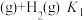 ;②
;②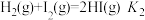 ;则反应
;则反应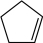
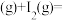
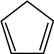
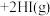 的平衡常数是
的平衡常数是
 (g)=
(g)=
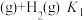 ;②
;②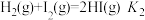 ;则反应
;则反应
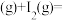

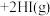 的平衡常数是
的平衡常数是A.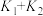 | B.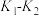 | C. | D.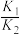 |
您最近一年使用:0次
6 . 二氧化碳减排和再利用技术是促进社会环保和工业可持续发展的重要措施。将工业废气中的 转化为
转化为 ,可以通过以下途径实现。
,可以通过以下途径实现。
反应Ⅰ:

反应Ⅱ:
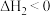
反应Ⅲ:

反应Ⅰ和反应Ⅱ的平衡常数K随温度T的变化如图所示。
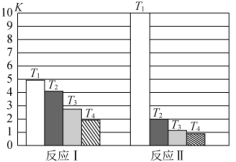
下列说法错误的是
 转化为
转化为 ,可以通过以下途径实现。
,可以通过以下途径实现。反应Ⅰ:


反应Ⅱ:

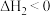
反应Ⅲ:


反应Ⅰ和反应Ⅱ的平衡常数K随温度T的变化如图所示。

下列说法错误的是
| A.反应Ⅰ、Ⅱ都是放热反应 | B.温度: |
C.反应Ⅲ的 | D. 时反应Ⅲ的平衡常数 时反应Ⅲ的平衡常数 |
您最近一年使用:0次
2022-03-22更新
|
147次组卷
|
6卷引用:内蒙古乌兰察布市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 实验:①将0.1 mol·L-1的AgNO3溶液和0.1 mol·L-1的NaCl溶液等体积混合,得到浊液a,过滤,得到滤液b和白色沉淀c;
②取一部分沉淀c,向其中滴加0.1 mol·L-1的 KI溶液,沉淀变为黄色(AgI);
KI溶液,沉淀变为黄色(AgI);
③往剩余的沉淀c中滴加0.1 mol·L-1的KBr溶液,沉淀变为淡黄色(AgBr)。
通过以上实验进行分析,下列有关结论不正确的是
②取一部分沉淀c,向其中滴加0.1 mol·L-1的
 KI溶液,沉淀变为黄色(AgI);
KI溶液,沉淀变为黄色(AgI);③往剩余的沉淀c中滴加0.1 mol·L-1的KBr溶液,沉淀变为淡黄色(AgBr)。
通过以上实验进行分析,下列有关结论不正确的是
A.滤液b中:c(Na+)=c(NO ) ) |
B.实验②中反应达到平衡时,平衡常数表达式为K= |
C.实验③中发生反应的化学方程式为AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq) AgBr(s)+Cl-(aq) |
| D.根据实验②③可得出:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI) |
您最近一年使用:0次
2021-08-30更新
|
561次组卷
|
4卷引用:内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题
内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题河南省新乡市2020-2021学年高二下学期期末考试化学试题(已下线)高中化学《新教材变化解读与考法剖析》第三章 水溶液中的离子反应与平衡(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)
名校
解题方法
8 . Ⅰ.工业上常用如下反应消除氮氧化物的污染:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O
(g) △H。回答下面问题:
(1)在某绝热容器中进行上述反应,下列能说明反应一定达到平衡状态的是_______ 。
A.当容器内温度不变时
B.当恒容混合气体密度不变时
C.当混合气体的颜色不变时
D.当恒压混合气体的总压强不变时
(2)在温度为T1和T2时,分别将0.40molCH4和1.0molNO2,充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示。
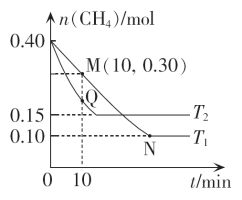
①温度为T1时,0~10min内NO2的平均反应速率v(NO2)=_______ 。
②温度为T2时,该反应的平衡常数K=_______ (保留两位有效数字)。
③下列措施中,能够使上述平衡正向移动,且提高NO2转化率的有_______ 。
A.使用高效催化剂
B.增加CH4的充入量
C.缩小容器体积,增大压强
D.恒容时,再次充入0.40molCH4和1.0molNO2
E.降低温度
Ⅱ.(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH 3-4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ ,(从下面四个选项选择)调整溶液的pH3-4,使Fe3+转化为Fe(OH)3沉淀。
A.H2O2 B.CuO C.Cl2 D.Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据:常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,通过计算确定上述方案_______ (填“可行”或“不可行”)。
(g) △H。回答下面问题:
(1)在某绝热容器中进行上述反应,下列能说明反应一定达到平衡状态的是
A.当容器内温度不变时
B.当恒容混合气体密度不变时
C.当混合气体的颜色不变时
D.当恒压混合气体的总压强不变时
(2)在温度为T1和T2时,分别将0.40molCH4和1.0molNO2,充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示。

①温度为T1时,0~10min内NO2的平均反应速率v(NO2)=
②温度为T2时,该反应的平衡常数K=
③下列措施中,能够使上述平衡正向移动,且提高NO2转化率的有
A.使用高效催化剂
B.增加CH4的充入量
C.缩小容器体积,增大压强
D.恒容时,再次充入0.40molCH4和1.0molNO2
E.降低温度
Ⅱ.(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH 3-4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:为除去溶液中的Fe2+,可先加入
A.H2O2 B.CuO C.Cl2 D.Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据:常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,通过计算确定上述方案
您最近一年使用:0次
2021-03-13更新
|
108次组卷
|
2卷引用:内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题



