1 . 钛 由于其稳定的化学性质,良好的耐高温、耐低温、抗腐蚀,以及高强度、低密度,被誉为“太空金属”。工业上制金属钛是先将金红石
由于其稳定的化学性质,良好的耐高温、耐低温、抗腐蚀,以及高强度、低密度,被誉为“太空金属”。工业上制金属钛是先将金红石 和炭粉混合加热至
和炭粉混合加热至 ,进行氯化处理,发生反应如下:
,进行氯化处理,发生反应如下:
 。再采用金属热还原法还原四氯化钛得到钛。
。再采用金属热还原法还原四氯化钛得到钛。
(1)氯化反应的平衡常数表达式
_______ 。若反应容器的容积为 后达到平衡,测得固体的质量减少了
后达到平衡,测得固体的质量减少了 ,则
,则 的平均反应速率为
的平均反应速率为_______ 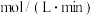 。
。
(2)上述反应达到平衡后,下列说法正确的是_______  选填编号,下同
选填编号,下同 。
。
 其他条件不变,增大
其他条件不变,增大 的质量,
的质量, 的转化率提高
的转化率提高
 其他条件不变,升高温度,平衡常数
其他条件不变,升高温度,平衡常数 减小
减小
 其他条件不变,减小压强,平衡向右移动
其他条件不变,减小压强,平衡向右移动
 其他条件不变,分离出
其他条件不变,分离出 ,正反应速率增大
,正反应速率增大
(3)一定条件下,在密闭恒容的容器中,无法表示上述反应达到化学平衡状态的是_______ 。
a. b.
b.
c. d.混合气体密度保持不变
d.混合气体密度保持不变
(4)若平衡时 和
和 的物质的量之比为
的物质的量之比为 ,保持其他条件不变,升高温度后达到新的平衡时,
,保持其他条件不变,升高温度后达到新的平衡时, 和
和 的物质的量之比
的物质的量之比_______  填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” 。
。
 由于其稳定的化学性质,良好的耐高温、耐低温、抗腐蚀,以及高强度、低密度,被誉为“太空金属”。工业上制金属钛是先将金红石
由于其稳定的化学性质,良好的耐高温、耐低温、抗腐蚀,以及高强度、低密度,被誉为“太空金属”。工业上制金属钛是先将金红石 和炭粉混合加热至
和炭粉混合加热至 ,进行氯化处理,发生反应如下:
,进行氯化处理,发生反应如下:
 。再采用金属热还原法还原四氯化钛得到钛。
。再采用金属热还原法还原四氯化钛得到钛。(1)氯化反应的平衡常数表达式

 后达到平衡,测得固体的质量减少了
后达到平衡,测得固体的质量减少了 ,则
,则 的平均反应速率为
的平均反应速率为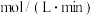 。
。(2)上述反应达到平衡后,下列说法正确的是
 选填编号,下同
选填编号,下同 。
。 其他条件不变,增大
其他条件不变,增大 的质量,
的质量, 的转化率提高
的转化率提高 其他条件不变,升高温度,平衡常数
其他条件不变,升高温度,平衡常数 减小
减小 其他条件不变,减小压强,平衡向右移动
其他条件不变,减小压强,平衡向右移动 其他条件不变,分离出
其他条件不变,分离出 ,正反应速率增大
,正反应速率增大(3)一定条件下,在密闭恒容的容器中,无法表示上述反应达到化学平衡状态的是
a.
 b.
b.
c.
 d.混合气体密度保持不变
d.混合气体密度保持不变(4)若平衡时
 和
和 的物质的量之比为
的物质的量之比为 ,保持其他条件不变,升高温度后达到新的平衡时,
,保持其他条件不变,升高温度后达到新的平衡时, 和
和 的物质的量之比
的物质的量之比 填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” 。
。
您最近一年使用:0次
2 . 一定温度下,某气态平衡体系的平衡常数表达式为 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是A.升高温度,平衡常数 一定增大 一定增大 |
B.增大 浓度,平衡向正反应方向移动 浓度,平衡向正反应方向移动 |
| C.增大压强,C体积分数增加 |
D.升高温度,若 的百分含量减少,则正反应是放热反应 的百分含量减少,则正反应是放热反应 |
您最近一年使用:0次
3 . 臭氧是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。臭氧可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生如下反应①:O3⇌O2+[O] ΔH>0平衡常数为Ka,反应②:[O]+O3⇌2O2 ΔH<0平衡常数为Kb,总反应:2O3⇌3O2 ΔH<0平衡常数为K。下列说法错误的是
| A.降低温度,K减小 | B.K=Ka·Kb |
| C.适当升温,可提高消毒效率 | D.压强增大,Kb不变 |
您最近一年使用:0次
名校
解题方法
4 . 铁及其化合物的制备与性质探究。
I.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如下装置制备FeCO3(夹持装置略)。
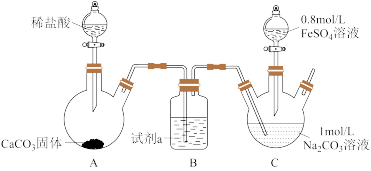
具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为_______ 。
(2)写出整个实验过程中C中发生反应的离子方程式_______ 。
(3)某实验小组用酸性高锰酸钾标准液去测定补血剂中乳酸亚铁含量,从而计算乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是_______ 。
II.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。
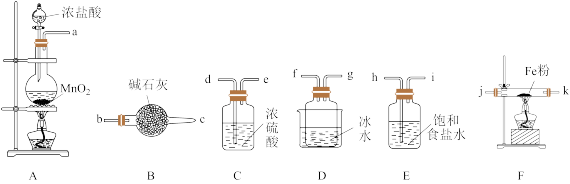
已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→_______ →j→k→_______ (按气流方向,用小写字母表示)。
(5)将所得无水FeCl3溶于_______ 可得FeCl3溶液,FeCl3溶液是一种常用的创伤止血剂,其止血原理为_______ 。
(6)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,第一种:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);第二种:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:_______ 。
②这两种反应平衡常数的大小关系为K1_______ K2(填“<”“>”或“=”)。
I.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如下装置制备FeCO3(夹持装置略)。

具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为
(2)写出整个实验过程中C中发生反应的离子方程式
(3)某实验小组用酸性高锰酸钾标准液去测定补血剂中乳酸亚铁含量,从而计算乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是
II.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。

已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→
(5)将所得无水FeCl3溶于
(6)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,第一种:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);第二种:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:
②这两种反应平衡常数的大小关系为K1
您最近一年使用:0次
5 . 二氧化碳催化加氢制甲醇,可减少CO2排放,并合成清洁能源。其反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
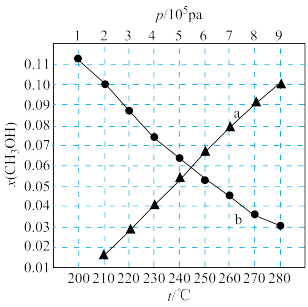
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
 CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
A.该反应的平衡常数表达式为K=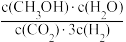 |
| B.图中对应等温过程的曲线是a |
| C.当χ(CH3OH)=0.10时,CO2的平衡转化率为33.3% |
| D.当χ(CH3OH)=0.10时,反应条件可能为2×105Pa、210℃或9×105Pa、280℃ |
您最近一年使用:0次
名校
6 . 为治理环境污染,工业上常用醋酸亚铜氨溶液来吸收含有大量N2的高炉气体系中的CO,从而实现CO和N2的分离,反应的化学方程式如下:CH3COOCu(NH3)2 (aq) + CO(g) 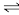 CH3COOCu(NH3)2·CO(aq) + Q(Q>0),
CH3COOCu(NH3)2·CO(aq) + Q(Q>0),
(1)该反应的化学平衡常数表达式K=_______ ;欲使K值变大,可采取的措施是_______ 。
(2)吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的适当处理措施有_______ (选填序号)。
a.适当升高温度 b.适当降低温度 c.增大压强 d.减小压强
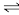 CH3COOCu(NH3)2·CO(aq) + Q(Q>0),
CH3COOCu(NH3)2·CO(aq) + Q(Q>0),(1)该反应的化学平衡常数表达式K=
(2)吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的适当处理措施有
a.适当升高温度 b.适当降低温度 c.增大压强 d.减小压强
您最近一年使用:0次
2022-10-18更新
|
147次组卷
|
3卷引用:湖南省株洲市第一中学2022-2023学年高二上学期期中考试化学试题
名校
7 . 用尿素水解生成的NH3催化还原 ,是柴油机车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g)
,是柴油机车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g) 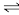 4N2(g)+6H2O(g),下列说法正确的是
4N2(g)+6H2O(g),下列说法正确的是
 ,是柴油机车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g)
,是柴油机车辆尾气净化的主要方法。反应为4NH3(g)+O2(g)+4NO(g) 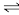 4N2(g)+6H2O(g),下列说法正确的是
4N2(g)+6H2O(g),下列说法正确的是| A.上述反应ΔS<0 |
B.上述反应平衡常数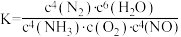 |
| C.上述反应中消耗2mol NH3,转移电子的数目为3×6.02×1023 |
| D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小 |
您最近一年使用:0次
名校
解题方法
8 . 在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g) CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是

 CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
| A.CO合成甲醇的反应为吸热反应 |
B.平衡常数K=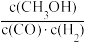 |
| C.该反应在T1时的平衡常数比T2时的小 |
D.处于A点的反应体系从T1变到T2,达到平衡时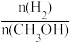 增大 增大 |
您最近一年使用:0次
2022-08-28更新
|
2153次组卷
|
29卷引用:湖南省长沙市明达中学2021-2022学年高二上学期期末考试化学试题
湖南省长沙市明达中学2021-2022学年高二上学期期末考试化学试题黑龙江省大庆市实验中学2021-2022学年高二下学期开学考试化学试题福建省龙岩第一中学2021-2022学年高二下学期开学考化学试题(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)第二节 化学平衡 第2课时 化学平衡常数福建省三明第一中学2022-2023学年高二上学期第一次月考化学试题陕西省宝鸡市千阳县中学2022-2023学年高二上学期第一次月考(理)化学试题吉林省九台龙成实验学校2022-2023学年高二上学期第一次月考化学试题【全国校级联考】全国大联考2019届高三入学调研考试卷(四)化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二上学期第一次月考(10月)化学试题(已下线)2018年11月浙江省普通高校招生选考科目考试化学仿真模拟试卷03(已下线)2019年1月浙江省普通高中学业水平考试化学仿真模拟试题03浙江省杭州市富阳区新登中学2018-2019学年高二上学期期末模拟化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(B)内蒙古北方重工业集团有限公司第三中学2019-2020学年高二10月月考化学试题江西省南昌市第十中学2020届高三上学期第一次月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题内蒙古翁牛特旗乌丹第一中学2019-2020学年高二10月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二10月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一次阶段考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2020-2021学年高二10月月考化学试题四川省宜宾翠屏棠湖学校2020-2021学年高二上学期10月月考化学试题山西省沁源县第一中学2020-2021学年高二下学期开学考试化学试题江西省新余市2022-2023学年高二上学期期末质量检测化学试题(已下线)第七章 化学反应速率与化学平衡 第43练 化学平衡移动原理及应用微项目 探讨如何利用工业废气中的二氧化碳合成甲醇四川省宜宾市兴文第二中学校2023-2024学年高二上学期10月月考化学试题【精品卷】2.2.2 化学平衡常数课堂例题-人教版2023-2024学年选择性必修1【定心卷】2.2.2 化学平衡常数随堂练习-人教版2023-2024学年选择性必修1
9 .  时,向
时,向 密闭容器中充入
密闭容器中充入 和
和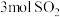 发生反应:
发生反应: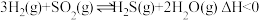 。部分物质的物质的量
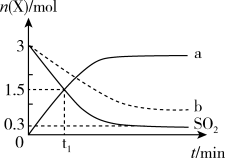
。部分物质的物质的量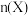 随时间t变化如图实线所示。下列说法正确的是
随时间t变化如图实线所示。下列说法正确的是
 时,向
时,向 密闭容器中充入
密闭容器中充入 和
和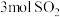 发生反应:
发生反应: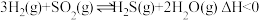 。部分物质的物质的量
。部分物质的物质的量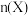 随时间t变化如图实线所示。下列说法正确的是
随时间t变化如图实线所示。下列说法正确的是
A.该反应的平衡常数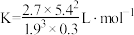 |
B. 时, 时, |
C.曲线a代表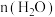 随时间变化的曲线 随时间变化的曲线 |
D.若该反应在 时进行,则虚线b可表示 时进行,则虚线b可表示 的变化 的变化 |
您最近一年使用:0次
2022-07-10更新
|
1413次组卷
|
11卷引用:湖南省株洲市茶陵县第一中学2022届高三下学期期中考试化学试题
湖南省株洲市茶陵县第一中学2022届高三下学期期中考试化学试题广东省深圳市2022届高三下学期第二次调研考化学试题(已下线)化学-2022年高考考前押题密卷(重庆卷)福建省漳平第一中学、永安一中 2022届高考前高三毕业班联考化学试题(已下线)2022年广东卷高考真题变式题(11-16)内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2022年北京高考真题变式题1-14安徽省舒城晓天中学2022-2023学年高二上学期期中考试化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)广东省潮州市2022-2023学年高三下学期第二次模拟考试化学试题
名校
解题方法
10 . 在160℃、200℃条件下,分别向两个容积为2L的刚性容器中充入2molCO和2mol ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是

 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是
A.ac段 的平均反应速率为 的平均反应速率为 |
| B.逆反应速率:c=d>b |
| C.160℃时,该反应的平衡常数K=9 |
| D.当容器中混合气体的密度不随时间变化时,该反应达到平衡状态 |
您最近一年使用:0次
2022-07-01更新
|
214次组卷
|
6卷引用:湖南省岳阳市2021-2022学年高二下学期期末教学质量监测化学试题



