1 . 用尿素水解生成的 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为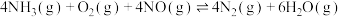 ,下列说法不正确的是
,下列说法不正确的是
 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为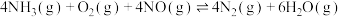 ,下列说法不正确的是
,下列说法不正确的是A.上述反应 |
B.上述反应平衡常数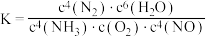 |
C.上述反应中消耗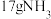 ,转移电子的数目为 ,转移电子的数目为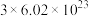 |
| D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气产生的污染越小 |
您最近一年使用:0次
2023-08-08更新
|
311次组卷
|
5卷引用:湖北省重点中学4G+联合体2022-2023学年高二上学期期中考试化学试题
名校
2 . 在一个容积不变的密闭容器中发生反应: ,其平衡常数(K)和温度(t)的关系如下表所示。下列说法不正确的是
,其平衡常数(K)和温度(t)的关系如下表所示。下列说法不正确的是
 ,其平衡常数(K)和温度(t)的关系如下表所示。下列说法不正确的是
,其平衡常数(K)和温度(t)的关系如下表所示。下列说法不正确的是| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
A.该反应的平衡常数表达式为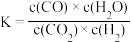 |
| B.该反应为吸热反应 |
C.在830℃时,向容器中充入1mol CO、 ,保持温度不变,反应达到平衡后, ,保持温度不变,反应达到平衡后, |
D.若1200℃时,在某时刻反应混合物中 、 、 、CO、 、CO、 的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时上述反应向正反应方向进行 的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时上述反应向正反应方向进行 |
您最近一年使用:0次
2023-07-24更新
|
205次组卷
|
3卷引用:湖北省黄冈市2022-2023学年高二上学期11月期中考试化学试题
3 .  可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:
反应①:

反应②: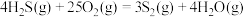
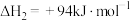
反应③: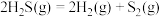

下列说法正确的是
 可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:反应①:


反应②:
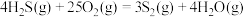
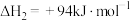
反应③:
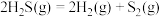

下列说法正确的是
| A.反应①可在任意温度下自发进行 |
B.反应②使用催化剂时 减小 减小 |
C.反应③的化学平衡常数表达式为 |
D.由上述反应可得 的 的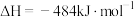 |
您最近一年使用:0次
4 . 在一定温度下,氯气溶于水的过程为:
①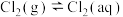 ;
;
②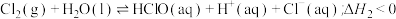 ,下列说法错误的是
,下列说法错误的是
①
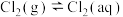 ;
;
②
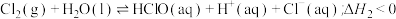 ,下列说法错误的是
,下列说法错误的是A. |
B.②的平衡常数表达式为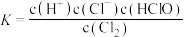 |
C.升高温度,氯水中的 减小 减小 |
D.取氯水稀释,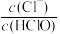 增大 增大 |
您最近一年使用:0次
名校
5 . 已知某化学反应的平衡常数表达式为K= ,其平衡常数K和温度的关系如表:
,其平衡常数K和温度的关系如表:
下列有关叙述错误的是
 ,其平衡常数K和温度的关系如表:
,其平衡常数K和温度的关系如表:| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A.该反应的化学方程式为CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) |
| B.上述反应的正反应是放热反应 |
| C.在一定容积的密闭容器中加入CO2和H2各1mol,温度升高到恒定值,5min后反应达到平衡,此时测得CO2的物质的量为0.4mol,则该温度为830℃ |
D.某温度下,若平衡浓度符合下列关系式: = = ,则此时的温度是1000℃ ,则此时的温度是1000℃ |
您最近一年使用:0次
2022-10-11更新
|
333次组卷
|
3卷引用:湖北省武汉市东湖中学2022-2023学年高二上学期期中考试化学试题
6 . 在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应I:
反应I:
反应III: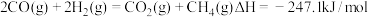
向恒容、密闭容器中通入 和
和 ,平衡时
,平衡时 、
、 、
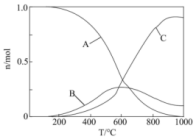
、 的物质的量随温度的变化如图所示。下列说法正确的是
的物质的量随温度的变化如图所示。下列说法正确的是
反应I:

反应I:

反应III:
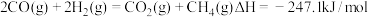
向恒容、密闭容器中通入
 和
和 ,平衡时
,平衡时 、
、 、
、 的物质的量随温度的变化如图所示。下列说法正确的是
的物质的量随温度的变化如图所示。下列说法正确的是
A.反应I的平衡常数可表示为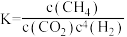 |
| B.图中曲线B表示CO的物质的量随温度的变化 |
C.提高 转化为 转化为 的转化率,需要研发在低温区高效的催化剂 的转化率,需要研发在低温区高效的催化剂 |
| D.混合气体密度保持不变,表示反应处于化学平衡状态。 |
您最近一年使用:0次
7 . 保护生态环境,实现可持续发展。试回答下列有关NO无害化处理的问题。
Ⅰ.在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g) + 2CO(g) 2CO2(g) + N2(g)。在某恒容密闭容器中,通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如下图所示:
2CO2(g) + N2(g)。在某恒容密闭容器中,通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如下图所示:

(1)该反应的平衡常数表达式为K=_______ ,由右图分析,该反应的正反应是_______ (填“放热”或“吸热”)反应。若要使K值增大,可采取的措施为_______ (填字母序号)。
a.增大c(NO) b.增加压强 c.降低温度 d.使用催化剂 e.升高温度
(2)温度为T1时,反应达到平衡时NO的转化率为_______ ,温度为T2时,从起始到建立平衡,υ(N2)=_______  。
。
Ⅱ.目前烟气脱硝采用的技术有无催化剂的选择性还原法(SNCR)和使用催化剂的选择性还原法(SCR)。若用NH3作还原剂,则主要反应均可表示为:4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(l) + Q (Q>0),其中体系温度对SNCR技术脱硝效率的影响如下图所示:
4N2(g) + 6H2O(l) + Q (Q>0),其中体系温度对SNCR技术脱硝效率的影响如下图所示:

(3)当有标准状况下的3.36L氧气参加反应时,被氧气氧化的NH3为_______ mol。
(4)①当体系温度过高时,SNCR技术脱硝效率会降低,其原因是_______ ;
②SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是_______ 。
Ⅰ.在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g) + 2CO(g)
 2CO2(g) + N2(g)。在某恒容密闭容器中,通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如下图所示:
2CO2(g) + N2(g)。在某恒容密闭容器中,通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如下图所示:
(1)该反应的平衡常数表达式为K=
a.增大c(NO) b.增加压强 c.降低温度 d.使用催化剂 e.升高温度
(2)温度为T1时,反应达到平衡时NO的转化率为
 。
。Ⅱ.目前烟气脱硝采用的技术有无催化剂的选择性还原法(SNCR)和使用催化剂的选择性还原法(SCR)。若用NH3作还原剂,则主要反应均可表示为:4NH3(g) + 4NO(g) + O2(g)
 4N2(g) + 6H2O(l) + Q (Q>0),其中体系温度对SNCR技术脱硝效率的影响如下图所示:
4N2(g) + 6H2O(l) + Q (Q>0),其中体系温度对SNCR技术脱硝效率的影响如下图所示:
(3)当有标准状况下的3.36L氧气参加反应时,被氧气氧化的NH3为
(4)①当体系温度过高时,SNCR技术脱硝效率会降低,其原因是
②SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是
您最近一年使用:0次
8 . Cu2+与NH3可结合生成多种络合物,在水溶液中存在如下平衡:[Cu(NH3)4]2+ [Cu(NH3)3]2+
[Cu(NH3)3]2+ [Cu(NH3)2]2+
[Cu(NH3)2]2+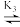 [Cu(NH3)]2+
[Cu(NH3)]2+ Cu2+。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的lgc(NH3)关系如图所示。下列说法正确的是
Cu2+。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的lgc(NH3)关系如图所示。下列说法正确的是

 [Cu(NH3)3]2+
[Cu(NH3)3]2+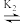 [Cu(NH3)2]2+
[Cu(NH3)2]2+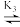 [Cu(NH3)]2+
[Cu(NH3)]2+ Cu2+。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的lgc(NH3)关系如图所示。下列说法正确的是
Cu2+。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的lgc(NH3)关系如图所示。下列说法正确的是
A. < < |
| B.曲线c表示[Cu(NH3)2]2+ |
| C.lgc(NH3)=-4时,c(Cu2+)>c([Cu(NH3)]2+)>c([Cu(NH3)2]2+) |
D.M点时,lgc(NH3)= |
您最近一年使用:0次
2022-03-03更新
|
1569次组卷
|
2卷引用:湖北省重点中学2021-2022学年高二下学期3月联考化学试题
解题方法
9 . 在恒容密闭容器中发生反应: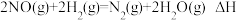 ,其反应速率与浓度关系式为
,其反应速率与浓度关系式为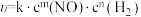 (k为常数,只与温度有关,m、n为反应级数,均为正整数),在某温度下测得有关数据如表所示:
(k为常数,只与温度有关,m、n为反应级数,均为正整数),在某温度下测得有关数据如表所示:
下列说法正确的是
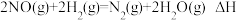 ,其反应速率与浓度关系式为
,其反应速率与浓度关系式为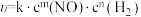 (k为常数,只与温度有关,m、n为反应级数,均为正整数),在某温度下测得有关数据如表所示:
(k为常数,只与温度有关,m、n为反应级数,均为正整数),在某温度下测得有关数据如表所示:| 序号 | 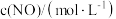 |  | 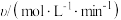 |
| ① | 0.05 | 0.20 | 0.207 |
| ② | 0.20 | 0.80 | 13.248 |
| ③ | 0.10 | 0.20 | 0.828 |
A.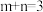 |
B.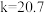 |
C.该反应的平衡常数表达式为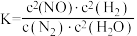 |
D.反应时,加入适宜的催化剂, 和k均变大 和k均变大 |
您最近一年使用:0次
2022-01-27更新
|
180次组卷
|
2卷引用:湖北省十堰市2021-2022学年高二上学期元月期末调研考试化学试题
10 . 碳及其化合物在工农业生产中有着广泛的应用。工业上用CH4与H2O、CO2重整生产H2,CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g) CO(g)+3H2(g),下列说法正确的是
CO(g)+3H2(g),下列说法正确的是
 CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g) CO(g)+3H2(g),下列说法正确的是
CO(g)+3H2(g),下列说法正确的是A.反应的平衡常数可表示为K= |
| B.1molCO和3molH2充分反应时放出的热量为161.1kJ |
| C.达平衡时缩小容器体积,正反应速率增大,逆反应速率减小 |
D.其他条件相同,增大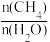 ,CH4的转化率下降 ,CH4的转化率下降 |
您最近一年使用:0次
2022-01-20更新
|
1045次组卷
|
9卷引用:湖北省宜城一中、枣阳一中等六校联考2022-2023学年高二上学期期中考试化学试题
湖北省宜城一中、枣阳一中等六校联考2022-2023学年高二上学期期中考试化学试题江苏省无锡市普通高中2021-2022学年上学期高三期末调研考试化学试题(已下线)一轮巩固卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)江西省上饶市铅山县第一中学2021-2022学年高二下学期开学考试化学试题 (已下线)押江苏卷第8题 化学反应速率与化学平衡、热化学 -备战2022年高考化学临考题号押题(江苏卷)江苏省南京市宁海中学2021-2022学年高二下学期期末考试化学试题广东省信宜市第二中学2021-2022高二下学期开学考试化学试题湖南省株洲市第一中学2022-2023学年高二上学期期末考试化学试题吉林省吉林市普通高中友好学校2022-2023学年高二上学期期末考试化学试题



