名校
1 . 硅是大数据时代的关键材料。工业上常在1800—2000℃时,用碳单质还原的方法制取单质硅。涉及反应的相关数据如表所示。下列相关说法正确的是
| 反应 | △H/(kJ•mol-1) | △S/(J•K-1•mol-1) |
| 反应(1):SiO2(s)+2C(s)=Si(s)+2CO(g) | 687.27 | 359.04 |
| 反应(2):SiO2(s)+C(s)=Si(s)+CO2(g) | 514.85 | 183.35 |
| A.反应(1)可证明Si的还原性大于C |
| B.生活中利用单晶硅良好的导光性能做光导纤维 |
| C.工业生产条件下反应(2)无法自发进行发生 |
| D.C(s)+CO2(g)=2CO(g) △H=-172.42kJ·mol-1 |
您最近一年使用:0次
2022-01-08更新
|
1344次组卷
|
6卷引用:吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题
吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题河南省郑州市2022届高三上学期第一次质量预测(1月)化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)
名校
解题方法
2 . 研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
A. 、 、 的反应在温度低时不能自发进行 的反应在温度低时不能自发进行 |
| B.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可以改变产生尾气的反应的方向 |
C.反应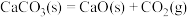 在室温下不能自发进行,说明该反应的 在室温下不能自发进行,说明该反应的 |
D.高温下, 反应能自发进行,则其 反应能自发进行,则其 、 、 |
您最近一年使用:0次
2021-12-21更新
|
352次组卷
|
14卷引用:吉林省长春市农安县五校联考2020-2021学年高二上学期期末考试化学试题
吉林省长春市农安县五校联考2020-2021学年高二上学期期末考试化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题选择性必修1(SJ)专题2第二单元课时1 化学反应的方向甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题(已下线)专题2 综合评价(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题湖南省常德市西洞庭管理区第一中学2022-2023学年高二上学期第二次月考化学试题2.2.1化学反应的方向 课后章末检测卷(二)化学反应的方向、限度与速率山西大学附属中学校2022-2023学年高二上学期11月期中考试化学试题海南省三亚第一中学2023-2024学年高二上学期第一次月考化学试题 福建省福清西山学校2023-2024学年高二上学期12月月考化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题
名校
3 . 物质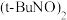 在正庚烷溶剂中发生如下反应:
在正庚烷溶剂中发生如下反应: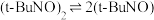 。
。
(1)当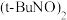 的起始浓度(c0)为
的起始浓度(c0)为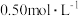 时,实验测得
时,实验测得 时的平衡转化率(
时的平衡转化率( )是65%,计算
)是65%,计算 时上述反应的平衡常数
时上述反应的平衡常数
___________ 。
(2)一定温度下,随着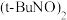 的起始浓度增大,其平衡转化率
的起始浓度增大,其平衡转化率___________ (填“增大”、“不变”或“减小”)。已知 时该反应在
时该反应在 溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成
溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成 ,并保持
,并保持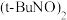 起始浓度相同,则它在
起始浓度相同,则它在 溶剂中的平衡转化率
溶剂中的平衡转化率___________ 。(填“大于”、“等于”或“小于”)其在正庚烷溶剂中的平衡转化率。
(3)该反应的
___________ 0(填“>”、“<”或“=”),实验测得该反应的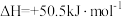 ,则在
,则在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
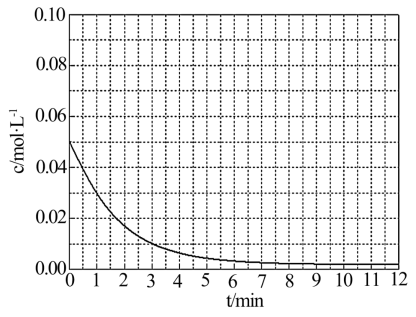
(4)通过比色分析得到 时
时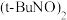 浓度随时间的变化关系如下图所示,请在同一图中绘出
浓度随时间的变化关系如下图所示,请在同一图中绘出 浓度随时间的变化曲线
浓度随时间的变化曲线________________ 。
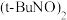 在正庚烷溶剂中发生如下反应:
在正庚烷溶剂中发生如下反应: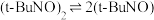 。
。(1)当
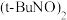 的起始浓度(c0)为
的起始浓度(c0)为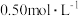 时,实验测得
时,实验测得 时的平衡转化率(
时的平衡转化率( )是65%,计算
)是65%,计算 时上述反应的平衡常数
时上述反应的平衡常数
(2)一定温度下,随着
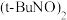 的起始浓度增大,其平衡转化率
的起始浓度增大,其平衡转化率 时该反应在
时该反应在 溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成
溶剂中的平衡常数为1.9,若将反应溶剂正庚烷改成 ,并保持
,并保持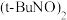 起始浓度相同,则它在
起始浓度相同,则它在 溶剂中的平衡转化率
溶剂中的平衡转化率(3)该反应的

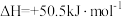 ,则在
,则在(4)通过比色分析得到
 时
时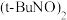 浓度随时间的变化关系如下图所示,请在同一图中绘出
浓度随时间的变化关系如下图所示,请在同一图中绘出 浓度随时间的变化曲线
浓度随时间的变化曲线
您最近一年使用:0次
名校
4 . 下列有关说法中正确的是
A.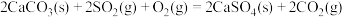 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
B. 室温下不能自发进行,说明该反应的 室温下不能自发进行,说明该反应的 |
| C.自发反应在任何条件下都能实现 |
D.冰融化为水的过程中: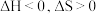 |
您最近一年使用:0次
5 . 回答下列问题
(1)对于反应C(s)+H2O(g)= CO(g)+ H2(g); △H=131.3kJ/mol ,当升高温度时,正反应速率___________ ,逆反应速率___________ ,混合气体密度___________ 作为判断达到平衡状态的标志。在其他条件不变的情况下, 达到平衡后如果增大压强,平衡向___________ 反应方向移动,反应的平衡常数___________ 变化。正反应的反应物的总能量___________ 生成物的总能量。[用 “变慢”“加快”“正”“逆”“能”“不能”“不发生”“发生” “大于”“小于”等填空]
(2)燃烧热是指101kPa时,___________ mol纯物质完全燃烧生成指定产物时所放出的热量。可燃物中的碳元素变为CO2(g),氢元素变为H2O(l),氮元素变为___________ ,硫元素变为SO2(g)
(3)如果一个可逆反应的正反应的焓变___________ 0,熵变___________ 0,则正反应的一定是自发的反应。
(1)对于反应C(s)+H2O(g)= CO(g)+ H2(g); △H=131.3kJ/mol ,当升高温度时,正反应速率
(2)燃烧热是指101kPa时,
(3)如果一个可逆反应的正反应的焓变
您最近一年使用:0次
6 . 已知:可逆反应2SO2(g) + O2(g)  2SO3(g) △H<0.现有甲、乙两个体积为VL的真空恒容密闭容器,向甲容器中加入2mol SO2(g) 和1mol O2(g) ,在一定条件下发生反应,达到平衡时放出热量为Q1kJ,且平衡时SO3的体积分数为a1.在相同条件下,向乙容器中加入2molSO3(g) 并发生反应,达到平衡时吸收热量为Q2kJ,若3Q1=5Q2.下列叙述中正确的是
2SO3(g) △H<0.现有甲、乙两个体积为VL的真空恒容密闭容器,向甲容器中加入2mol SO2(g) 和1mol O2(g) ,在一定条件下发生反应,达到平衡时放出热量为Q1kJ,且平衡时SO3的体积分数为a1.在相同条件下,向乙容器中加入2molSO3(g) 并发生反应,达到平衡时吸收热量为Q2kJ,若3Q1=5Q2.下列叙述中正确的是
 2SO3(g) △H<0.现有甲、乙两个体积为VL的真空恒容密闭容器,向甲容器中加入2mol SO2(g) 和1mol O2(g) ,在一定条件下发生反应,达到平衡时放出热量为Q1kJ,且平衡时SO3的体积分数为a1.在相同条件下,向乙容器中加入2molSO3(g) 并发生反应,达到平衡时吸收热量为Q2kJ,若3Q1=5Q2.下列叙述中正确的是
2SO3(g) △H<0.现有甲、乙两个体积为VL的真空恒容密闭容器,向甲容器中加入2mol SO2(g) 和1mol O2(g) ,在一定条件下发生反应,达到平衡时放出热量为Q1kJ,且平衡时SO3的体积分数为a1.在相同条件下,向乙容器中加入2molSO3(g) 并发生反应,达到平衡时吸收热量为Q2kJ,若3Q1=5Q2.下列叙述中正确的是| A.达平衡时甲、乙中SO2的体积分数:乙>甲 |
| B.达平衡时甲中SO2的转化率为60% |
C.乙中反应的热化学方程式为2SO3(g)  2SO2(g)+ O2(g) △H=+Q2kJ/mol 2SO2(g)+ O2(g) △H=+Q2kJ/mol |
| D.达到平衡后,再向甲中加入0.5molSO2(g) 、0.25molO2(g),再次平衡后,SO3的体积分数大于a1 |
您最近一年使用:0次
2021-11-07更新
|
716次组卷
|
2卷引用:吉林省长春市十一高中2021-2022学年高二上学期期中考试化学试题
7 . 在下列变化过程中,体系的熵减的是
| A.水凝结成冰 | B.蔗糖溶于水 |
| C.两种气体混合过程 | D.氯化铵固体分解成氯化氢气体和氨气 |
您最近一年使用:0次
8 . 下列过程的方向能用焓判据判断的是
| A.湿的衣服经过晾晒变干 |
| B.硝酸铵溶于水 |
| C.水蒸气凝结成水 |
D.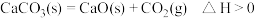 |
您最近一年使用:0次
2021-10-29更新
|
87次组卷
|
3卷引用:吉林省吉林市第五十五中学2021-2022学年高二上学期期中考试化学试题
解题方法
9 . 用CH4催化还原NOx可以消除氮氧化合物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH=-1160kJ/mol
下列说法中正确的是
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH=-1160kJ/mol
下列说法中正确的是
| A.等物质的量的CH4在反应①、②中转移电子数不同 |
| B.由反应①可推知:焓变影响是此反应能自发的唯一原因 |
| C.4NO2(g)+2N2(g)=8NO(g);ΔH=+586kJ/mol |
| D.若用4.48L CH4把NO2还原为N2,整个过程中转移的电子总数为1.6NA |
您最近一年使用:0次
名校
解题方法
10 . 下列关于判断过程方向的说法正确的是
| A.所有自发进行的化学反应都是放热反应 |
| B.由焓判据和熵判据组合而成的复合判据将更适合于判断所有的过程 |
| C.同一物质的固、液、气三种状态的熵值相同 |
D.反应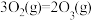 的 的 、 、 ,该反应在任何情况下均不能自发进行 ,该反应在任何情况下均不能自发进行 |
您最近一年使用:0次



