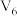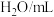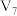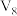名校
1 . 回答下列问题
(1)纯水在 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
___________ .
(2)若某溶液中只存在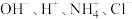 四种离子,且
四种离子,且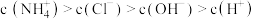 ,该溶液的溶质是
,该溶液的溶质是___________ .
(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
请完成此实验设计,其中
___________ ,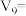
___________ .
(4)常温下,用 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中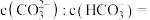
___________ [常温下,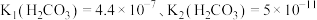 ].
].
(5)常温下,将 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在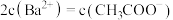 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
___________ (用含a和b的代数式表示)
(1)纯水在
 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
(2)若某溶液中只存在
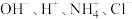 四种离子,且
四种离子,且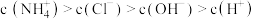 ,该溶液的溶质是
,该溶液的溶质是(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量
 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.混合溶液组成 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
|
|
| 10 | 0 |

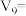
(4)常温下,用
 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中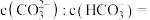
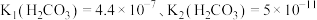 ].
].(5)常温下,将
 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在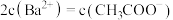 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
您最近一年使用:0次
名校
2 . 下列说法正确的是
A. 时, 时, 为9的 为9的 溶液和 溶液和 为5的 为5的 溶液中,水的电离程度不同 溶液中,水的电离程度不同 |
B.测定中和热实验中,用氨水代替 溶液做实验,所得反应热偏低 溶液做实验,所得反应热偏低 |
C. 时,等体积等物质的量浓度的 时,等体积等物质的量浓度的 和 和 溶液中所含离子总数前者大 溶液中所含离子总数前者大 |
D. 溶液与 溶液与 氨水等体积混合: 氨水等体积混合: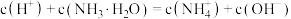 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作能够达到预期目的的是
A.用 试纸测定某浓度 试纸测定某浓度 溶液的 溶液的 为4 为4 |
B.加热 能得到纯净的无水氯化镁 能得到纯净的无水氯化镁 |
| C.增大压强,可以提高单位体积内活化分子的百分数,从而提高化学反应速率 |
D.中和 与体积均相同的 与体积均相同的 和氨水,消耗 和氨水,消耗 的量前者小于后者 的量前者小于后者 |
您最近一年使用:0次
名校
4 . NH4Al(SO4)2 常用食品加工中的食品添加剂,用于焙烤食品;NH4HSO4 在分析试剂、医药、电子工业中用途广泛;(NH4)2Fe(SO4)2∙6H2O(硫酸亚铁铵)是一种重要的化工原料用途广泛。请回答下列问题:
(1)NH4Al(SO4)2 可用作净水剂,其原理是___________ (用离子方程式说明)。
(2)相同条件下,0.1 mol∙L−1NH4Al(SO4)2 溶液中的 c( )
)______ (填“等于”“大于”或“小于”)0.1 mol∙L−1NH4HSO4 溶液中的 c( )。
)。
(3)几种均为 0.1 mol∙L−1 的电解质溶液的 pH 随温度变化的曲线如图所示。
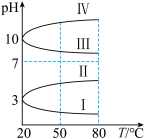
①其中符合 0.1 mol∙L−1NH4Al(SO4)2 溶液的 pH 随温度变化的曲线是_____ (填数字),导致NH4Al(SO4)2 溶液的 pH 随温度变化的原因是_______ 。
②20℃时,写出 0.1 mol∙L−1NH4Al(SO4)2 溶液中电荷守恒关系________ 。
(4)室温时,向 100mL0.1 mol∙L−1NH4HSO4 溶液中滴加 0.1 mol∙L−1NaOH 溶液,溶液 pH 与加入NaOH 溶液体积的关系曲线如图所示。

试分析图中 a、b、c、d 四个点,水的电离程度最大的是_____ 点。在 b 点,溶液中各离子浓度由大到小的排列顺序是______ 。
A. c(Na+)>c( )>c(
)>c( )>c(OH-)=c(H+) B. c(Na+)>c(
)>c(OH-)=c(H+) B. c(Na+)>c( )=c(
)=c( )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
C. c(Na+)>c( )>c(
)>c( )>c(OH-)>c(H+) D. c(
)>c(OH-)>c(H+) D. c( )>c(Na+)>c(
)>c(Na+)>c( )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
由 b 到 c 发生反应的离子方程式为______ 。
(5)将(NH4)2Fe(SO4)2 中非金属元素的简单负离子按半径由小到大的顺序排列:___________ 。铁原子核外有____ 种能量不同的电子,占有的轨道总数是______ 个。设计实验,证明(NH4)2Fe(SO4)2·6H2O 晶体中含有 Fe2+_______ 。
(6)已知:(NH4)2Fe(SO4)2·6H2O 在 200℃失去全部结晶水。将一定质量的粉末状该晶体置于坩埚中,保持 200℃受热,经冷却、恒重等正确操作,计算得到的 1mol 晶体中结晶水含量总是偏低,偏低的可能原因是_________ (写一条即可)。
(1)NH4Al(SO4)2 可用作净水剂,其原理是
(2)相同条件下,0.1 mol∙L−1NH4Al(SO4)2 溶液中的 c(
 )
) )。
)。(3)几种均为 0.1 mol∙L−1 的电解质溶液的 pH 随温度变化的曲线如图所示。

①其中符合 0.1 mol∙L−1NH4Al(SO4)2 溶液的 pH 随温度变化的曲线是
②20℃时,写出 0.1 mol∙L−1NH4Al(SO4)2 溶液中电荷守恒关系
(4)室温时,向 100mL0.1 mol∙L−1NH4HSO4 溶液中滴加 0.1 mol∙L−1NaOH 溶液,溶液 pH 与加入NaOH 溶液体积的关系曲线如图所示。

试分析图中 a、b、c、d 四个点,水的电离程度最大的是
A. c(Na+)>c(
 )>c(
)>c( )>c(OH-)=c(H+) B. c(Na+)>c(
)>c(OH-)=c(H+) B. c(Na+)>c( )=c(
)=c( )>c(OH-)=c(H+)
)>c(OH-)=c(H+)C. c(Na+)>c(
 )>c(
)>c( )>c(OH-)>c(H+) D. c(
)>c(OH-)>c(H+) D. c( )>c(Na+)>c(
)>c(Na+)>c( )>c(OH-)=c(H+)
)>c(OH-)=c(H+)由 b 到 c 发生反应的离子方程式为
(5)将(NH4)2Fe(SO4)2 中非金属元素的简单负离子按半径由小到大的顺序排列:
(6)已知:(NH4)2Fe(SO4)2·6H2O 在 200℃失去全部结晶水。将一定质量的粉末状该晶体置于坩埚中,保持 200℃受热,经冷却、恒重等正确操作,计算得到的 1mol 晶体中结晶水含量总是偏低,偏低的可能原因是
您最近一年使用:0次
名校
5 . 25℃时,向二元酸H2A溶液中滴加NaOH溶液,溶液的pH与pX的变化关系如图所示。pX表示-lg 或-lg
或-lg

下列选项正确的是
 或-lg
或-lg

下列选项正确的是
| A.Ka1为H2A的第一步电离常数,则-lgKa1=1.2 |
| B.pH=4.2时,c(A2-)>c(HA-) |
| C.pH=7时,c(Na+)>3c(A2-) |
| D.H2A与NaOH恰好完全反应生成正盐时,c(OH-)=c(HA-)+c(H2A)+c(H+) |
您最近一年使用:0次
2024-01-18更新
|
323次组卷
|
4卷引用:新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题
新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题黑龙江省牡丹江市第一中学2023-2024学年高三上学期 期末化学试卷(已下线)选择题11-14(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
6 . 化学有自己独特的语言,下列化学用语表达正确的是
A.NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++H++ |
| B.HS-的电离方程式:HS-⇌H++S2- |
| C.Na2S的水解方程式:S2-+2H2O⇌H2S+2OH- |
| D.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol |
您最近一年使用:0次
2024-01-18更新
|
67次组卷
|
2卷引用:四川省南充高级中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 已知在25℃时,醋酸、次氯酸、碳酸、亚硫酸和氢氰酸的电离平衡常数分别为
醋酸: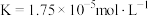
次氯酸: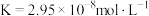
碳酸: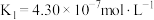 ;
;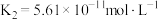
亚硫酸: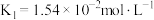 ;
;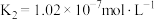
氢氰酸: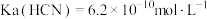
(1)写出碳酸的第一级电离平衡常数表达式:
_______ 。
(2)在相同条件下,等浓度的 、
、 、
、 和
和 溶液中碱性最强的是
溶液中碱性最强的是_______ 。
 溶液中各离子浓度大小顺序为
溶液中各离子浓度大小顺序为_______ 。
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是_________ 。
a.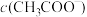 b.
b.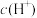 c.醋酸的电离平衡常数
c.醋酸的电离平衡常数
(4)下列离子方程式中错误的是___________ 。
a.少量 通入次氯酸钠溶液中:
通入次氯酸钠溶液中: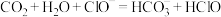
b.少量 通入次氯酸钙溶液中:
通入次氯酸钙溶液中: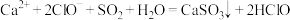
c.过量 通入澄清石灰水中:
通入澄清石灰水中:
(5)等物质的量浓度的NaCN和HCN的混合溶液中粒子浓度大小顺序_______ 。
醋酸:
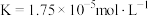
次氯酸:
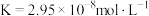
碳酸:
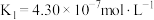 ;
;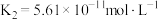
亚硫酸:
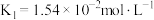 ;
;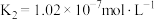
氢氰酸:
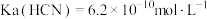
(1)写出碳酸的第一级电离平衡常数表达式:

(2)在相同条件下,等浓度的
 、
、 、
、 和
和 溶液中碱性最强的是
溶液中碱性最强的是
 溶液中各离子浓度大小顺序为
溶液中各离子浓度大小顺序为(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是
a.
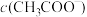 b.
b.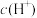 c.醋酸的电离平衡常数
c.醋酸的电离平衡常数(4)下列离子方程式中错误的是
a.少量
 通入次氯酸钠溶液中:
通入次氯酸钠溶液中: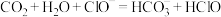
b.少量
 通入次氯酸钙溶液中:
通入次氯酸钙溶液中: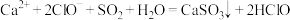
c.过量
 通入澄清石灰水中:
通入澄清石灰水中:
(5)等物质的量浓度的NaCN和HCN的混合溶液中粒子浓度大小顺序
您最近一年使用:0次
名校
8 . 下列溶液中各微粒的浓度关系正确的是
A.pH相等的① ② ②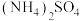 ③ ③ 溶液, 溶液,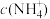 大小顺序为① 大小顺序为① ② ② ③ ③ |
B.pH相等的NaF与 溶液: 溶液: |
C. 的 的 溶液: 溶液: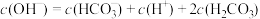 |
D. HCl与 HCl与  溶液等体积混合: 溶液等体积混合: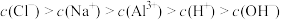 |
您最近一年使用:0次
名校
解题方法
9 . 把
 溶液和
溶液和 NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是
NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是

 溶液和
溶液和 NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是
NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是A. |
B. |
C. |
D. |
您最近一年使用:0次
名校
10 . 下列哪组离子能在水溶液中大量共存
A. 、 、 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次

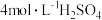 溶液/
溶液/




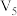
 溶液/
溶液/