1 . 下表为元素周期表的一部分,其中的编号代表对应的元素。
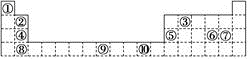
请回答下列问题:
(1)表中属于ds区的元素是________ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状物结构简式为________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子数为________ 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______________________ 。
(5)画出⑨的外围电子排布图____________________________ .

请回答下列问题:
(1)表中属于ds区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状物结构简式为
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子数为
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
(5)画出⑨的外围电子排布图
您最近一年使用:0次
2 . 下面是元素周期表的一部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)___________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:__________ 。
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:_____________ 。
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为____________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
名校
3 . 下表为元素周期表的一部分请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)⑧、⑩的最高价含氧酸的酸性由强到弱的顺序是__________________ 。③的最高价氧化物为__________ ;⑨的最高价含氧酸是__________ (均填化学式)
(2)④、⑤、⑥的形成的简单离子半径的大小顺序___________ 。(用离子符号表示)⑤与水反应的离子方程式___________ 。
(3)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:__________ 。
(4)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度_______ (选填“更大”“更小”或“相同”)。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| ⑩ |
(1)⑧、⑩的最高价含氧酸的酸性由强到弱的顺序是
(2)④、⑤、⑥的形成的简单离子半径的大小顺序
(3)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:
(4)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度
您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分, 回答下列问题:
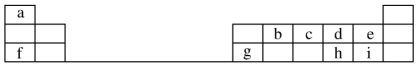
(1)元素e的负一价离子的结构示意图为____________ , e、f、g、h、i对应简单离子的半径由大到小的顺序为______________ (用具体微粒符号表示)。
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为_____ 。
(3)以元素b的最简气态氢化物为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式________________________________ 。

(1)元素e的负一价离子的结构示意图为
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为
(3)以元素b的最简气态氢化物为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式
您最近一年使用:0次
9-10高一下·吉林·期中
5 . (1)在短周期元素中:
①金属性最强的元素是______ ,与水反应最剧烈的非金属是_____ ;
②地壳中含量最丰富的元素位于第________ 周期第________ 族,地壳中含量最多的金属元素位于周期表的第________ 周期第________ 族.
(2)在11~18号的元素中:
③原子半径最小的元素是________ ;
④元素最高价氧化物中既能与盐酸反应又能与烧碱反应,该氧化物是________ .
①金属性最强的元素是
②地壳中含量最丰富的元素位于第
(2)在11~18号的元素中:
③原子半径最小的元素是
④元素最高价氧化物中既能与盐酸反应又能与烧碱反应,该氧化物是
您最近一年使用:0次
9-10高二下·吉林·期中
6 . A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: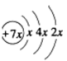 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A_________ B__________ C __________ D __________
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是__________ ,碱性最强的是_________ 。
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是__________ ,电负性最大的元素是__________ 。
(4)D的氢化物比C的氢化物的沸点__________ (填"高"或"低"),原因_____________
(5)E元素原子的核电荷数是__________ ,E元素在周期表的第_______ 周期,第________ 族,已知元素周期表可按电子排布分为s区、p区等,则E元素在_______ 区。
(6)A、B、C最高价氧化物的晶体类型是分别是______ 晶体、______ 晶体、_____ 晶体。
(7)画出D的核外电子排布图_____________________ ,这样排布遵循了_______ 规则。
(8)用电子式表示B的硫化物的形成过程:______________________________________
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
(8)用电子式表示B的硫化物的形成过程:
您最近一年使用:0次
10-11高一下·江西吉安·期中
7 . (1)X元素的原子核外有2个电子层,其中L层有5个电子,该元素在周期表中的位置是_________________________ ,最高价氧化物的化学式为___________ ,该元素的氢化物和最高价氧化物对应的水化物反应的化学方程式为_____________________________ 。
(2)Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO3,则此时Y元素的化合价为____________ ,Y原子的最外层电子数为_________ ,其气态氢化物的化学式为____________ 。
(2)Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO3,则此时Y元素的化合价为
您最近一年使用:0次
2011-05-09更新
|
1124次组卷
|
5卷引用:2016-2017学年吉林省汪清县第六中学高一3月月考化学试卷
2016-2017学年吉林省汪清县第六中学高一3月月考化学试卷(已下线)2010-2011学年江西省安福中学高一下学期期中考试化学试卷(已下线)同步君 必修2 第1章 第2节 元素周期表和元素周期律的应用高中化学人教版 必修2 第一章 物质结构 元素周期律 第二节 元素周期律 元素周期表和元素周期律的应用(已下线)4.2.2 元素周期表和元素周期律的应用练习(1)——《高中新教材同步备课》(人教版 必修第一册)



