名校
1 . 人们运用元素周期律和元素周期表,可以系统研究元素的性质。试回答:
(1)碱金属元素中,锂原子的结构示意图为_______ ,其中6Li、7Li互为_______ ;
(2)金属钾19K位于元素周期表中的第_______ 周期第_______ 族,钾的氧化物有多种,其中过氧化钾(K2O2)和超氧化钾(KO2)常作供氧剂,写出过氧化钾与CO2反应的化学方程式:_______ ;
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为_______ 、可作半导体材料的元素是_______ (填名称),已知H2+Cl2 2HCl,请用电子式表达HCl的形成过程
2HCl,请用电子式表达HCl的形成过程_______ 。
(1)碱金属元素中,锂原子的结构示意图为
(2)金属钾19K位于元素周期表中的第
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为
 2HCl,请用电子式表达HCl的形成过程
2HCl,请用电子式表达HCl的形成过程
您最近一年使用:0次
2 . “天宫二号”使用的冷原子钟突破人类太空计时精度,三千万年误差小于1秒,攻克了冷原子钟超低噪声微波频率源等关键技术,制作该钟用到了铷。图甲为元素周期表的部分信息,图乙为铷原子的结构示意图。
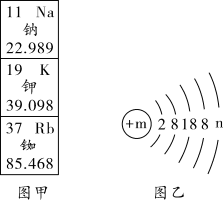
(1)钾的相对原子质量为___ 、质子数为__ 。
(2)乙图中m和n的数值分别为___ 、___ 。
(3)写出11号元素所形成离子的离子符号___ 。

(1)钾的相对原子质量为
(2)乙图中m和n的数值分别为
(3)写出11号元素所形成离子的离子符号
您最近一年使用:0次
名校
3 . 已知A、B两种元素,A的原子序数为x,A和B所在周期的元素种类数目分别为m和n。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为___________ ,当B在A的下一周期时,B的原子序数为___________ ;
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ ;当B在A的下一周期时,B的原子序数为___________ 。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次
2021-09-02更新
|
662次组卷
|
4卷引用:海南省琼海市嘉积中学2023-2024学年高一上学期期末考试化学试题B卷
海南省琼海市嘉积中学2023-2024学年高一上学期期末考试化学试题B卷云南省曲靖市罗平县第二中学2019-2020学年高一下学期期中考试化学试题(已下线)4.1.2 元素周期表 核素-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)5.1.2 元素周期表(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)
名校
解题方法
4 . 表是元素周期表的一部分。
请回答:
(1)世界上第一张元素周期表的作者是_______ (填序号);
a.阿伏加德罗 b.门捷列夫 c.居里夫人
(2)从表中查出第2周期第ⅠA族的元素是_______ ;
(3)上表列出的元素中,非金属性最强的是_______ ;
(4)某同学探究元素性质递变规律与原子结构的关系,进行了如下实验:
【实验操作】取已除去氧化膜且面积相等的镁条和铝条,分别投入2ml 1mol/L的盐酸中;
【实验现象】镁比铝与酸反应更剧烈;
【实验结论】①金属性:Mg_______ Al(选填“>”或“<”)
【查阅资料】原子半径(nm)Mg-0.160 Al-0.143;
【思考】②利用元素周期律对上述实验结论进行解释_______ 。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | Li | Be | B | C | N | O | F | Ne |
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar |
请回答:
(1)世界上第一张元素周期表的作者是
a.阿伏加德罗 b.门捷列夫 c.居里夫人
(2)从表中查出第2周期第ⅠA族的元素是
(3)上表列出的元素中,非金属性最强的是
(4)某同学探究元素性质递变规律与原子结构的关系,进行了如下实验:
【实验操作】取已除去氧化膜且面积相等的镁条和铝条,分别投入2ml 1mol/L的盐酸中;
【实验现象】镁比铝与酸反应更剧烈;
【实验结论】①金属性:Mg
【查阅资料】原子半径(nm)Mg-0.160 Al-0.143;
【思考】②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
名校
5 . 下表为元素周期表的一部分。
(1)表中元素_______ 的非金属性最强;元素_______ 的金属性最强; (写元素符号)。
(2)表中半径最大的元素是_______ ;(写元素符号)
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是_______ ;(写化学式,下同)
(4)表中元素⑥、⑦氢化物的稳定性顺序为_______ ;
(5)表中元素最高价氧化物对应水化物酸性最强的酸是_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ⑤ | |||||
| 三 | ③ | ⑥ | |||||
| 四 | ④ | ⑦ | |||||
(1)表中元素
(2)表中半径最大的元素是
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是
(4)表中元素⑥、⑦氢化物的稳定性顺序为
(5)表中元素最高价氧化物对应水化物酸性最强的酸是
您最近一年使用:0次
6 . 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
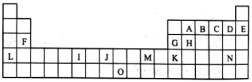
试回答下列问题:
(1)I的元素符号为______ ,在周期表中位于______ 区。
(2)写出A原子的核外电子排布的轨道表示式:______ ;写出J元素基态原子的价层电子排布式:______ ,J在周期表中的位置是______ 。
(3)A、B、G、H的非金属性顺序是______ 。(用元素符号表示)

试回答下列问题:
(1)I的元素符号为
(2)写出A原子的核外电子排布的轨道表示式:
(3)A、B、G、H的非金属性顺序是
您最近一年使用:0次
2021-02-22更新
|
404次组卷
|
2卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高二下学期3月月考化学试jgh同
7 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)写出②元素是_______ ,⑤元素是 _______ (填元素符号);
(2)③、④可形成的化合物的化学式_______ ;
(3)非金属性最强的是_______ (填元素符号);
(4)②和③的原子半径大小关系是②_______ ③(填“>”“<”或“=”);
(5)⑤和⑥的最高价氧化物对应的水化物的酸性较强的是_______ (填酸的化学式)。

(1)写出②元素是
(2)③、④可形成的化合物的化学式
(3)非金属性最强的是
(4)②和③的原子半径大小关系是②
(5)⑤和⑥的最高价氧化物对应的水化物的酸性较强的是
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分,请回答下列问题:
(1)写出下列元素符号:⑤________ ,⑥________ 。
(2)在这些元素中(表中①~⑧),最活泼的金属元素是__________ (填元素符号,下同),最活泼的非金属元素是______ ,最不活泼的元素是________ 。
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是________ (填化学式),碱性最强的是________ (填化学式),原子半径最小的是________ (填元素符号)。
(4)在③与④中,化学性质较活泼的是________ (填元素符号),怎样用化学实验证明?
(简述方法即可)___________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)写出下列元素符号:⑤
(2)在这些元素中(表中①~⑧),最活泼的金属元素是
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是
(4)在③与④中,化学性质较活泼的是
(简述方法即可)
您最近一年使用:0次
9 . 下表为元素周期表中的一部分,回答下列问题。
(1)这10种元素中,非金属性最强的是___ (填元素符号)。
(2)这10种元素中,最高价氧化物对应的水化物中碱性最强的是___ (填化学式)。.
(3)①、③两种元素按原子个数比1:4形成的化合物的结构式为___ 。
(4)元素④的最高价氧化物对应的水化物与元素⑩的简单氢化物反应的离子方程式为___ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ | ⑨ | ⑩ |
(1)这10种元素中,非金属性最强的是
(2)这10种元素中,最高价氧化物对应的水化物中碱性最强的是
(3)①、③两种元素按原子个数比1:4形成的化合物的结构式为
(4)元素④的最高价氧化物对应的水化物与元素⑩的简单氢化物反应的离子方程式为
您最近一年使用:0次
10 . 海水约占地球总储水量的97%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量氯化钠,氯化钠的电子式为_____ ,氯化钠中的非金属元素在元素周期表中的位置为第________ 周期第________ 族。
(2)目前,国际上广泛应用的海水淡化的主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得到高纯度淡水,由此可判断蒸馏的过程中发生的是________ (填“物理变化”或“化学变化”)。
(3)工业上从海水中提取溴,第一步是将氯气通入富含溴离子的海水中,将溴置换出来;第二步用空气把溴吹出,用SO2的水溶液吸收,使溴转化为氢溴酸;第三步用氯气氧化氢溴酸即得单质溴。写出上述过程中第一、二步发生反应的离子方程式:①______ ;②______ 。
(1)海水中含有大量氯化钠,氯化钠的电子式为
(2)目前,国际上广泛应用的海水淡化的主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得到高纯度淡水,由此可判断蒸馏的过程中发生的是
(3)工业上从海水中提取溴,第一步是将氯气通入富含溴离子的海水中,将溴置换出来;第二步用空气把溴吹出,用SO2的水溶液吸收,使溴转化为氢溴酸;第三步用氯气氧化氢溴酸即得单质溴。写出上述过程中第一、二步发生反应的离子方程式:①
您最近一年使用:0次



