名校
解题方法
1 . 下列粒子的VSEPR模型与其空间结构不一致的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-03-28更新
|
57次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高二下学期3月月考化学试题
2 . 物质的结构决定其性质。下列实例与解释不相符的是
选项 | 实例 | 解释 |
A | 不存在稳定的H3、H2Cl和Cl3 | 共价键具有饱和性 |
B | 分子的极性:BF3<NF3 | F-N键的极性小于F-B键的极性 |
C | 冠醚12-冠-4能够与Li+形成超分子,而不能与K+形成超分子 | 该冠醚空腔的直径与Li+的直径相当,与K+的直径不匹配 |
D | 沸点:N2低于CO | 二者分子量相同,但分子的极性不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-27更新
|
299次组卷
|
2卷引用:2024届河北省张家口市高三下学期一模化学试题
名校
解题方法
3 . 下列化学用语使用正确的是
A.乙烯的碳碳 键的电子云形状为: 键的电子云形状为: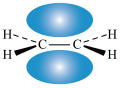 |
B. 分子的VSEPR模型: 分子的VSEPR模型: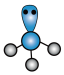 |
C. 的电子式为: 的电子式为: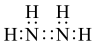 |
D.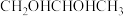 的名称为:丙二醇 的名称为:丙二醇 |
您最近一年使用:0次
解题方法
4 . 氟元素可形成多种有工业价值和科研价值的化合物,如OF2、NF3、XeF2等。其中XeF2的四方晶胞结构如图所示,图中M点原子坐标参数为( ,
, ,
, ),Xe和F的最短距离为bnm、下列说法错误的是
),Xe和F的最短距离为bnm、下列说法错误的是

 ,
, ,
, ),Xe和F的最短距离为bnm、下列说法错误的是
),Xe和F的最短距离为bnm、下列说法错误的是
A. OF2分子中键角小于 分子中的 分子中的 |
B. 中Xe的杂化方式为sp 中Xe的杂化方式为sp |
| C.基态N、F原子核外电子均有5种空间运动状态 |
D.Q点原子坐标参数为 [ ] ] |
您最近一年使用:0次
2023-05-20更新
|
223次组卷
|
3卷引用:河北省张家口市2023届高三高考三模化学试题
名校
解题方法
5 . 三卤化氮( )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:
(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式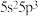 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是___________ 。基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是___________ ,原子半径由大到小的顺序是___________ 。
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为___________ 。液晶在放电过程中会产生 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是___________ ,键角:
___________  (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。
(4)已知热稳定性 高于
高于 ,解释其原因是
,解释其原因是___________ 。常温常压下 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为___________ , 和
和 的分子空间构型均为
的分子空间构型均为___________ 。
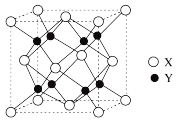
(5) 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是___________ ;若该立方晶胞参数为apm, 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度=___________  (写出表达式)。
(写出表达式)。
 )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式
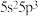 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为
 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是
 (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。(4)已知热稳定性
 高于
高于 ,解释其原因是
,解释其原因是 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为 和
和 的分子空间构型均为
的分子空间构型均为(5)
 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度= (写出表达式)。
(写出表达式)。
您最近一年使用:0次
2023-05-14更新
|
93次组卷
|
3卷引用:河北省尚义县第一中学2022-2023学年高二下学期第三次阶段测试化学试题
名校
解题方法
6 . 下列图示不正确 的是
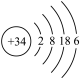 |  |  | 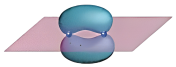 |
| A.Se的原子结构示意图 | B. 的VSEPR模型 的VSEPR模型 | C.基态 的价层电子的轨道表示式 的价层电子的轨道表示式 | D. 键的电子云轮廓图 键的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-07更新
|
413次组卷
|
2卷引用:河北省张家口市张北县第一中学2022-2023学年高二下学期4月月考化学试题
名校
解题方法
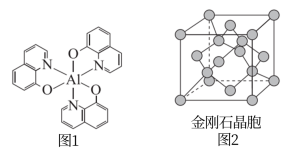
7 . 光电材料在能源军事等领域有重要应用,分为无机光电材料如ZnS、ZnSe、GaAs、 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:
(1)基态Zn原子的价层电子排布图为_____ ;Ga、As、Se的第一电离能由大到小的顺序为___________ 。
(2)图1所示化合物中所含有的化学键类型有_____ (填选项字母),N原子的杂化方式为_____ 。
A.共价键 B.离子键 C.配位键 D.氢键
(3)在水溶液中,以 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:
①表中氧化物之间沸点差异的原因为___________ 。
② 的VSEPR模型为
的VSEPR模型为___________ 。
③ 和
和 分子中,键角更大的是
分子中,键角更大的是___________ 。
(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为___________ 。
②若阿伏加德罗常数的值为 ,ZnS晶体的密度为
,ZnS晶体的密度为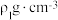 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为___________ 。
 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:(1)基态Zn原子的价层电子排布图为
(2)图1所示化合物中所含有的化学键类型有
A.共价键 B.离子键 C.配位键 D.氢键

(3)在水溶液中,以
 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:| 氧化物 |  |  |  |
| 沸点/℃ | 100 | -10 | -78.5 |
②
 的VSEPR模型为
的VSEPR模型为③
 和
和 分子中,键角更大的是
分子中,键角更大的是(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为
②若阿伏加德罗常数的值为
 ,ZnS晶体的密度为
,ZnS晶体的密度为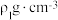 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
您最近一年使用:0次
2022-03-23更新
|
295次组卷
|
2卷引用:河北省张家口市2022届高三第一次模拟考试化学试题
解题方法
8 . 2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,回答下列问题。

(1)基态P原子中,电子占据的最高能级符号为___ 。
(2)磷酸氯喹中N-H键是___ σ键,NH3易液化,其原因是___ 。
(3)PO 的空间构型是
的空间构型是___ ,与PO 互为等电子体的分子是
互为等电子体的分子是___ (写一种即可)。
(4)磷化镓是人工合成的III-V族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被Ga原子代替,顶点和面心的碳原子被P原子代替。
①磷化镓晶体中含有的化学键类型为___ (填选项字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键F.非极性键
②设磷化镓的晶体密度为ag·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为___ pm(用代数式表示)。

(1)基态P原子中,电子占据的最高能级符号为
(2)磷酸氯喹中N-H键是
(3)PO
 的空间构型是
的空间构型是 互为等电子体的分子是
互为等电子体的分子是(4)磷化镓是人工合成的III-V族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被Ga原子代替,顶点和面心的碳原子被P原子代替。
①磷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键F.非极性键
②设磷化镓的晶体密度为ag·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为
您最近一年使用:0次
名校
解题方法
9 . 下列物质中,分子的立体结构与水分子相似的是 ( )
| A.CO2 | B.H2S | C.PCl3 | D.SiCl4 |
您最近一年使用:0次
2020-05-23更新
|
730次组卷
|
11卷引用:2016-2017学年河北省张家口一中高二12月月考化学卷
2016-2017学年河北省张家口一中高二12月月考化学卷广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构(人教版2019)选择性必修2 第二章 分子结构与性质 章末综合检测卷(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构(已下线)2.2.1 分子空间结构的理论分析-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)宁夏海原第一中学2020-2021学年高二下学期期末考试化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题
名校
解题方法
10 . 已知:A、B、C、D、E五种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E的原子序数比D大3。试回答下列有关的问题:
(1)写出D元素价电子的电子排布图:______________ 。
(2)D可形成化合物[D(H2O)6](NO3)3 ,[D(H2O)6](NO3)3中阴离子的立体构型是____________ 。NO2-中心原子的轨道杂化类型为______________ ,1 mol [D(H2O)6] 3+ 中含有的σ键数为 ______________ 。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中___________ (填化学式)为非极性分子。另一种物质的电子式为 ______________ 。
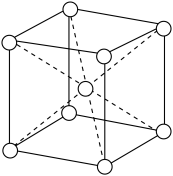
(4)D是一种硬而脆抗腐蚀性强的金属,常用于电镀和制造特种钢。下图为D的晶胞结构图,则D晶胞属于___________ 堆积;该晶胞中原子的体积占晶胞体积的百分率为___________ 。(已知:π=3.14, =1.732)
=1.732)
(5)E晶体的一种晶胞(如图所示)的边长为anm,密度为ρg·cm-3,NA表示阿伏伽德罗常数的值,则E的原子半径为___________ nm,E的相对原子质量可表示为___________ 。
(1)写出D元素价电子的电子排布图:
(2)D可形成化合物[D(H2O)6](NO3)3 ,[D(H2O)6](NO3)3中阴离子的立体构型是
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中
(4)D是一种硬而脆抗腐蚀性强的金属,常用于电镀和制造特种钢。下图为D的晶胞结构图,则D晶胞属于
 =1.732)
=1.732)
(5)E晶体的一种晶胞(如图所示)的边长为anm,密度为ρg·cm-3,NA表示阿伏伽德罗常数的值,则E的原子半径为
您最近一年使用:0次
2019-03-06更新
|
277次组卷
|
3卷引用:河北省张家口市宣化区第一中学2020届高三下学期3月月考化学试题



