名校
1 . 下列说法正确的是
| A.键角:Cl2O>OF2 | B.酸性:CH3COOH>CH2FCOOH |
| C.分子的极性:O2>O3 | D.基态原子未成对电子数:Mn>Cr |
您最近一年使用:0次
名校
2 . 某次研究性学习活动中,实验小组用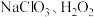 和稀硫酸制备
和稀硫酸制备 ,反应较慢。若反应开始时加入少量盐酸,
,反应较慢。若反应开始时加入少量盐酸, 的生成速率大大提高,且不含
的生成速率大大提高,且不含 ,可能的反应历程示意图如下。
,可能的反应历程示意图如下。

下列有关分析或评价不正确的是
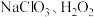 和稀硫酸制备
和稀硫酸制备 ,反应较慢。若反应开始时加入少量盐酸,
,反应较慢。若反应开始时加入少量盐酸, 的生成速率大大提高,且不含
的生成速率大大提高,且不含 ,可能的反应历程示意图如下。
,可能的反应历程示意图如下。
下列有关分析或评价不正确的是
| A.a等于37 | B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 为总反应的催化剂 为总反应的催化剂 | D.活化能:反应I大于反应II |
您最近一年使用:0次
2024-01-29更新
|
384次组卷
|
3卷引用: 河南省洛阳市孟津区第一高级中学2023-2024学年高三上学期12月月考化学试题
河南省洛阳市孟津区第一高级中学2023-2024学年高三上学期12月月考化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河南省新乡市第一中学2023-2024学年高三上学期12月月考化学试题
2024·黑龙江·模拟预测
解题方法
3 . CO2资源化利用受到越来越多的关注,它能有效减少碳排放,有效应对全球的气候变化,并且能充分利用碳资源。二氧化碳催化加氢制甲醇有利于减少温室气体排放,涉及的反应如下:
I.


II.
 kJ⋅mol-1
kJ⋅mol-1 
III.
 kJ⋅mol-1
kJ⋅mol-1 
回答下列问题:
(1)CO2分子的空间结构为___________ 形。
(2)
___________ kJ⋅mol-1。
(3)平衡常数
___________ (用 、
、 表示)。
表示)。
(4)为提高反应Ⅲ中 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。
(5)不同压强下,按照 投料,发生反应I,实验测得
投料,发生反应I,实验测得 的平衡转化率随温度的变化关系如下图所示。
的平衡转化率随温度的变化关系如下图所示。 、
、 由大到小的顺序为
由大到小的顺序为___________ ,判断的依据是___________ 。
②图中A点对应的甲醇的体积分数是___________ %(计算结果保留1位小数)。
(6)在恒温恒压(压强为p)的某密闭容器中,充入1mol 和3mol
和3mol ,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得
,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[
的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[ ]},则该温度下反应I的平衡常数
]},则该温度下反应I的平衡常数
___________ (写出计算式即可,分压=总压×物质的量分数)。
I.



II.

 kJ⋅mol-1
kJ⋅mol-1 
III.

 kJ⋅mol-1
kJ⋅mol-1 
回答下列问题:
(1)CO2分子的空间结构为
(2)

(3)平衡常数

 、
、 表示)。
表示)。(4)为提高反应Ⅲ中
 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
 投料,发生反应I,实验测得
投料,发生反应I,实验测得 的平衡转化率随温度的变化关系如下图所示。
的平衡转化率随温度的变化关系如下图所示。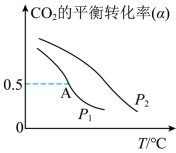
 、
、 由大到小的顺序为
由大到小的顺序为②图中A点对应的甲醇的体积分数是
(6)在恒温恒压(压强为p)的某密闭容器中,充入1mol
 和3mol
和3mol ,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得
,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[
的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[ ]},则该温度下反应I的平衡常数
]},则该温度下反应I的平衡常数
您最近一年使用:0次
2024·吉林·模拟预测
解题方法
4 . 下列化学用语表述正确的是
A. 的空间结构为V形 的空间结构为V形 | B.顺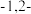 二溴乙烯结构式为 二溴乙烯结构式为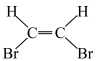 |
C. 的电子式为 的电子式为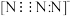 | D.基态 原子价电子排布式为 原子价电子排布式为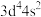 |
您最近一年使用:0次
23-24高三上·福建莆田·阶段练习
名校
5 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式________ , 空间构型为
空间构型为________
(2)提高“酸浸”速率的方法有_________ 。(任写一条)
(3)“滤渣1”的主要成分是_________ 。(写化学式)
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F- )最小为______ mol·L-1(已知离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全,Ksp(CaF2)=1.0 ×10-10,Ksp(MgF2)=7.5×10-11)。
(6)获得NiSO4(s)的“一系列操作”是________ 。
(7)工艺流程中,可循环利用的物质是___________ 。
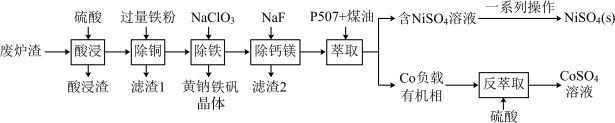
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式
 空间构型为
空间构型为(2)提高“酸浸”速率的方法有
(3)“滤渣1”的主要成分是
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(6)获得NiSO4(s)的“一系列操作”是
(7)工艺流程中,可循环利用的物质是
您最近一年使用:0次
2023·浙江绍兴·一模
名校
6 . 下列化学用语表示正确的是
A.C2H6的空间填充模型: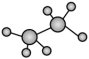 | B.SO2的价层电子对互斥模型: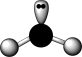 |
C.HCl的电子式: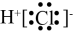 | D.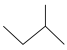 的名称:3-甲基丁烷 的名称:3-甲基丁烷 |
您最近一年使用:0次
名校
解题方法
7 . 下列各组物质中,都是由极性键构成的极性分子的是
| A.PCl3和NCl3 | B.BeCl2(g)和HCl | C.NH3和BH3 | D.CO2和SO2 |
您最近一年使用:0次
2024-01-20更新
|
364次组卷
|
7卷引用:山东省济南市2023-2024学年高二上学期1月期末化学试题
23-24高二·全国·假期作业
解题方法
8 . CH4和CH3Cl分子的空间结构都是正四面体。( )
您最近一年使用:0次
23-24高二·全国·假期作业
解题方法
9 . C2H4分子中的键角都约是120°,则碳原子的杂化方式是sp2。( )
您最近一年使用:0次
23-24高二·全国·假期作业
解题方法
10 . 由价层电子对互斥模型可知SnBr2分子中Sn—Br的键角小于180°。( )
您最近一年使用:0次



