名校
解题方法
1 . 锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为_______ 。
(2) 具有较高的熔点(872℃),其化学键类型是
具有较高的熔点(872℃),其化学键类型是_______ ; 不溶于有机溶剂而
不溶于有机溶剂而 、
、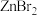 、
、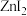 却能够溶于乙醇、乙醚等有机溶剂,你分析其中原因可能是
却能够溶于乙醇、乙醚等有机溶剂,你分析其中原因可能是_______ 。(已知电负性:Zn-1.6 F-4.0 Cl-3.0 Br-2.8 I-2.5)
(3)《中华本草》等中医典籍中,记载了炉甘石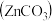 入药,可用于治疗皮肤炎症或表面创伤。
入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为_______ ,C原子的杂化形式为_______ 。
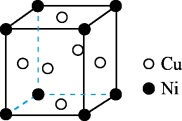
(4)某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为_______ 。
(5)钒的某种氧化物晶胞结构如图1所示(O原子2个位于体内,4个位于面上)。该氧化物的化学式为_______ ,若它的晶胞棱长为x nm(假设为正六面体),则该晶体的密度为_______  。(原子量:V 51,O 16;
。(原子量:V 51,O 16; ;阿伏加德罗常数为
;阿伏加德罗常数为 )
)

(1)Zn原子核外电子排布式为
(2)
 具有较高的熔点(872℃),其化学键类型是
具有较高的熔点(872℃),其化学键类型是 不溶于有机溶剂而
不溶于有机溶剂而 、
、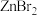 、
、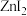 却能够溶于乙醇、乙醚等有机溶剂,你分析其中原因可能是
却能够溶于乙醇、乙醚等有机溶剂,你分析其中原因可能是(3)《中华本草》等中医典籍中,记载了炉甘石
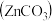 入药,可用于治疗皮肤炎症或表面创伤。
入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为(4)某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为

(5)钒的某种氧化物晶胞结构如图1所示(O原子2个位于体内,4个位于面上)。该氧化物的化学式为
 。(原子量:V 51,O 16;
。(原子量:V 51,O 16; ;阿伏加德罗常数为
;阿伏加德罗常数为 )
)
您最近一年使用:0次
2022-09-08更新
|
401次组卷
|
2卷引用:北京市第十四中学2022-2023学年高三上学期开学检测化学试题
2022高三·全国·专题练习
2 . 硫铁化合物( 、
、 等)应用广泛。
等)应用广泛。
(1)纳米 可去除水中微量六价铬
可去除水中微量六价铬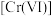 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。
已知: ,
,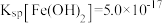 ;
; 电离常数分别为
电离常数分别为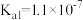 、
、 。
。
①在弱碱性溶液中, 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为_______ 。
②在弱酸性溶液中,反应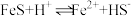 的平衡常数K的数值为
的平衡常数K的数值为_______ 。
③在 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是_______ 。
(2) 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为_______ ,在 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
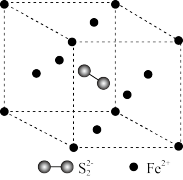
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来_______ 。
(3) 、
、 在空气中易被氧化,将
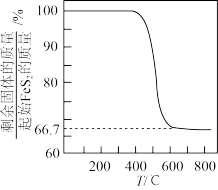
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为_______ (填化学式,写出计算过程)。
 、
、 等)应用广泛。
等)应用广泛。(1)纳米
 可去除水中微量六价铬
可去除水中微量六价铬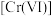 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。已知:
 ,
,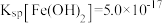 ;
; 电离常数分别为
电离常数分别为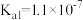 、
、 。
。①在弱碱性溶液中,
 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为②在弱酸性溶液中,反应
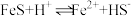 的平衡常数K的数值为
的平衡常数K的数值为③在
 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是(2)
 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来
(3)
 、
、 在空气中易被氧化,将
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为
您最近一年使用:0次
2022-07-21更新
|
8788次组卷
|
13卷引用:北京市第二中学2022-2023学年高三下学期2月开学测试化学试题
北京市第二中学2022-2023学年高三下学期2月开学测试化学试题北京市第二中学2023-2024学年高三下学期开学考化学试卷(已下线)2022年北京高考真题化学试题变式题(结构与性质)(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题14-17(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十四 结构性质中的新材料(已下线)专题三 离子反应-实战高考·二轮复习核心突破江苏省南京市金陵中学河西分校2022-2023学年高二上学期期末检测化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(结构与性质)(已下线)专题20 结构与性质(已下线)专题20 结构与性质
名校
解题方法
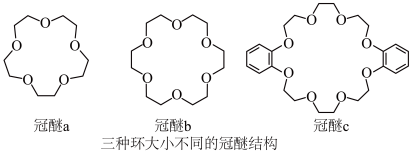
3 . 超分子指多个分子组合在一起形成的具有特定结构和功能的聚集体,超分子内部分子通过非共价键相结合.冠醚是大环多醚类物质的总称,能与阳离子作用,并随环大小不同对阳离子具有选择性作用,图为常见的三种冠醚结构。
已知: 与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
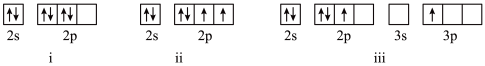
(1)下列冠醚中O原子的基态或激发态价电子中,能量由低到高排列的正确顺序为________ 。
(2) 具有强氧化性,
具有强氧化性, 在元素周期表中的位置是
在元素周期表中的位置是________ ,其水溶液对环己烯的氧化效果很差,若将环己烯溶于冠醚b再加入 ,氧化效果大幅度提升,原因是
,氧化效果大幅度提升,原因是________ 。
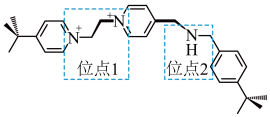
(3)分子A(结构如图所示)能与冠醚c形成一种分子梭结构,其中N的杂化为________ ,该分子梭可以通过加入酸或碱使冠醚c在位点1和位点2之间来回移动.加酸冠醚c移动到位点2,冠醚c与位点2之间的相互作用为________ 。
a.静电相互作用 b.离子键 c.共价键 d.氢键
(4) 与冠醚a结合能力强,
与冠醚a结合能力强, 有独特的电性、磁性和光致发光性能。
有独特的电性、磁性和光致发光性能。
① 的价电子排布式为
的价电子排布式为________ 。
② 晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中
晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中 的配位数为
的配位数为________ ,该晶体密度为 ,则该晶胞的棱长为
,则该晶胞的棱长为________  。
。
已知:
 与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
(1)下列冠醚中O原子的基态或激发态价电子中,能量由低到高排列的正确顺序为

(2)
 具有强氧化性,
具有强氧化性, 在元素周期表中的位置是
在元素周期表中的位置是 ,氧化效果大幅度提升,原因是
,氧化效果大幅度提升,原因是(3)分子A(结构如图所示)能与冠醚c形成一种分子梭结构,其中N的杂化为

a.静电相互作用 b.离子键 c.共价键 d.氢键
(4)
 与冠醚a结合能力强,
与冠醚a结合能力强, 有独特的电性、磁性和光致发光性能。
有独特的电性、磁性和光致发光性能。①
 的价电子排布式为
的价电子排布式为②
 晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中
晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中 的配位数为
的配位数为 ,则该晶胞的棱长为
,则该晶胞的棱长为 。
。
您最近一年使用:0次
2022-05-29更新
|
501次组卷
|
3卷引用:北京市第二中学2023-2024学年高三下学期开学考试化学试卷
4 . MnO2可作氨选择性催化还原法脱除NOx的催化剂。
(1)基态Mn的价层电子排布的轨道表示式是____ 。
(2)MnO2可由(NH4)2S2O8与MnSO4反应制得。S2O 的结构如图。
的结构如图。

①S2O 中S—O—O
中S—O—O____ (填“是”或“不是”)在一条直线上。
②S2O 中的O—O比H2O2中的更
中的O—O比H2O2中的更____ (填“难”或“易”)断裂。
(3)一种MnO2晶体的晶胞示意图如图,该长方体晶胞的长和宽均为anm,高为bnm。

①图中“●”代表的是____ (填“Mn”或“O”)。
②NA为阿伏加德罗常数,该晶体的密度为____ g·cm-3。
③MnO2作催化剂,氨催化还原脱除NO的一种催化机理示意图如图。

从化学键的角度解释MnO2能结合NH3的原因:____ 。该催化过程的总反应的化学方程式是____ 。
(1)基态Mn的价层电子排布的轨道表示式是
(2)MnO2可由(NH4)2S2O8与MnSO4反应制得。S2O
 的结构如图。
的结构如图。
①S2O
 中S—O—O
中S—O—O②S2O
 中的O—O比H2O2中的更
中的O—O比H2O2中的更(3)一种MnO2晶体的晶胞示意图如图,该长方体晶胞的长和宽均为anm,高为bnm。

①图中“●”代表的是
②NA为阿伏加德罗常数,该晶体的密度为
③MnO2作催化剂,氨催化还原脱除NO的一种催化机理示意图如图。

从化学键的角度解释MnO2能结合NH3的原因:
您最近一年使用:0次
2022-05-08更新
|
639次组卷
|
4卷引用:北京市广渠门中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
5 . 由氧元素形成的常见物质有H2O、H2O2、O2和O3等。
(1)基态氧原子的电子排布式是_______ 。
(2)H2O分子的VSEPR模型是_______ 形。
(3)对H2O2分子结构的研究,曾有以下推测:

①根据测定H2O2分子中_______ (填字母序号),确定其结构一定不是甲。
a.H-O键长 b.O-O键能 c.H-O-O键角
②由于H2O2不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素( )与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
)与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
a.H2O2为_______ (填“极性”或“非极性”)分子。
b.用“X—H…Y”表示出上述晶体中形成的氢键:_______ 。
(4)O2的晶胞为立方体,结构如下。
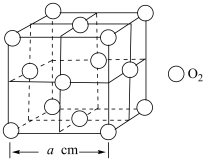
根据图中信息,可计算O2晶体密度是_____ g·cm-3。
(5)已知O3分子空间结构为V形,中心O为sp2杂化。除σ键外,O3分子中还形成了含4个电子的大π键。每个O3分子中用于成键的电子总数是_____ 个,中心O提供参与成键的电子数是_____ 个。
(1)基态氧原子的电子排布式是
(2)H2O分子的VSEPR模型是
(3)对H2O2分子结构的研究,曾有以下推测:

①根据测定H2O2分子中
a.H-O键长 b.O-O键能 c.H-O-O键角
②由于H2O2不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素(
 )与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
)与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。a.H2O2为
b.用“X—H…Y”表示出上述晶体中形成的氢键:
(4)O2的晶胞为立方体,结构如下。

根据图中信息,可计算O2晶体密度是
(5)已知O3分子空间结构为V形,中心O为sp2杂化。除σ键外,O3分子中还形成了含4个电子的大π键。每个O3分子中用于成键的电子总数是
您最近一年使用:0次
2022-05-08更新
|
705次组卷
|
5卷引用:北京市清华大学附属中学2023-2024学年高三上学期开学考试化学(B)试题
名校
解题方法
6 . Zn2+、三乙撑二胺和对苯二甲酸根离子可形成晶体M,其晶胞示意图如下。_______ 。
(2)C、O、N的电负性从大到小的顺序是_______ 。
(3)三乙撑二胺( )与Zn2+能形成配位键的原因是
)与Zn2+能形成配位键的原因是_______ 。
(4)在晶体M每个空腔中装入一个顺式偶氮苯分子后形成晶体M1,晶胞示意图如图。一定条件下随着偶氮苯顺反结构的变化,晶体骨架发生畸变,晶体在M1和M2两种结构之间相互转化,可以吸收和释放N2,被称为“会呼吸”的晶体。
资料:ⅰ.
ⅱ.M1和M2相互转化时,Zn2+的配体和配体数均不变
①N2的电子式是_______ 。
②偶氮苯( )中N的杂化轨道类型是
)中N的杂化轨道类型是_______ 。偶氮苯存在顺反异构的原因是分子中两个氮原子间存在_______ (填“σ键”或“π键”)。
③x=_______ 。
④晶胞密度小则晶体内部的空隙大。能让“会呼吸”的晶体吸收N2的条件是_______ 光照射。

(2)C、O、N的电负性从大到小的顺序是
(3)三乙撑二胺(
 )与Zn2+能形成配位键的原因是
)与Zn2+能形成配位键的原因是(4)在晶体M每个空腔中装入一个顺式偶氮苯分子后形成晶体M1,晶胞示意图如图。一定条件下随着偶氮苯顺反结构的变化,晶体骨架发生畸变,晶体在M1和M2两种结构之间相互转化,可以吸收和释放N2,被称为“会呼吸”的晶体。

晶体 | 装载分子 | 晶胞中Zn2+个数 | 晶胞体积/cm3 |
M1 | 顺式偶氮苯 | x |
|
M2 | 反式偶氮苯 | 4 |
|

ⅱ.M1和M2相互转化时,Zn2+的配体和配体数均不变
①N2的电子式是
②偶氮苯(
 )中N的杂化轨道类型是
)中N的杂化轨道类型是③x=
④晶胞密度小则晶体内部的空隙大。能让“会呼吸”的晶体吸收N2的条件是
您最近一年使用:0次
2022-04-10更新
|
1197次组卷
|
9卷引用:北京交通大学附属中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
7 . 硅是地壳中储量仅次于氧的元素,在自然界中主要以 和硅酸盐的形式存在。
和硅酸盐的形式存在。
(1)基态硅原子的价电子排布式为___________ 。
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次为___________ 。
(3)晶态 的晶胞如图。
的晶胞如图。

①硅原子的杂化方式为___________ 。
②已知 晶胞的棱长均为a pm,则
晶胞的棱长均为a pm,则 晶体的密度
晶体的密度
___________  (列出计算式)。
(列出计算式)。
(4)硅元素最高价氧化物对应的水化物为原硅酸 。
。
资料:原硅酸()( )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
①原硅酸钠 溶液吸收空气中的
溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:___________ 。
②从结构的角度解释 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:___________ 。
 和硅酸盐的形式存在。
和硅酸盐的形式存在。(1)基态硅原子的价电子排布式为
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次为
(3)晶态
 的晶胞如图。
的晶胞如图。
①硅原子的杂化方式为
②已知
 晶胞的棱长均为a pm,则
晶胞的棱长均为a pm,则 晶体的密度
晶体的密度
 (列出计算式)。
(列出计算式)。(4)硅元素最高价氧化物对应的水化物为原硅酸
 。
。资料:原硅酸()(
 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。①原硅酸钠
 溶液吸收空气中的
溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:②从结构的角度解释
 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:
您最近一年使用:0次
2022-04-01更新
|
701次组卷
|
6卷引用:北京交通大学附属中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
8 . 铁的多种化合物均为磁性材料,氮化铁(FexNy)是其中一种,某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe在元素周期表中的位置______ 。
(2)丙酮(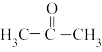 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是______ ,1mol丙酮分子中含有σ键的数目为______ mol。
(3)乙醇的晶体类型为______ ,乙醇分子中C、O、H三种元素中电负性最大的元素是______ 。
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是______ 。
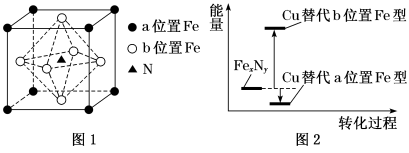
(5)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。由FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为______ 。基态Cu原子的价电子轨道表示式为______ 。
(1)Fe在元素周期表中的位置
(2)丙酮(
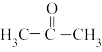 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)乙醇的晶体类型为
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是
(5)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。由FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
2022-01-18更新
|
496次组卷
|
3卷引用:北京市第一七一中学2021-2022学年高三下学期开学考试化学试卷
9 . 硼及其化合物在新材料、工农业生产等方面用途广泛。
(1)氮化硼存在不同的变体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,则六方氮化硼的晶体类型属于_______ 。
②高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,每个立方氮化硼晶胞中硼原子和氮原子的个数比为_______ 。
(2)氨硼烷( )是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
)是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)

①氨硼烷分子为_______ (填“极性”或“非极性”)分子。
②氨硼烷分子中,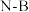 键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:
键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:_______ 。
③氨硼烷常温下为固态,它的熔点比乙烷的熔点高近300℃,是由于其分子间除了分子间作用力,还存在正电性H和负电性H的相互作用,这种作用称为“双氢键”。仿照氢键的表示方法:“ ”,上述双氢键可表示为
”,上述双氢键可表示为_______ (式中用“ ”及“
”及“ ”表示氢的带电情况)。
”表示氢的带电情况)。
④氨硼烷常温下稳定,加热到90℃左右分解产生 ,若该反应中只有氢元素的化合价发生变化,则每产生
,若该反应中只有氢元素的化合价发生变化,则每产生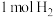 ,反应转移的电子的物质的量是
,反应转移的电子的物质的量是_______  。
。
⑤由氨硼:烷的组成或性质分析,氨硼烷作为储氢材料的优势有_______ 。
(1)氮化硼存在不同的变体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,则六方氮化硼的晶体类型属于
②高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,每个立方氮化硼晶胞中硼原子和氮原子的个数比为
(2)氨硼烷(
 )是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
)是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
①氨硼烷分子为
②氨硼烷分子中,
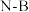 键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:
键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:③氨硼烷常温下为固态,它的熔点比乙烷的熔点高近300℃,是由于其分子间除了分子间作用力,还存在正电性H和负电性H的相互作用,这种作用称为“双氢键”。仿照氢键的表示方法:“
 ”,上述双氢键可表示为
”,上述双氢键可表示为 ”及“
”及“ ”表示氢的带电情况)。
”表示氢的带电情况)。④氨硼烷常温下稳定,加热到90℃左右分解产生
 ,若该反应中只有氢元素的化合价发生变化,则每产生
,若该反应中只有氢元素的化合价发生变化,则每产生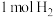 ,反应转移的电子的物质的量是
,反应转移的电子的物质的量是 。
。⑤由氨硼:烷的组成或性质分析,氨硼烷作为储氢材料的优势有
您最近一年使用:0次
2021-07-12更新
|
283次组卷
|
2卷引用:北京市中国农业大学附属中学2021-2022学年高三上学期开学考试化学试题
名校
10 . 金属K和C60能够发生反应产生一系列金属球碳盐KxC60,部分金属球碳盐具有超导性,是球碳族化合物的研究热点之一、
(1)K中含有的化学键是___________ 键。
(2)C60晶体中分子密堆积,其晶胞结构如图所示。C60晶体属于___________ 晶体,每个C60分子周围等距离且紧邻的C60有___________ 个。

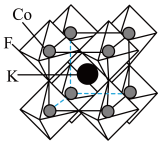
(3)某种KxC60的晶胞结构如图所示。 位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。
位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。

① KxC60中x=___________ 。
② 该晶胞立方体的边长为a cm,NA为阿伏加德罗常数的值,KxC60的摩尔质量为M g/mol,则晶体的密度为___________ g/cm3。
③ KxC60的熔点高于C60,原因是___________ 。
(1)K中含有的化学键是
(2)C60晶体中分子密堆积,其晶胞结构如图所示。C60晶体属于

(3)某种KxC60的晶胞结构如图所示。
 位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。
位于立方体晶胞的顶点和面心,K+位于晶胞的体心和棱心,另外晶胞内还有8个K+。
① KxC60中x=
② 该晶胞立方体的边长为a cm,NA为阿伏加德罗常数的值,KxC60的摩尔质量为M g/mol,则晶体的密度为
③ KxC60的熔点高于C60,原因是
您最近一年使用:0次
2021-07-11更新
|
584次组卷
|
7卷引用:北京市通州区潞河中学2021-2022学年高三下学期开学考试化学试卷





