解题方法
1 . 某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象________ 。
(2)U形管中溶液的颜色_____ ,说明有__________ 生成。
(3)铜丝的变化现象____________ ,说明有________ 生成;若去掉后面的装置,简述检验气体的方法____
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______ 。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象
(2)U形管中溶液的颜色
(3)铜丝的变化现象
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是
您最近一年使用:0次
2019-08-31更新
|
528次组卷
|
5卷引用:贵州省黎平第二中学2019-2020学年高一上学期期末考试化学试题
贵州省黎平第二中学2019-2020学年高一上学期期末考试化学试题广西武宣县第二中学2019-2020学年高一上学期期末考试化学试题第二课时 研究物质性质的基本方法 练习鲁教版高中化学必修1第一章《认识化学科学》测试卷2(已下线)1.2.1 研究物质性质的基本方法 练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)
名校
2 . 某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示

(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是___________ 、___________ 。
(2)下列实验方案适用于在实验室制取所需SO2的是______________________ 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.硫化氢在纯氧中燃烧
(3)装置C的作用是_________________________________ 。
(4)装置B中反应的离子方程式____________________________________________ 。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿色,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的方案是___________ ,原因是___________ 。

(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是
(2)下列实验方案适用于在实验室制取所需SO2的是
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.硫化氢在纯氧中燃烧
(3)装置C的作用是
(4)装置B中反应的离子方程式
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿色,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的方案是
您最近一年使用:0次
2019-01-30更新
|
160次组卷
|
6卷引用:贵州省思南中学2019-2020学年高二下学期期末考试化学试题
3 . 为了探究和验证氯气的性质,某研究性学习小组以MnO2和浓盐酸为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了研究。

(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________ 。
(2)装置B中的试剂为_________ ,装置D作用是________ 。
(3)装置C中发生反应的离子方程式为_____________________________ 。
(4)反应开始后,装置E发生反应的化学方程式为____________________________ 。
(5)装置F中发生反应的化学方程式为________________________ 。

(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为
(2)装置B中的试剂为
(3)装置C中发生反应的离子方程式为
(4)反应开始后,装置E发生反应的化学方程式为
(5)装置F中发生反应的化学方程式为
您最近一年使用:0次
4 . 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下"Fe与水蒸气反应的实验"。

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是_____________ 。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_______________ ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_______________ 。
(3)酒精灯和酒精喷灯点燃的顺序是__________ 。
(4)干燥管中盛装的物质可以是_____________ ,作用是__________ 。
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行_________ ,这一操作的目的_____ 。

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)干燥管中盛装的物质可以是
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行
您最近一年使用:0次
2018-12-05更新
|
437次组卷
|
7卷引用:贵州省剑河县第二中学2019-2020学年高一上学期期末考试化学试题
贵州省剑河县第二中学2019-2020学年高一上学期期末考试化学试题贵州省天柱县第二中学2019-2020学年高一上学期期末考试化学试题云南省通海三中2019-2020学年高一上学期期末考试化学试题云南省玉溪市民族中学2021-2022学年高一上学期期末考试化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高一上学期期中考试化学试题(已下线)专题3.1.1 铁的单质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)云南省玉溪市通海县第三中学2020-2021学年高一上学期期中考试化学试题
5 . 下图是实验室干馏煤的装置图,结合下图回答问题。
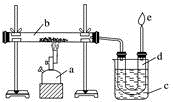
(1)指出图中仪器名称:a__________ ;b__________ ;c__________ ;d__________ 。
(2)装置c的作用是____________________________________ ,d中的液体有________ 和________ 。有机物可以通过________ 的方法使其中的重要成分分离出来。
(3)e处点燃的气体是________ ,火焰的颜色是________ 色。
(4)下列叙述错误的是________ 。
A.煤发生了化学变化
B.d中液体显碱性
C.d中液体不分层
D.e处的气体可以还原氧化铜,也可以使溴水褪色

(1)指出图中仪器名称:a
(2)装置c的作用是
(3)e处点燃的气体是
(4)下列叙述错误的是
A.煤发生了化学变化
B.d中液体显碱性
C.d中液体不分层
D.e处的气体可以还原氧化铜,也可以使溴水褪色
您最近一年使用:0次
2018-08-02更新
|
234次组卷
|
5卷引用:贵州省剑河县二中2018-2019学年高二上学期期末考试化学试题
6 . 某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________ (填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
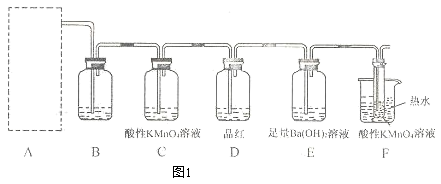
试回答下列问题:
①图1的A中最好选用下列装置_________ (填编号);
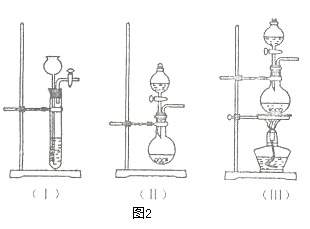
②图1的 B装置所装试剂是_________ ;D装置中试剂的作用是_________ ;E装置中发生的现象是_________ ;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________ ,后体积膨胀的化学方程式为:_________ ;
④某学生按图进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________ ,其反应的离子方程式是_________ 。
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
①图1的A中最好选用下列装置

②图1的 B装置所装试剂是
③图1的A装置中使蔗糖先变黑的化学反应方程式为
④某学生按图进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因
您最近一年使用:0次
2018-06-29更新
|
547次组卷
|
30卷引用:贵州省毕节纳雍县一中2018-2019学年高二下学期期末考试化学试题
贵州省毕节纳雍县一中2018-2019学年高二下学期期末考试化学试题贵州省麻江县第一中学2019-2020学年高二上学期期末考试化学试题贵州省黔西南布依族苗族自治州册亨县第三中学2019-2020学年高二上学期期末考试化学试题贵州省铜仁市沿河县第二高级中学2019-2020学年高二上学期期末考试化学试题云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题云南省玉溪市江川区二中2019-2020学年高二上学期期末考试化学试题云南省陇川县民族中学2019-2020学年高二上学期期末考试化学试题云南省普洱市墨江县民族学校2019—2020学年高二上学期期末考试化学试题云南省普洱市景东县第二中学2019-2020学年高二上学期期末考试化学试题云南省巧家县第三中学2019-2020学年高二上学期期末考试化学试题云南省盐津县第三中学2019-2020学年高二上学期期末考试化学试题云南省昭通市水富县第二中学2019-2020学年高二上学期期末考试化学试题云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题云南省绥江县第三中学2019-2020学年高二上学期期末考试化学试题云南省昭通市巧家县第四中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市马龙区第二中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市沾益县第二中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市富源县第三中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市陆良县第十中学2019-2020学年高二上学期期末考试化学试题广西来宾市象州县中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区崇左市扶绥县第二中学2019-2020学年高二上学期期末考试化学试题广西来宾市忻城县高级中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区来宾市金秀县民族中学2019-2020学年高二上学期期末考试化学试题云南省建水县民中2017-2018学年高二下学期6月份考试化学试题云南省玉溪市通海县第三中学2019-2020学年高二上学期12月月考化学试题云南省红河哈尼族彝族自治州绿春县一中2019-2020学年高二上学期12月月考化学试题云南省大姚县一中2019-2020学年高二12月月考化学试题云南省永德县第一中学2019-2020学年高二12月月考化学试题云南省玉溪市元江民族中学2019-2020学年高二12月月考化学试题云南省施甸县第三中学2019-2020学年高二12月月考化学试题
解题方法
7 . 为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如图:
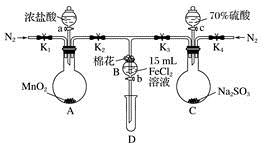
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是________________________ 。
(2)棉花中浸润的溶液为_____________ 。作用是___________________ 。
(3)A中发生反应的化学方程式:______________________________________ 。
(4)导致步骤Ⅲ中溶液变黄的离子反应是______________________________ 。用______________ (写试剂化学式)检验氧化产物,现象是____________ 。
(5)能说明氧化性Fe3+>SO2的离子方程式是__________________________ 。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是________________ (填“甲”“乙”或“丙”)。

Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)A中发生反应的化学方程式:
(4)导致步骤Ⅲ中溶液变黄的离子反应是
(5)能说明氧化性Fe3+>SO2的离子方程式是
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是

您最近一年使用:0次
2018-06-28更新
|
540次组卷
|
4卷引用:贵州省三都水族自治县高级中学2019-2020学年高一上学期期末考试化学试题
8 . 亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。制备装置如下图所示:(其中Ⅲ、Ⅳ、Ⅴ中都为浓硫酸)
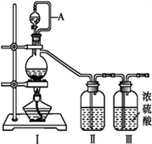
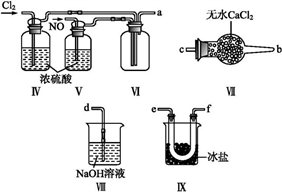
(1)用同一装置Ⅰ、Ⅱ、III分别制备纯净干燥的NO和Cl2,下表中缺少的药品是:
(2)A的作用____________________________ 。
(3)NOCl的电子式_________ 。
(4)利用制得的NO和Cl2制备NOCl,方程式:2NO + Cl2= 2NOCl;装置如上图所示:
①装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________ 。
③装置Ⅷ中吸收尾气时,Cl2发生反应的离子方程式为________________ 。
(5)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气,该反应的化学方程式为__________________ 。


(1)用同一装置Ⅰ、Ⅱ、III分别制备纯净干燥的NO和Cl2,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | 浓盐酸 | ① |
| 制备纯净NO | Cu | ② | 水 |
(3)NOCl的电子式
(4)利用制得的NO和Cl2制备NOCl,方程式:2NO + Cl2= 2NOCl;装置如上图所示:
①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③装置Ⅷ中吸收尾气时,Cl2发生反应的离子方程式为
(5)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 下列陈述Ⅰ和Ⅱ均正确,并存在因果关系的是
| 陈述Ⅰ | 陈述Ⅱ | |
| A | BaSO4难溶于水 | SO2气体通入Ba(NO3)2溶液中产生白色沉淀 |
| B | 非金属性:Cl>S | 酸性:HClO3>H2SO4 |
| C | 常温下,NaHCO3的溶解度比Na2CO3小 | 向饱和Na2CO3溶液中通入CO2产生沉淀 |
| D | 常温下,SO2与氢硫酸和NaOH溶液均可反应 | SO2是两性氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-07-21更新
|
444次组卷
|
3卷引用:贵州省思南中学2016-2017学年高二下学期期末考试化学试题
贵州省思南中学2016-2017学年高二下学期期末考试化学试题四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题(已下线)模块五 非金属及其化合物(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)
名校
10 . 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整_________ 。
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L−1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:__________________ ;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________ ;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是________ (填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是_____________ ,待反应结束后,向C中烧杯内加入沸水,D中观察到的现象是_____________ 。
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决__________________ (实验用品自选)。

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L−1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决
您最近一年使用:0次
2016-12-09更新
|
767次组卷
|
10卷引用:贵州省贵阳市第二中学高一下学期期末考试化学试题
贵州省贵阳市第二中学高一下学期期末考试化学试题四川省棠湖中学2018-2019学年高一下学期期末考试化学试题2015-2016学年河北省武邑中学高一下学期周考化学试卷(已下线)2018年12月11日 《每日一题》人教必修1-浓硫酸的特性【全国百强校】四川省阆中中学2018-2019学年高一下学期期中考试化学试题(已下线)2019年12月10日 《每日一题》化学人教版(必修1)——浓硫酸的特性福建省福州市琅岐中学2017-2018学年高二下学期期中考试化学试题四川省棠湖中学2019-2020学年高一下学期第二次月考化学试题四川省泸县第四中学2019-2020学年高一下学期期中考试化学试题四川省眉山市彭山区第一中学2019-2020学年高一下学期期中考试化学试题



