名校
1 . 亚硝酸钠NaNO2主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物制备产品NaNO2。
回答下列问题:
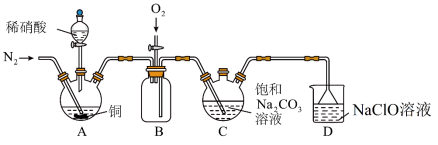
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出反应的化学方程式___________ 。【可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)】___________ 。
(3)装置C中NO不能单独被纯碱溶液吸收,若要使氮的氧化物完全被纯碱溶液吸收且产品纯度最高,则n(NO):n(NO2)=___________ ;装置D中倒置漏斗的作用是___________ 。
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量粗产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
①上述实验___________ (填标号)的结论不可靠,理由是___________ 。
②经实验测得实验乙反应后的溶液中氮元素仅以NO 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为___________ 。
回答下列问题:
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出反应的化学方程式
(3)装置C中NO不能单独被纯碱溶液吸收,若要使氮的氧化物完全被纯碱溶液吸收且产品纯度最高,则n(NO):n(NO2)=
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量粗产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
| 实验操作及现象 | 结论 | |
| 甲 | 滴加少量酸性KI淀粉溶液,振荡,溶液变蓝 | 酸性条件下NO 具有氧化性 具有氧化性 |
| 乙 | 滴加少量酸性KMnO4溶液,振荡,紫色褪去 | 酸性条件下NO 具有还原性 具有还原性 |
②经实验测得实验乙反应后的溶液中氮元素仅以NO
 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 .  (四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为
(四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为 ,含少量
,含少量 、
、 和
和 等)为原料制备四氢铝钠的流程如下。
等)为原料制备四氢铝钠的流程如下。 是酸性氧化物;
是酸性氧化物;
② 。
。
回答下列问题:
(1)浸渣的主要成分是___________ (填化学式)。
(2)“除杂”时铝元素转化的离子方程式为___________ 。
(3)将“沉铝”后的滤液蒸干、灼烧得到的固体是___________ (填化学式)。实验室进行“蒸干、灼烧”时不需要使用的仪器有___________ (填字母)。
A.酒精灯 B.烧杯 C.坩埚 D.蒸发皿
(4)实验室用氢气和钠共热制备 ,
, 的电子式为
的电子式为___________ 。
(5)写出 和
和 反应制备
反应制备 的化学方程式:
的化学方程式:___________ 。
(6)在化学上,含氢还原剂的还原能力用“有效氢”表示。“有效氢”的定义是单位质量含氢还原剂的还原能力相当于多少克氢气。一般地,含氢还原剂中氢元素被氧化成 ,还原能力用失去电子数多少表示。
,还原能力用失去电子数多少表示。 、
、 的“有效氢”之比为
的“有效氢”之比为___________ 。
 (四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为
(四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为 ,含少量
,含少量 、
、 和
和 等)为原料制备四氢铝钠的流程如下。
等)为原料制备四氢铝钠的流程如下。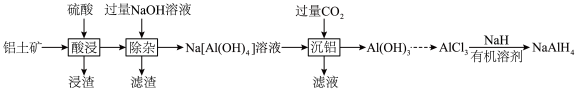
 是酸性氧化物;
是酸性氧化物;②
 。
。回答下列问题:
(1)浸渣的主要成分是
(2)“除杂”时铝元素转化的离子方程式为
(3)将“沉铝”后的滤液蒸干、灼烧得到的固体是
A.酒精灯 B.烧杯 C.坩埚 D.蒸发皿
(4)实验室用氢气和钠共热制备
 ,
, 的电子式为
的电子式为(5)写出
 和
和 反应制备
反应制备 的化学方程式:
的化学方程式:(6)在化学上,含氢还原剂的还原能力用“有效氢”表示。“有效氢”的定义是单位质量含氢还原剂的还原能力相当于多少克氢气。一般地,含氢还原剂中氢元素被氧化成
 ,还原能力用失去电子数多少表示。
,还原能力用失去电子数多少表示。 、
、 的“有效氢”之比为
的“有效氢”之比为
您最近一年使用:0次
名校
解题方法
3 . 亚硝酸钠 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
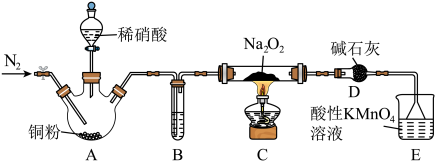
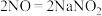 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1) 装置的作用是
装置的作用是___________ 。
(2)写出 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:___________ 。
(3) 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为___________ 。
(4)实验完毕,设计实验证明产品是否含有 :
:___________ 。
(5)为了探究 的性质,设计如下实验:
的性质,设计如下实验:
上述实验能证明 具有氧化性的是
具有氧化性的是___________ (填“I”或“II”)。
(6)取
 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与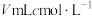 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为___________ (已知: 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
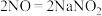 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1)
 装置的作用是
装置的作用是(2)写出
 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:(3)
 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为(4)实验完毕,设计实验证明产品是否含有
 :
:(5)为了探究
 的性质,设计如下实验:
的性质,设计如下实验:| 序号 | 操作 | 现象 |
| I | 取少量 溶于水,滴加酚酞溶液 溶于水,滴加酚酞溶液 | 溶液变红色 |
| II | 取少量  溶于水,滴加稀硫酸和 溶于水,滴加稀硫酸和 溶液,再滴加淀粉溶液 溶液,再滴加淀粉溶液 | 溶液变蓝色 |
 具有氧化性的是
具有氧化性的是(6)取

 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与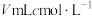 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
您最近一年使用:0次
解题方法
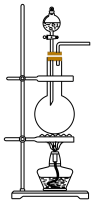
4 . 下列实验装置可用于实验室制备少量无水 ,已知
,已知 遇水会强烈反应。
遇水会强烈反应。
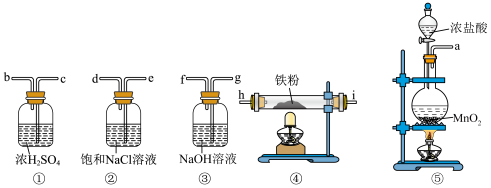
(1)装置⑤装有浓盐酸的仪器名称为_______ ,装有 的仪器名称为
的仪器名称为_______ 。
(2)为达到实验目的,各装置的正确连接顺序是:
__________ 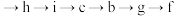 (填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(3)请写出装置⑤中制备氯气的离子方程式_______ 。
(4)装置②的作用_______ 。
(5)请写出④制备 的化学方程式
的化学方程式_______ 。
(6)用离子方程式表示③的作用_______ 。
(7)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃_______ (填装置序号)处酒精灯,后点燃_______ (填装置序号)处酒精灯。
(8)①装置前后两次使用,第1次使用时①装置的作用为_______ ,第2次使用时①装置的作用为_______ 。
 ,已知
,已知 遇水会强烈反应。
遇水会强烈反应。
(1)装置⑤装有浓盐酸的仪器名称为
 的仪器名称为
的仪器名称为(2)为达到实验目的,各装置的正确连接顺序是:

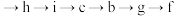 (填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。(3)请写出装置⑤中制备氯气的离子方程式
(4)装置②的作用
(5)请写出④制备
 的化学方程式
的化学方程式(6)用离子方程式表示③的作用
(7)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃
(8)①装置前后两次使用,第1次使用时①装置的作用为
您最近一年使用:0次
5 . 明代宋应星所著的《天工开物》中有关于火法炼锌的记载:“每炉甘石(主要成分为ZnCO3)十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛。……发火煅红,罐中炉甘石熔化成团,冷定,……即倭铅(金属锌)也”。火法炼锌涉及的主要反应为: 。回答下列问题:
。回答下列问题:
(1)“逐层用煤炭饼垫盛”,其中煤炭在该反应中的两个最主要作用是作还原剂和_______ 。
(2)“冷定毁罐取出,……即倭铅(金属锌)也”,“倭铅”要充分冷却之后再“毁罐取出”,原因是_______ 。
(3)若炉甘石中ZnCO3的质量分数为90%,则“每炉甘石十斤(按5kg计)”含ZnCO3的物质的量为_______ 。
(4)某化学兴趣小组在实验室中模拟火法炼锌,采用如下装置进行实验:
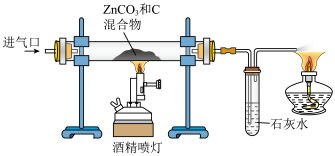
①连接装置,检验_______ 。
②取下硬质玻璃管,装入适量ZnCO3和C的混合粉末后连接装置。
③从进气口先通入氮气,一段时间后再点燃酒精喷灯。先通氮气的目的是_______ 。
④反应完成后,先_______ (填字母序号,下同),待装置冷却后,再_______ 。
A.熄灭酒精喷灯 B.停止通氮气
 。回答下列问题:
。回答下列问题:(1)“逐层用煤炭饼垫盛”,其中煤炭在该反应中的两个最主要作用是作还原剂和
(2)“冷定毁罐取出,……即倭铅(金属锌)也”,“倭铅”要充分冷却之后再“毁罐取出”,原因是
(3)若炉甘石中ZnCO3的质量分数为90%,则“每炉甘石十斤(按5kg计)”含ZnCO3的物质的量为
(4)某化学兴趣小组在实验室中模拟火法炼锌,采用如下装置进行实验:

①连接装置,检验
②取下硬质玻璃管,装入适量ZnCO3和C的混合粉末后连接装置。
③从进气口先通入氮气,一段时间后再点燃酒精喷灯。先通氮气的目的是
④反应完成后,先
A.熄灭酒精喷灯 B.停止通氮气
您最近一年使用:0次
名校
解题方法
6 . Fe3O4是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备Fe3O4并验证所得产物的成分与性质。回答下列问题:
I.制备Fe3O4


(1)装置A的作用是___________ ;装置D的名称是___________ 。
(2)装置B中反应的化学方程式为___________ 。
(3)实验过程中可观察到E中的现象是___________ 。
Ⅱ.探究B中所得黑色固体的成分
待硬质玻璃管B冷却后,取少许其中的固体物质继续进行如下实验(已知酸性KMnO4溶液能与盐酸发生反应):
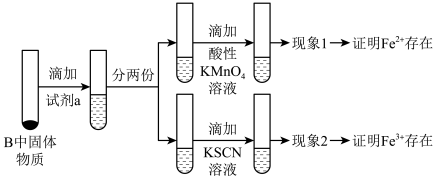
(4)①试剂a是___________ (填物质名称),现象1为___________ 。
②若现象2中溶液未变红色,结合装置B中固体的成分,用离子方程式解释可能的原因:___________ 。
(5)已知温度高于570℃时,铁与水蒸气反应的氧化产物只有Fe3O4,甲同学称取16.8g Fe粉于装置B中,在600℃反应一段时间后停止加热,冷却后称得固体质量为20.0g,则实验后的固体物质中Fe3O4的物质的量为___________ 。
I.制备Fe3O4


(1)装置A的作用是
(2)装置B中反应的化学方程式为
(3)实验过程中可观察到E中的现象是
Ⅱ.探究B中所得黑色固体的成分
待硬质玻璃管B冷却后,取少许其中的固体物质继续进行如下实验(已知酸性KMnO4溶液能与盐酸发生反应):

(4)①试剂a是
②若现象2中溶液未变红色,结合装置B中固体的成分,用离子方程式解释可能的原因:
(5)已知温度高于570℃时,铁与水蒸气反应的氧化产物只有Fe3O4,甲同学称取16.8g Fe粉于装置B中,在600℃反应一段时间后停止加热,冷却后称得固体质量为20.0g,则实验后的固体物质中Fe3O4的物质的量为
您最近一年使用:0次
2024-02-14更新
|
101次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一上学期第三次月考化学试卷
名校
解题方法
7 . 高铁酸钾( )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓 溶液,极易溶于水而成浅紫红色溶液,静置后会分解放出氧气,并生成
溶液,极易溶于水而成浅紫红色溶液,静置后会分解放出氧气,并生成 胶体,因杀菌消毒和除污能力全面优于氯水,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于
胶体,因杀菌消毒和除污能力全面优于氯水,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于 、
、 等。工业上湿法制备
等。工业上湿法制备 的流程如下:
的流程如下:

下列关于 的说法不正确的是
的说法不正确的是
 )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓 溶液,极易溶于水而成浅紫红色溶液,静置后会分解放出氧气,并生成
溶液,极易溶于水而成浅紫红色溶液,静置后会分解放出氧气,并生成 胶体,因杀菌消毒和除污能力全面优于氯水,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于
胶体,因杀菌消毒和除污能力全面优于氯水,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于 、
、 等。工业上湿法制备
等。工业上湿法制备 的流程如下:
的流程如下:
下列关于
 的说法不正确的是
的说法不正确的是A. 在浓 在浓 溶液中的溶解度低于 溶液中的溶解度低于 |
B.将 与盐酸混合使用,可增强其杀菌消毒效果 与盐酸混合使用,可增强其杀菌消毒效果 |
C. 溶液具有除污能力是因为其生成的 溶液具有除污能力是因为其生成的 胶体有吸附作用 胶体有吸附作用 |
D.可用丁达尔效应鉴别 和 和 两种紫红色溶液 两种紫红色溶液 |
您最近一年使用:0次
2024-02-13更新
|
124次组卷
|
2卷引用:海南省海口市琼山区海南中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用废铁屑(含Fe单质约35%、Fe2O3约30%、Fe3O4约29%,含其它不含铁元素的杂质约6%)为原料,制备高纯氧化铁的生产流程示意图。

已知氨水呈碱性(主要成分NH3·H2O是一种碱):(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时废铁屑中的Fe3O4与CO发生反应的化学方程式___________ 。
(2)加适量氨水的目的是___________ ,使加入的(NH4)2CO3能顺利发生复分解反应而生成FeCO3,则②处反应的化学方程式为___________ 。
(3)加入(NH4)2CO3后,该反应必须控制的条件是___________ 。
(4)用蒸馏水洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入少量的BaCl2溶液,___________ (填现象),即为洗涤干净。
(5)ag废铁经上述制备流程,可得到高纯氧化铁的质量最多是___________ g(用含a的式子表示)。

已知氨水呈碱性(主要成分NH3·H2O是一种碱):(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时废铁屑中的Fe3O4与CO发生反应的化学方程式
(2)加适量氨水的目的是
(3)加入(NH4)2CO3后,该反应必须控制的条件是
(4)用蒸馏水洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入少量的BaCl2溶液,
(5)ag废铁经上述制备流程,可得到高纯氧化铁的质量最多是
您最近一年使用:0次
解题方法
9 . 实验室用如图所示装置制备干燥纯净的 并验证氯气没有漂白性。
并验证氯气没有漂白性。
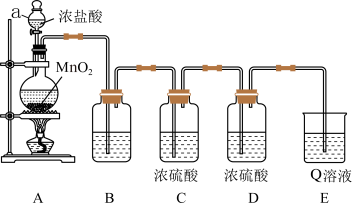

回答下列问题:
(1)仪器 的名称是
的名称是_________ ,装置 中制备氯气的离子方程式为
中制备氯气的离子方程式为____________________________________ 。
(2)装置 中盛放的试剂是
中盛放的试剂是_________ ;欲证明氯气没有漂白性,装置 应置于装置
应置于装置_________ 之间(填字母)。
(3)若Q溶液是 溶液(滴有2滴淀粉试液),则
溶液(滴有2滴淀粉试液),则 中的现象是
中的现象是___________________________ ;若 溶液是
溶液是 溶液且当其恰好反应完后,向
溶液且当其恰好反应完后,向 中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是
中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是_______ ,写出 溶液吸收
溶液吸收 反应的化学方程式:
反应的化学方程式:__________________ 。
 并验证氯气没有漂白性。
并验证氯气没有漂白性。

回答下列问题:
(1)仪器
 的名称是
的名称是 中制备氯气的离子方程式为
中制备氯气的离子方程式为(2)装置
 中盛放的试剂是
中盛放的试剂是 应置于装置
应置于装置(3)若Q溶液是
 溶液(滴有2滴淀粉试液),则
溶液(滴有2滴淀粉试液),则 中的现象是
中的现象是 溶液是
溶液是 溶液且当其恰好反应完后,向
溶液且当其恰好反应完后,向 中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是
中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是 溶液吸收
溶液吸收 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 用如图所示装置进行实验,证明过氧化钠(Na2O2)可在呼吸面具和潜水艇中做供氧剂。
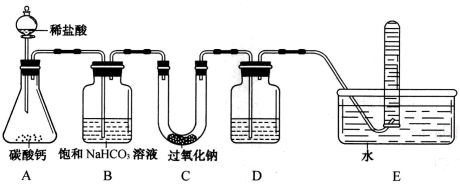
请回答:
(1)装置A中盛放稀盐酸的仪器名称是___ 。
(2)装置B的作用是__ 。
(3)装置C中过氧化钠与二氧化碳反应的化学方程式是__ 。
(4)装置D中盛放的试剂是__ 。
(5)当装置内气流平稳后开始用试管收集气体,该气体能__ ,证明过氧化钠可做供氧剂。

请回答:
(1)装置A中盛放稀盐酸的仪器名称是
(2)装置B的作用是
(3)装置C中过氧化钠与二氧化碳反应的化学方程式是
(4)装置D中盛放的试剂是
(5)当装置内气流平稳后开始用试管收集气体,该气体能
您最近一年使用:0次
2021-08-07更新
|
907次组卷
|
4卷引用:海南省海口嘉勋高级中学2021-2022学年高一下学期(2月)检测化学试题



