解题方法
1 . 四氯化锡( )是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
)是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
回答下列问题:
(1)“仪器a”的名称是___________ ,A中反应的离子方程式为___________ 。
(2)实验前应进行的操作是___________ ,实验开始时,应先点燃___________ (填“A”或“D”)处的酒精灯。
(3)若无“洗气瓶B”,可能会导致的问题是___________ 。
(4)实验结束后,“小试管b”内收集到的液体呈淡黄色,其原因是___________ 。
(5)“洗气瓶F”中所盛放的药品是___________ 。
 )是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
)是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。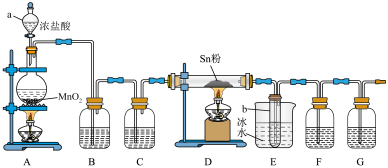
| 药品 | 颜色、状态 | 熔点(℃) | 沸点(℃) | 其他性质 |
| Sn | 银白色固体 | 231 | 2260 | 较活泼金属能与 、HCl等气体发生反应 、HCl等气体发生反应 |
 | 无色液体 | ﹣33 | 114 | 极易与水反应产生 溶胶 溶胶 |
(1)“仪器a”的名称是
(2)实验前应进行的操作是
(3)若无“洗气瓶B”,可能会导致的问题是
(4)实验结束后,“小试管b”内收集到的液体呈淡黄色,其原因是
(5)“洗气瓶F”中所盛放的药品是
您最近一年使用:0次
名校
解题方法
2 . 利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如图所示:
红磷 无色液体与P4(g)
无色液体与P4(g)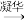 白磷(s)
白磷(s)
红磷
 无色液体与P4(g)
无色液体与P4(g)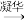 白磷(s)
白磷(s)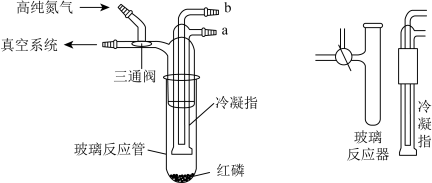
已知:①白磷分子式为P4,易氧化②“三通阀”的孔路结构如图:
| A.红磷使用前水洗可以除去表面的氧化物杂质 |
| B.加热外管并抽真空可以除去装置中的水和氧气 |
C.“冷凝指”的冷凝水需从 口通入 口通入 |
| D.控制“三通阀”可向装置中通入氮气排空气 |
您最近一年使用:0次
3 . 实验室利用 合成磺酰氯(
合成磺酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。
和HClO的酸性强弱进行探究。
Ⅰ.磺酰氯( )是一种重要的有机合成试剂,实验室可利用
)是一种重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应,制取少量的
在活性炭作用下反应,制取少量的 ,
, ,该反应放热,装置如图所示(部分夹持装置省略)。
,该反应放热,装置如图所示(部分夹持装置省略)。
已知 的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。
的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。 ,则下列试剂组合中不合适的是______。
,则下列试剂组合中不合适的是______。
(2)装置乙和丁中可以使用同一种试剂,该试剂为______ 。
(3)仪器b的名称为______ ,其作用是____________ 。
(4)导管a的作用是______ 。
(5)若反应中消耗的氯气体积为896 mL(已转化为标准状况, 足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为______ (保留三位有效数字)。(产率:实际产量/理论产量×100%)
(6)选用下面的装置探究酸性: ,其连接顺序为A→
,其连接顺序为A→______ 。能证明 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为____________ 。
 合成磺酰氯(
合成磺酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。
和HClO的酸性强弱进行探究。Ⅰ.磺酰氯(
 )是一种重要的有机合成试剂,实验室可利用
)是一种重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应,制取少量的
在活性炭作用下反应,制取少量的 ,
, ,该反应放热,装置如图所示(部分夹持装置省略)。
,该反应放热,装置如图所示(部分夹持装置省略)。已知
 的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。
的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。
 ,则下列试剂组合中不合适的是______。
,则下列试剂组合中不合适的是______。A.18.4 mol·L 的硫酸和Cu 的硫酸和Cu | B.10 mol·L 的硝酸和 的硝酸和 固体 固体 |
C.70%的硫酸和 固体 固体 | D.碳和浓硫酸反应 |
(2)装置乙和丁中可以使用同一种试剂,该试剂为
(3)仪器b的名称为
(4)导管a的作用是
(5)若反应中消耗的氯气体积为896 mL(已转化为标准状况,
 足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为(6)选用下面的装置探究酸性:
 ,其连接顺序为A→
,其连接顺序为A→ 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为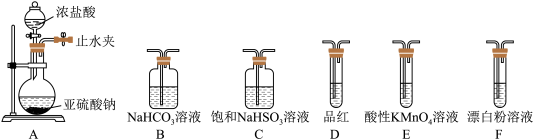
您最近一年使用:0次
4 .  能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为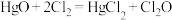 ,装置如图所示。
,装置如图所示。 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是
 能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为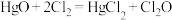 ,装置如图所示。
,装置如图所示。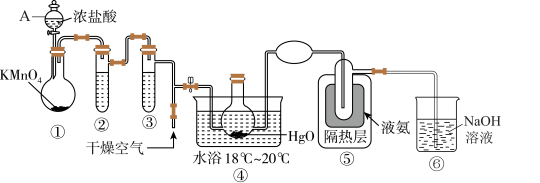
 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。下列说法中正确的是
A.装置②中盛装的试剂是浓硫酸,用来干燥 |
| B.装置④与⑤之间可用橡胶管连接 |
C. 易液化,装置⑤中的液氨只能冷凝 易液化,装置⑤中的液氨只能冷凝 ,因此从装置⑤中逸出气体的主要成分是 ,因此从装置⑤中逸出气体的主要成分是 |
D.通入干燥空气的目的是将生成的 稀释,减小爆炸危险 稀释,减小爆炸危险 |
您最近一年使用:0次
名校
5 . 硫酰氯(SO2Cl2)是一种重要的有机氯化剂,可用于制造医药品、农药和染料等。某化学学习小组用干燥的SO2和Cl2在活性炭催化下制取硫酰氯,反应的化学方程式为: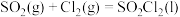 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。
,该反应为放热反应,装置如图所示(部分夹持装置省略)。
(1)仪器A的名称为___________ 。
(2)C中盛放的药品是___________ ,其作用为___________ 。
(3)用浓盐酸和高锰酸钾反应可以制备氯气,写出相关离子方程式___________ 。
(4)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示___________ 。
(5)反应过程中,为防止SO2Cl2分解,可采取的措施有___________ 。(至少写一条)
(6)该化学小组成员经过实验测得产物量较少,猜测可能是原料中亚硫酸钠部分变质,为了验证亚硫酸钠发生了变质,可设计如下实验:取少量亚硫酸钠原料加水溶解,___________ 。
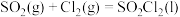 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。
,该反应为放热反应,装置如图所示(部分夹持装置省略)。
(1)仪器A的名称为
(2)C中盛放的药品是
(3)用浓盐酸和高锰酸钾反应可以制备氯气,写出相关离子方程式
(4)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示
(5)反应过程中,为防止SO2Cl2分解,可采取的措施有
(6)该化学小组成员经过实验测得产物量较少,猜测可能是原料中亚硫酸钠部分变质,为了验证亚硫酸钠发生了变质,可设计如下实验:取少量亚硫酸钠原料加水溶解,
您最近一年使用:0次
6 . 某学习小组通过下列装置探究MnO2与FeCl3•6H2O能否反应产生Cl2。

实验操作:点燃酒精灯,加热
实验现象:ⅰ.A中部分固体溶解,上方出现白雾
ⅱ.稍后,产生黄色气体,管壁附着黄色液滴
ⅲ.B中溶液变蓝
已知:①溴水为橙色;
②三氯化铁常温下为固体,熔点为282℃,300℃以上易升华,易溶于水。
(1)现象ⅰ中的白雾主要成分是______ (化学式)的水溶液。
(2)分析现象ⅰ和ⅱ,推测黄色气体的成分,有以下三种可能:
甲.同时存在Cl2和FeCl3 乙.FeCl3 丙.Cl2
①为检验黄色气体中是否存在氯化铁,应将黄色气体通入______ 溶液,溶液变红。黄色气体中存在氯化铁说明氯化铁具有的性质为______ 。
结论:甲或乙成立。
氯化铁可使B中溶液变蓝,反应的离子方程式是____________________ 。
②为进一步确认黄色气体中存在氯气,该小组提出以下2个方案:
Ⅰ.在A、B间增加盛有某种试剂的洗气瓶C除去FeCl3,观察到B中溶液变为蓝色。C中盛放的试剂是______ (填字母序号)
A.饱和NaHCO3溶液 B.NaOH溶液 C.饱和NaCl溶液
D.浓硫酸 E.Na2SO3溶液
Ⅱ.将B中KI—淀粉溶液替换为NaBr溶液,B中溶液呈橙色;并检验反应后不存在 。检验
。检验 的原因是
的原因是____________________ 。
选择NaBr溶液是由氧化剂氧化性的强弱决定,则 、Cl2、Br2的氧化性由强到弱的顺序为
、Cl2、Br2的氧化性由强到弱的顺序为______ 。
结论:甲成立。
(3)使用NaOH溶液处理尾气中存在的Cl2所对应的离子反应方程式为____________________ 。

实验操作:点燃酒精灯,加热
实验现象:ⅰ.A中部分固体溶解,上方出现白雾
ⅱ.稍后,产生黄色气体,管壁附着黄色液滴
ⅲ.B中溶液变蓝
已知:①溴水为橙色;
②三氯化铁常温下为固体,熔点为282℃,300℃以上易升华,易溶于水。
(1)现象ⅰ中的白雾主要成分是
(2)分析现象ⅰ和ⅱ,推测黄色气体的成分,有以下三种可能:
甲.同时存在Cl2和FeCl3 乙.FeCl3 丙.Cl2
①为检验黄色气体中是否存在氯化铁,应将黄色气体通入
结论:甲或乙成立。
氯化铁可使B中溶液变蓝,反应的离子方程式是
②为进一步确认黄色气体中存在氯气,该小组提出以下2个方案:
Ⅰ.在A、B间增加盛有某种试剂的洗气瓶C除去FeCl3,观察到B中溶液变为蓝色。C中盛放的试剂是
A.饱和NaHCO3溶液 B.NaOH溶液 C.饱和NaCl溶液
D.浓硫酸 E.Na2SO3溶液
Ⅱ.将B中KI—淀粉溶液替换为NaBr溶液,B中溶液呈橙色;并检验反应后不存在
 。检验
。检验 的原因是
的原因是选择NaBr溶液是由氧化剂氧化性的强弱决定,则
 、Cl2、Br2的氧化性由强到弱的顺序为
、Cl2、Br2的氧化性由强到弱的顺序为结论:甲成立。
(3)使用NaOH溶液处理尾气中存在的Cl2所对应的离子反应方程式为
您最近一年使用:0次
2024-03-13更新
|
130次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
名校
解题方法
7 . 某学习小组根据氨气还原氧化铜的反应,设计实验测定铜元素相对原子质量Ar(Cu)(近似值)。甲同学模拟合成氨工业制备氨气,反应前先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。装置图如下: 。请回答下列问题:
。请回答下列问题:
(1)C装置应选用______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(2)装置B的作用是:①使气体混合均匀;②______ ;③______ 。
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为____________________ 。
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
(5)G装置的作用是①______ ;②______ 。
若没有G装置,测得结果Ar(Cu)______ (填“偏大”“偏小”或“无影响”)。
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。______ (填化学式)
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=______ (用含有m1、m2、m3的式子表示)。
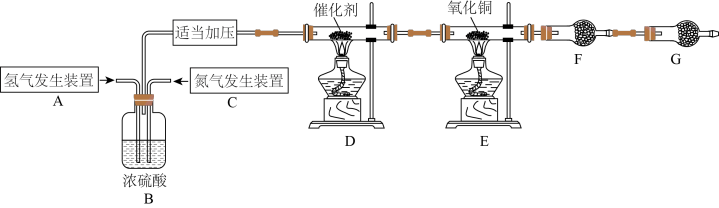
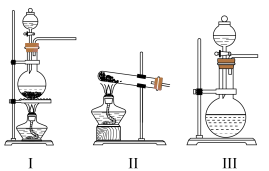
 。请回答下列问题:
。请回答下列问题:(1)C装置应选用
(2)装置B的作用是:①使气体混合均匀;②
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
| A.五氧化二磷 | B.无水CuSO4 | C.碱石灰 | D.无水CaCl2 |
(5)G装置的作用是①
若没有G装置,测得结果Ar(Cu)
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。
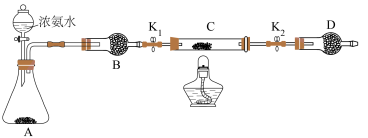
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=
您最近一年使用:0次
2024-03-12更新
|
592次组卷
|
5卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
名校
8 . 粉煤灰是火电厂的大宗固废。以某火电厂的粉煤灰为原料(主要含 、
、 和CaO等)提铝的工艺流程如图所示:
和CaO等)提铝的工艺流程如图所示:

请回答下列问题:
(1)“浸出”时,浸渣的主要成分有_______ 。
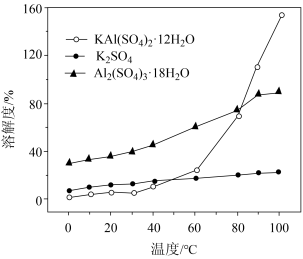
(2)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入 沉铝的目的是
沉铝的目的是_______ 。
(3)实验室在进行“焙烧”操作时,需要的仪器有酒精灯、三脚架、_______ 。
(4)氯化铝的熔点远低于氧化铝,但工业上选择氧化铝制备铝的原因是_______ 。
(5)冰晶石常用作电解制备铝的助熔剂,一种通过烟气净化制备冰晶石的简单流程如下图所示:

已知:酸性强弱:氢氟酸>碳酸
①合成槽中发生反应的化学方程式为_______ 。
②过滤后,经洗涤、干燥可得冰晶石,确定冰晶石已经洗涤干净的方法是_______ 。
 、
、 和CaO等)提铝的工艺流程如图所示:
和CaO等)提铝的工艺流程如图所示:
请回答下列问题:
(1)“浸出”时,浸渣的主要成分有
(2)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入
 沉铝的目的是
沉铝的目的是
(3)实验室在进行“焙烧”操作时,需要的仪器有酒精灯、三脚架、
(4)氯化铝的熔点远低于氧化铝,但工业上选择氧化铝制备铝的原因是
(5)冰晶石常用作电解制备铝的助熔剂,一种通过烟气净化制备冰晶石的简单流程如下图所示:

已知:酸性强弱:氢氟酸>碳酸
①合成槽中发生反应的化学方程式为
②过滤后,经洗涤、干燥可得冰晶石,确定冰晶石已经洗涤干净的方法是
您最近一年使用:0次
9 . 四氯化锡(SnCl4)是合成有机锡化合物的原料,制备SnCl4的装置如图所示(夹持装置已省略)。

已知:①金属锡的熔点为231.9℃,活泼性与铁相似;
②干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4常温下为无色液体,沸点为114℃,极易与水反应;
③ 与浓盐酸在常温下可反应生成
与浓盐酸在常温下可反应生成 。
。
(1)写出装置A中发生反应的化学方程式:___________ 。
(2)A装置中连接分液漏斗和蒸馏烧瓶的橡皮管a的作用是___________ 。
(3)B装置中的试剂是___________ 。
(4)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________ (填现象)后,开始加热D装置,锡熔化后适当增大氯气流量,继续加热D装置,制取并收集SnCl4。开始加热前,先通 的目的是
的目的是___________ 。
(5)F装置的作用是___________ 。
(6)图中F和G装置可用一个简单装置代替,请你提出改进方法:___________ 。

已知:①金属锡的熔点为231.9℃,活泼性与铁相似;
②干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4常温下为无色液体,沸点为114℃,极易与水反应;
③
 与浓盐酸在常温下可反应生成
与浓盐酸在常温下可反应生成 。
。(1)写出装置A中发生反应的化学方程式:
(2)A装置中连接分液漏斗和蒸馏烧瓶的橡皮管a的作用是
(3)B装置中的试剂是
(4)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到
 的目的是
的目的是(5)F装置的作用是
(6)图中F和G装置可用一个简单装置代替,请你提出改进方法:
您最近一年使用:0次
解题方法
10 . 钛白粉(纳米级 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图1。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图1。 反应。
反应。
回答下列问题:
(1)“酸浸”中增加稀硫酸的浸出率的方法有___________ (任写一种)。
(2)图2、图3分别为不同固液比、温度下“浸出”中Ti的浸出率。据图分析,最适合的固液比和温度分别是___________ 和___________ 。 形式存在,该反应的化学方程式为
形式存在,该反应的化学方程式为___________ 。
(4)“一系列操作”包含______________ 、过滤、洗涤、干燥。得到的绿矾用冰水洗涤的目的是___________ 。
(5)若取10kg钛铁矿( 的质量分数为95%),经过上述流程(钛元素损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%),经过上述流程(钛元素损失率为5%),则可制得钛白粉固体的质量为___________ kg。
 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图1。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图1。
 反应。
反应。回答下列问题:
(1)“酸浸”中增加稀硫酸的浸出率的方法有
(2)图2、图3分别为不同固液比、温度下“浸出”中Ti的浸出率。据图分析,最适合的固液比和温度分别是

 形式存在,该反应的化学方程式为
形式存在,该反应的化学方程式为(4)“一系列操作”包含
(5)若取10kg钛铁矿(
 的质量分数为95%),经过上述流程(钛元素损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%),经过上述流程(钛元素损失率为5%),则可制得钛白粉固体的质量为
您最近一年使用:0次



