名校
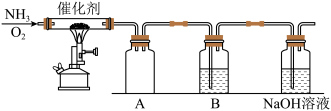
1 . 设计了下图所示的实验装置模拟工业生产制备少量硝酸。___________ (填“吸热”或“放热”),反应的化学方程式是___________ 。
(2)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是___________ ,白烟的化学式是___________ 。
②欲使氨气尽可能完全转化为硝酸,理论上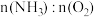 的最佳比例为
的最佳比例为___________ 。
(3)下图中制取氨气的装置和选用的试剂,合理的是(填字母)___________。
(4)实验室制备氨气的化学方程式是___________ 。
(5)用4mol/L稀硝酸与2mol/L稀硫酸的混合液10mL与2.56gCu反应,反应完毕后可生成标准状况下气体的体积是___________ L。
(2)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
②欲使氨气尽可能完全转化为硝酸,理论上
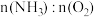 的最佳比例为
的最佳比例为(3)下图中制取氨气的装置和选用的试剂,合理的是(填字母)___________。

| A.①② | B.②③ | C.②④ | D.①③ |
(4)实验室制备氨气的化学方程式是
(5)用4mol/L稀硝酸与2mol/L稀硫酸的混合液10mL与2.56gCu反应,反应完毕后可生成标准状况下气体的体积是
您最近一年使用:0次
2024-04-30更新
|
157次组卷
|
2卷引用:上海市行知中学2023-2024学年高一下学期期中考试 化学试卷
2 . 某研究性学习小组用如图所示装置(部分夹持仪器省略)制备干燥的氨气并验证氨气的性质。已知反应 。
。
 。
。
| A.两盏酒精灯加热顺序是先甲后丁 |
| B.若用丙装置收集氨气,应将b管延长至集气瓶底部 |
C.实验过程中观察到丁中颜色由红棕色变为黑色,说明 具有还原性 具有还原性 |
| D.本实验不需要尾气处理装置 |
您最近一年使用:0次
3 . 实验室用如图所示装置(夹持仪器略)验证 的漂白性并制备无水
的漂白性并制备无水 。查阅相关资料得知:无水
。查阅相关资料得知:无水 在空气中易与水反应,加热易升华。
在空气中易与水反应,加热易升华。
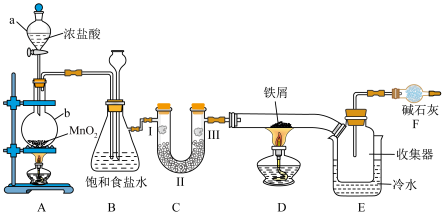
回答下列问题:
(1)仪器 的名称为
的名称为______ ,仪器b中发生反应的离子方程式为______ 。
(2)实验开始时,应先点燃______ (填“A”或“D”)处酒精灯。
(3)装置B中饱和食盐水的作用是______ ,同时还用作安全瓶(监测实验时装置C中是否发生堵塞),若装置C发生堵塞,则装置B中将观察到的现象是______ 。
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中I、Ⅱ、Ⅲ处依次放入的物质是______ 。(填“甲”“乙”“丙”或“丁”)。
(5)装置D中发生反应的化学方程式为______ 。
(6)写出装置 的作用:
的作用:______ 。
 的漂白性并制备无水
的漂白性并制备无水 。查阅相关资料得知:无水
。查阅相关资料得知:无水 在空气中易与水反应,加热易升华。
在空气中易与水反应,加热易升华。
回答下列问题:
(1)仪器
 的名称为
的名称为(2)实验开始时,应先点燃
(3)装置B中饱和食盐水的作用是
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中I、Ⅱ、Ⅲ处依次放入的物质是
| 装置 | I | Ⅱ | Ⅲ |
| 甲 | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| 乙 | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
| 丙 | 干燥的有色布条 | 无水氯化钙 | 湿润的有色布条 |
| 丁 | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
(5)装置D中发生反应的化学方程式为
(6)写出装置
 的作用:
的作用:
您最近一年使用:0次
名校
解题方法
4 . AlCl3是有机合成的催化剂,易潮解,升华温度为178℃。已知:实验室制备氯气的常用方法之一为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。某小组设计实验制备的装置如图所示。下列说法中正确的是

| A.②和③的位置可以互换 |
| B.先启动①中反应,当④中充满黄绿色时再点燃酒精灯 |
| C.上述实验方案只存在1处错误 |
| D.如果用MnO2替代KMnO4也可以完成上述实验 |
您最近一年使用:0次
23-24高一下·全国·课后作业
5 . 关于以下实验装置,说法不正确的是
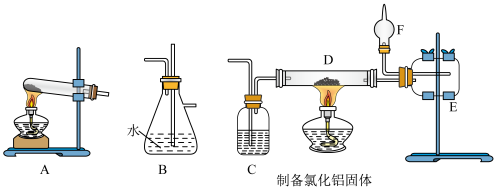

| A.用装置A盛装NH4Cl粉末来制取氨气,并用向下排气法收集 |
| B.装置B既可以防止倒吸,又可以检查实验时装置B后的装置是否发生堵塞 |
| C.装置C、F中盛装的试剂分别为浓硫酸、碱石灰,装置C用来除去Cl2中的水蒸气,装置F用来防止空气中的水蒸气进入装置E |
| D.装置D中的产物受热易升华,最好用粗短导管连接装置D、E |
您最近一年使用:0次
解题方法
6 . 碘化亚铜(CuI)可用作有机合成催化剂,是一种白色粉末,不溶于水,在空气中相对稳定。实验室制备碘化亚铜的装置如图(部分夹持及加热装置已略去):
Ⅰ.取 、40.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、40.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
Ⅱ.打开分液漏斗,将产生的 通向黄色沉淀,充分反应后得到白色沉淀;
通向黄色沉淀,充分反应后得到白色沉淀;
Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)仪器x的名称为_______ 。
(2)已知步骤Ⅰ中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为_______ 。
(3)步骤Ⅱ通入 的主要目的是
的主要目的是_______ 。
(4)单向阀C的作用是_______ 。
(5)步骤Ⅲ中“系列操作”包括_______ 。
(6)已知荧光强度比值与 在一定浓度范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
在一定浓度范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为_______ %(保留一位小数),据此推算CuI的产率接近于_______ (填标号)。

Ⅰ.取
 、40.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、40.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;Ⅱ.打开分液漏斗,将产生的
 通向黄色沉淀,充分反应后得到白色沉淀;
通向黄色沉淀,充分反应后得到白色沉淀;Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)仪器x的名称为
(2)已知步骤Ⅰ中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为
(3)步骤Ⅱ通入
 的主要目的是
的主要目的是(4)单向阀C的作用是
(5)步骤Ⅲ中“系列操作”包括
(6)已知荧光强度比值与
 在一定浓度范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
在一定浓度范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
您最近一年使用:0次
名校
7 . 草酸亚铁( )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。
(1)以 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:

①配制 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是___________ 。
②“转化”步骤的化学方程式为___________ 。
③若该流程中需要使用480mL 0.2000 的草酸溶液,则需要称取
的草酸溶液,则需要称取___________ g草酸晶体( ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及___________ ,若定容时俯视刻度线,则所配溶液中
___________ 0.2000 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:
 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为___________ 。
(3)写出草酸亚铁溶于足量稀硫酸的离子方程式___________ 。
(4)已知: (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是___________ (填化学式)。

 )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。(1)以
 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:
①配制
 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是②“转化”步骤的化学方程式为
③若该流程中需要使用480mL 0.2000
 的草酸溶液,则需要称取
的草酸溶液,则需要称取 ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:

 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为(3)写出草酸亚铁溶于足量稀硫酸的离子方程式
(4)已知:
 (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
您最近一年使用:0次
解题方法
8 . 1,2-二溴乙烷(CH2BrCH2Br)在常温下是无色液体,密度比水大,沸点是131.4 ℃,熔点是9.79 ℃,不溶于水。在实验室中可以用如图所示装置来制备1,2-二溴乙烷。其中烧杯D中小试管装有液溴(表面覆盖少量水)。
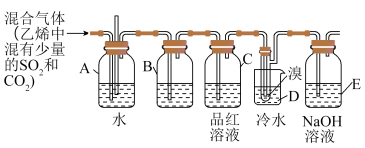
(1)写出制备1,2-二溴乙烷的化学方程式___________ 。
(2)A装置一个作用是可以检查实验进行时D中小试管里的导管是否发生堵塞。另一作用是___________ 。
(3)容器B中所装试剂为___________ 溶液,容器E中NaOH溶液的作用是___________ 。
(4)反应过程中应用冷水冷却装置D,如过度冷却(如用冰水),其后果是___________ 。

(1)写出制备1,2-二溴乙烷的化学方程式
(2)A装置一个作用是可以检查实验进行时D中小试管里的导管是否发生堵塞。另一作用是
(3)容器B中所装试剂为
(4)反应过程中应用冷水冷却装置D,如过度冷却(如用冰水),其后果是
您最近一年使用:0次
9 . Ⅰ.某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
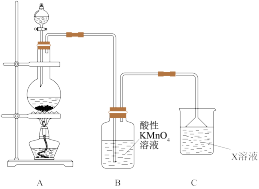
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为___________ 。C装置的作用___________ 。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是___________ 。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为___________ 。
(3)验证该气体的实验方案如下:
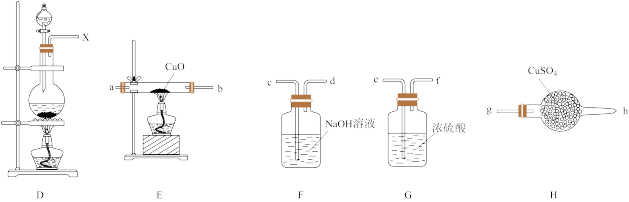
①装置连接顺序:________
X→___________→___________→___________→___________→a→b→___________。
②能证明上述假设成立的实验现象是___________ 。
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处___________ 。

(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是
(3)验证该气体的实验方案如下:

①装置连接顺序:
X→___________→___________→___________→___________→a→b→___________。
②能证明上述假设成立的实验现象是
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处
您最近一年使用:0次
名校
10 . 氯酸锶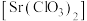 白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。
白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。 可溶于水,
可溶于水, 是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置图如图,反应的化学方程式为
是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置图如图,反应的化学方程式为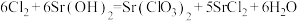 。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
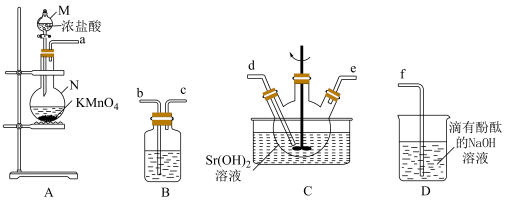
(1)仪器M的名称是___________ ,仪器N的名称是___________ ;
(2)仪器接口的连接顺序a→___________ ;
(3)A中发生反应的离子方程式为___________ ;
(4)使浓盐酸顺利滴下的操作方法为___________ ,再打开分液漏斗下端活塞。
(5)装置B中所装试剂名称为___________ ,其作用是___________ ;
(6)装置C中发生反应的离子方程式为___________ ;
(7)该兴趣小组在40℃条件下,将一定量的 通入一定量的
通入一定量的 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有 和
和 和
和 的物质的量之比为5:1,则此过程中氧化剂和还原剂的质量比为
的物质的量之比为5:1,则此过程中氧化剂和还原剂的质量比为___________ ;
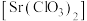 白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。
白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。 可溶于水,
可溶于水, 是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置图如图,反应的化学方程式为
是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置图如图,反应的化学方程式为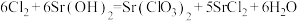 。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
(1)仪器M的名称是
(2)仪器接口的连接顺序a→
(3)A中发生反应的离子方程式为
(4)使浓盐酸顺利滴下的操作方法为
(5)装置B中所装试剂名称为
(6)装置C中发生反应的离子方程式为
(7)该兴趣小组在40℃条件下,将一定量的
 通入一定量的
通入一定量的 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有 和
和 和
和 的物质的量之比为5:1,则此过程中氧化剂和还原剂的质量比为
的物质的量之比为5:1,则此过程中氧化剂和还原剂的质量比为
您最近一年使用:0次
2023-11-16更新
|
140次组卷
|
3卷引用:河北省石家庄市高中五校(一中,正中等)2023-2024学年高一上学期期中联考化学试题



