19. 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如图:
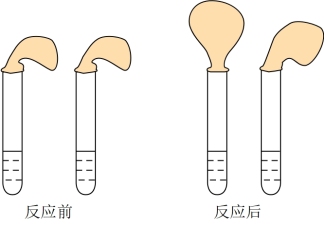
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol∙L
−1的HA、HCl溶液各10mL,按图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1 mol∙L
−1HA和HCl溶液的pH;
②再取0.1 mol∙L
−1的HA和HCl溶液各2滴(1滴约为

mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol∙L
−1的HA溶pH
____1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:
____。
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
____步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H
+)都减小,c(A
-)增大,可在0.1 mol∙L
−1的HA溶液中,选择加入
____试剂(选填“A”“B’“C”“D”下同)。
②使HA的电离程度减小,c(H
+)和c(A
-)都增大,可在0.1 mol∙L
−1的HA溶液中,选择加入
____试剂。
A.NaA固体(可完全溶于水)
B.1 mol∙L
−1NaOH溶液
C.1 mol∙L
−1H
2SO
4 D.2 mol∙L
−1HA