名校
解题方法
1 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。
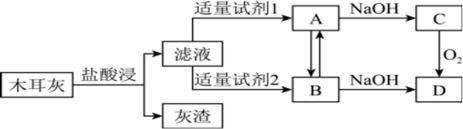
①浸泡液检测不出铁元素的原因是_______ 。
②试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为_______ 。
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为_______ L。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。

①浸泡液检测不出铁元素的原因是
②试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为
您最近一年使用:0次
名校
2 . A、B、C、D、E、F是原子序数依次增大的元素,其相关信息如下。
回答下列问题:
(1)元素A和E形成的化合物的电子式为___________ ,该化合物含有的化学键类型是___________ 。
(2)元素B在元素周期表中的位置为___________ ,其原子结构示意图为___________ 。
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为___________ ;元素D形成的单质久置于空气中最终得到的化合物的化学式为___________ 。
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
| 元素 | 特征 | 元素 | 特征 |
| A | 该元素的某种原子不含中子 | B | 简单氢化物的分子结构模型为 |
| C | 在人体中含量最多 | D | 该元素形成的化合物灼烧时火焰呈现黄色 |
| E | 该元素形成的单质常温下是黄绿色的有毒气体 | F | 由该元素形成的合金是目前我国用途最广的合金 |
(1)元素A和E形成的化合物的电子式为
(2)元素B在元素周期表中的位置为
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
A.酸性: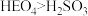 | B. 通入 通入 溶液能产生黄色沉淀 溶液能产生黄色沉淀 |
C.氢化物稳定性: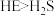 | D.常温下,E的单质为气态,S的单质为固态 |
您最近一年使用:0次
3 . 强氧化剂一般用来进行消毒、漂白等工序。回答下列问题:
(1)臭氧可以通过氧气在放电条件下生成,上述两种单质都是氧元素的_______ 。
(2)1984年,北京第一传染病医院研制成功能迅速杀灭各类肝炎病毒的消毒液,后更名为“84消毒液”。该消毒液可用氯气与氢氧化钠溶液在常温下反应制得,发生反应的离子方程式为_______ 。如果在某次反应中,有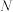 个氯气分子参与此反应,则过程中转移的电子数为
个氯气分子参与此反应,则过程中转移的电子数为_______ 。
(3)漂粉精中的有效成分为_______ ,其进行焰色试验的特征颜色为_______ (填标号)。
a.黄色 b.砖红色 c.绿色 d.紫红色
(4)新型的消毒剂 在中性溶液中可将剧毒的
在中性溶液中可将剧毒的 氧化为两种无毒的气体,自身被还原为
氧化为两种无毒的气体,自身被还原为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为_______ ;“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是“分别在氧化还原反应中得到等量的电子时, 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为_______ (结果保留两位小数)。
(1)臭氧可以通过氧气在放电条件下生成,上述两种单质都是氧元素的
(2)1984年,北京第一传染病医院研制成功能迅速杀灭各类肝炎病毒的消毒液,后更名为“84消毒液”。该消毒液可用氯气与氢氧化钠溶液在常温下反应制得,发生反应的离子方程式为
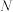 个氯气分子参与此反应,则过程中转移的电子数为
个氯气分子参与此反应,则过程中转移的电子数为(3)漂粉精中的有效成分为
a.黄色 b.砖红色 c.绿色 d.紫红色
(4)新型的消毒剂
 在中性溶液中可将剧毒的
在中性溶液中可将剧毒的 氧化为两种无毒的气体,自身被还原为
氧化为两种无毒的气体,自身被还原为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
4 . X、Y、Z、W是原子序数依次增大的短周期主族元素,可以构成某复合型高分子聚合物 ,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
 ,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是A.简单离子半径大小关系: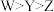 |
| B.M在水中能形成胶体,具有净水、杀菌、消毒的功能 |
| C.Z的最高价氧化物对应的水化物为强碱 |
D.M化学式中存在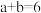 |
您最近一年使用:0次
解题方法
5 . 某学生学习了检验食品中的铁元素后,设想在课外研究测定某补血剂中铁元素(+2价)含量,其设计实验流程如下:
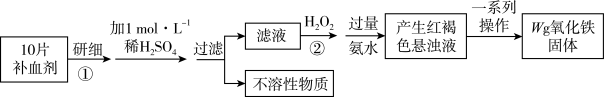
下列说法错误的是

下列说法错误的是
A.步骤②可以用新制氯水替代 |
B.步骤②加入氨水的作用是将 完全沉淀 完全沉淀 |
| C.每片补血剂中含铁元素的质量为0.07Wg |
| D.取步骤①操作后的溶液,滴加几滴KSCN溶液,若溶液变红,证明补血剂已完全被氧化变质 |
您最近一年使用:0次
2024-02-03更新
|
132次组卷
|
2卷引用:内蒙古呼和浩特市2023-2024学年高一上学期期末教学质量检测化学试卷
名校
6 . I.某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
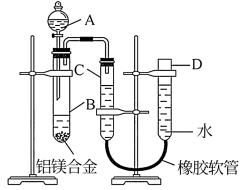
(1)A中试剂为___________ 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是___________ 。
(3)B中发生反应的化学方程式为___________ 。
(4)若实验用的铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为___________ 。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将___________ (填“偏大”“偏小”或“不受影响”)。
II.某同学设计了如图装置(气密性已检查,部分夹持装置已省略)用于制备Fe(OH)2白色沉淀。

请回答下列问题。
(6)仪器1的名称是___________ 。装置5的作用是___________ 。
(7)实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使3中溶液能进入4中:___________ 。
(8)装置改进后,将3中反应后的溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因:___________ 。

(1)A中试剂为
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是
(3)B中发生反应的化学方程式为
(4)若实验用的铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
II.某同学设计了如图装置(气密性已检查,部分夹持装置已省略)用于制备Fe(OH)2白色沉淀。

请回答下列问题。
(6)仪器1的名称是
(7)实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使3中溶液能进入4中:
(8)装置改进后,将3中反应后的溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因:
您最近一年使用:0次
解题方法
7 . 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。
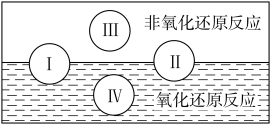
试写出有水参加的符合反应类型IV的一个离子反应方程式:________________ ,其中水为_____________ 剂;
(2)氯化铵常用于焊接。如在焊接铜器时用过量的浓氯化铵溶液除去铜器表面的氧化铜以便焊接,其反应为: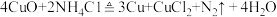
①该反应中,被氧化的元素是_____________ (填元素名称),氧化剂是_____________ (填化学式);
②往反应后的热溶液中加入过量澄清的石灰水,发现有气泡产生,写出该现象的离子方程式:_____________ ;
(3)铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。铝粉和赤铁矿发生铝热反应的化学方程式为:
若反应中消耗了0.2 mol Al,生成Fe的物质的量为____________ mol,转移电子的物质的量为____________ mol。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。

试写出有水参加的符合反应类型IV的一个离子反应方程式:
(2)氯化铵常用于焊接。如在焊接铜器时用过量的浓氯化铵溶液除去铜器表面的氧化铜以便焊接,其反应为:
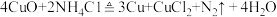
①该反应中,被氧化的元素是
②往反应后的热溶液中加入过量澄清的石灰水,发现有气泡产生,写出该现象的离子方程式:
(3)铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。铝粉和赤铁矿发生铝热反应的化学方程式为:

若反应中消耗了0.2 mol Al,生成Fe的物质的量为
您最近一年使用:0次
8 . 某化学实验室需要0.5 硫酸溶液450
硫酸溶液450 。根据溶液的配制情况回答下列问题:
。根据溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_______ (填序号),本实验所需玻璃仪器E的规格和名称是_______ ;
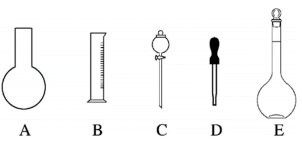
(2)现用质量分数为98%、密度为1.84 的浓硫酸来配制450
的浓硫酸来配制450 、0.5
、0.5 的稀硫酸。计算所需浓硫酸的体积为
的稀硫酸。计算所需浓硫酸的体积为_______  ,现有10
,现有10 、25
、25 、50
、50 、100
、100 四种规格的量筒,你选用的量筒是
四种规格的量筒,你选用的量筒是_______ ;
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_______ ;
(4)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇勺⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为:②→①→③→_______ →_______ →_______ →_______ →④(填序号)。
(5)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度_______ 0.5 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
 硫酸溶液450
硫酸溶液450 。根据溶液的配制情况回答下列问题:
。根据溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是

(2)现用质量分数为98%、密度为1.84
 的浓硫酸来配制450
的浓硫酸来配制450 、0.5
、0.5 的稀硫酸。计算所需浓硫酸的体积为
的稀硫酸。计算所需浓硫酸的体积为 ,现有10
,现有10 、25
、25 、50
、50 、100
、100 四种规格的量筒,你选用的量筒是
四种规格的量筒,你选用的量筒是(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
(4)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇勺⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为:②→①→③→
(5)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度
 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
您最近一年使用:0次
解题方法
9 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:______ 。
(2)D单质与C单质在加热条件下反应产物的电子式________ ,该物质与A2C反应的离子方程式______ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为______ 。
(4)用电子式写出A2C的形成过程________ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)用电子式写出A2C的形成过程
您最近一年使用:0次
10 . W、X、Y和Z为原子序数依次增大的短周期主族元素,W原子最外层电子数是次外层电子数的2倍,X是地壳中含量最多的元素,Y元素的原子是短周期中原子半径最大的原子,Z的质子数比W和X的质子数之和少1,下列说法错误的是
A.原子半径: |
B.化合物 中含有非极性共价键 中含有非极性共价键 |
C.单质的沸点: |
D.单质Z可与Y的最高价氧化物的水化物反应生成 |
您最近一年使用:0次
2023-04-23更新
|
462次组卷
|
4卷引用: 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)
2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)河南省濮阳市许昌市2022-2023学年高一上学期期末联考化学试题河南省濮阳市2022-2023学年高一上学期1月期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)



