20-21高二下·江苏南通·开学考试
名校
1 . 下列图示与对应的叙述相符的是


| A.图甲表示分别稀释0.1 mol·L-1的盐酸和醋酸时溶液pH的变化 |
| B.图乙表示反应2SO2(g)+O2(g)⇌2SO3(g) ΔH<0分别在有、无催化剂的情况下反应过程中的能量变化 |
| C.图丙表示反应H2(g)+I2(g)⇌2HI(g)中正、逆反应速率随时间的变化,t0时刻改变的条件可能是增大体系压强 |
| D.图丁表示反应“N2(g)+3H2(g)⇌2NH3(g) ΔH<0”的平衡常数随温度变化的关系 |
您最近一年使用:0次
2021-03-03更新
|
165次组卷
|
3卷引用:山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题
山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题(已下线)江苏省如皋市2020-2021学年高二下学期期初调研测试化学试题甘肃省张掖市高台县第一中学2022-2023学年高三上学期第四次检测化学试题
名校
2 . I.某学生用已知物质的量浓度的NaOH 标准溶液来测定未知物质的量浓度的盐酸时,选择甲基橙作指示剂。请回答下列问题:
(1)配制480mL 0.1000mol·L-1 NaOH 标准溶液。配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、_______ 、_______ 等。
(2)观察下图,标准液NaOH溶液应放入_______ 滴定管中。(填“甲”或“乙”)

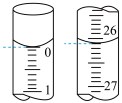
(3)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH 标准溶液的_______ mL。
(4)某学生根据3次实验分别记录有关数据如表所示:
依据表中数据计算该盐酸溶液的物质的量浓度_______ 。
(5)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有_______ (填序号)。
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
II. 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。硫代硫酸钠 又称大苏打,可用作定影剂、还原剂。现有某种硫代硫酸钠样品,为了测定该样品纯度,某兴趣小组设计如下实验方案,回答下列问题:
又称大苏打,可用作定影剂、还原剂。现有某种硫代硫酸钠样品,为了测定该样品纯度,某兴趣小组设计如下实验方案,回答下列问题:
(1)溶液配制:称取10.0g该硫代硫酸钠样品,用_______ (填“新煮沸并冷却的蒸馏水”或“自来水”)在烧杯中溶解完全溶解后冷却至室温,再用玻璃棒引流将溶液全部转移至100mL的容量瓶中,定容。
(2)滴定:取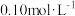 的
的 (硫酸酸化)标准溶液
(硫酸酸化)标准溶液 ,加入过量
,加入过量 ,发生反应:
,发生反应: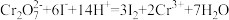 , 然后加入
, 然后加入_______ 溶液作为指示剂,用硫代硫酸钠样品溶液滴定至终点,发生反应: ,滴定终点时溶液的颜色变化是
,滴定终点时溶液的颜色变化是_______ 。重复实验,平均消耗 样品溶液的体积为
样品溶液的体积为 。
。
(3)样品纯度的计算:根据上述有关数据,该样品中 的质量分数为
的质量分数为_______
(1)配制480mL 0.1000mol·L-1 NaOH 标准溶液。配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、
(2)观察下图,标准液NaOH溶液应放入

(3)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH 标准溶液的

(4)某学生根据3次实验分别记录有关数据如表所示:
滴定次数 | 待测盐酸 的体积/mL | 标准NaOH溶液体积 | |
滴定前的刻度/mL | 滴定后的刻度/rnL | ||
第一次 | 25.00 | 0.00 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
(5)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
II. 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。硫代硫酸钠
 又称大苏打,可用作定影剂、还原剂。现有某种硫代硫酸钠样品,为了测定该样品纯度,某兴趣小组设计如下实验方案,回答下列问题:
又称大苏打,可用作定影剂、还原剂。现有某种硫代硫酸钠样品,为了测定该样品纯度,某兴趣小组设计如下实验方案,回答下列问题:(1)溶液配制:称取10.0g该硫代硫酸钠样品,用
(2)滴定:取
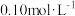 的
的 (硫酸酸化)标准溶液
(硫酸酸化)标准溶液 ,加入过量
,加入过量 ,发生反应:
,发生反应: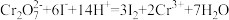 , 然后加入
, 然后加入 ,滴定终点时溶液的颜色变化是
,滴定终点时溶液的颜色变化是 样品溶液的体积为
样品溶液的体积为 。
。(3)样品纯度的计算:根据上述有关数据,该样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 电离平衡常数(K)是衡量弱电解质电离程度的重要指标。下图为水在不同温度下的电离平衡曲线。

(1)常温下,将pH=5的稀盐酸与pH=10的Ba(OH)2溶液混合,然后保持100℃的恒温,欲使混合溶液pH=7,则盐酸与Ba(OH)2的体积比为_______ 。
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,用离子方程式表示Na2CO3溶液显碱性的原因_______ ,由水电离出的c(OH-)=_______ mol·L-1。
(3)298K时,碳酸、醋酸和亚硫酸的电离平衡常数见下表:
①写出向醋酸钠溶液通SO2的离子方程式_______ 。
②为证明醋酸是弱电解质,下列方法正确的是_______ 。
A.测定0.1mol·L-1醋酸溶液的pH
B.测定0.1mol·L-1CH3COONa溶液的酸碱性
C.比较浓度均为0.1mol·L-1盐酸和醋酸溶液的导电能力
D.等pH的盐酸和醋酸溶液,分别与等量的相同颗粒度的Zn反应,观察开始时产生气泡的速率
E.等pH的盐酸和醋酸溶液,比较中和这两种酸所需相同物质的量浓度的NaOH溶液的体积
(4)①将FeCl3的水溶液加热蒸干并灼烧最终得到物质是_______ (填化学式)
②温度相同,浓度均为0.1mol•L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤NH4HSO4溶液,它们中的c( )由大到小的排列顺序是
)由大到小的排列顺序是_______ 。(用序号表示)
(5)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA-⇌H++A2-。现有0.1 mol·L-1 Na2A的溶液,其中各种微粒浓度关系正确的是_______ (填字母)。
A.c(Na+)>c(A2-)>c(OH-)>c(HA-) B.c(Na+)=2c(HA-)+2c((A2-)+2c(H2A)
C.c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-) D.c(OH-)=c(HA-)+c(H+)

(1)常温下,将pH=5的稀盐酸与pH=10的Ba(OH)2溶液混合,然后保持100℃的恒温,欲使混合溶液pH=7,则盐酸与Ba(OH)2的体积比为
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,用离子方程式表示Na2CO3溶液显碱性的原因
(3)298K时,碳酸、醋酸和亚硫酸的电离平衡常数见下表:
名称 | 碳酸 | 醋酸 | 亚硫酸 |
电离常数(298K) | K1=4.4×10–7 K2=4.7×10–11 | K=1.8×10–5 | K1=1.3×10–2 K2=6.2×10–8 |
②为证明醋酸是弱电解质,下列方法正确的是
A.测定0.1mol·L-1醋酸溶液的pH
B.测定0.1mol·L-1CH3COONa溶液的酸碱性
C.比较浓度均为0.1mol·L-1盐酸和醋酸溶液的导电能力
D.等pH的盐酸和醋酸溶液,分别与等量的相同颗粒度的Zn反应,观察开始时产生气泡的速率
E.等pH的盐酸和醋酸溶液,比较中和这两种酸所需相同物质的量浓度的NaOH溶液的体积
(4)①将FeCl3的水溶液加热蒸干并灼烧最终得到物质是
②温度相同,浓度均为0.1mol•L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤NH4HSO4溶液,它们中的c(
 )由大到小的排列顺序是
)由大到小的排列顺序是(5)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA-⇌H++A2-。现有0.1 mol·L-1 Na2A的溶液,其中各种微粒浓度关系正确的是
A.c(Na+)>c(A2-)>c(OH-)>c(HA-) B.c(Na+)=2c(HA-)+2c((A2-)+2c(H2A)
C.c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-) D.c(OH-)=c(HA-)+c(H+)
您最近一年使用:0次
4 . 碳酸钴(CoCO3)是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉。以含钴废料 (主要成分为CoO、Co2O3还含少量Al2O3、Zn等杂质)为原料制备CoCO3的一种工艺如下:
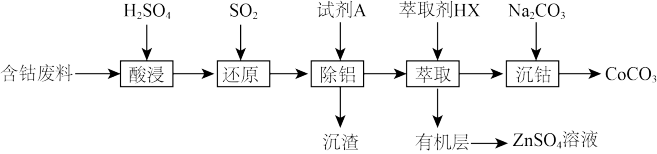
回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是_______ 。
(2)“还原”过程中还原8.3kgCo2O3理论上需消耗SO2的体积为_______ L(标准状况)。
(3)已知“萃取” 的原理为
的原理为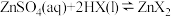 (有机层)
(有机层)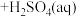 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入__ (填试剂名称),其作用是___ (从平衡移动原理角度分析)。

回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是
(2)“还原”过程中还原8.3kgCo2O3理论上需消耗SO2的体积为
(3)已知“萃取”
 的原理为
的原理为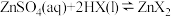 (有机层)
(有机层)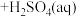 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入
您最近一年使用:0次
名校
5 . 下列有关化学反应速率和化学平衡影响的图像,其中图像和实验结论表达正确的是
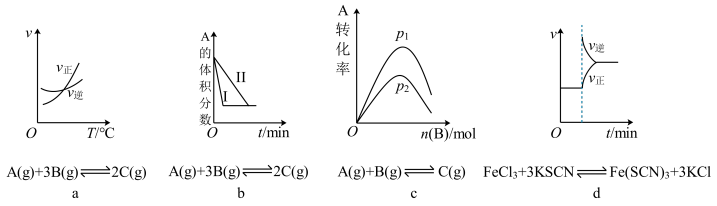

| A.a是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0 |
| B.b是在有无催化剂存在下建立的平衡过程图像,Ⅰ是使用催化剂时的曲线 |
| C.c是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1 <p2 |
| D.d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图像 |
您最近一年使用:0次
名校
6 . 已知Ka(CH3COOH)=1.7×10-5,Kb(NH3·H2O)=1.7×10-5.常温下,用0.01mol·L-1氨水滴定20mL浓度均为0.01mol·L-1的HCl和CH3COOH混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述错误的是
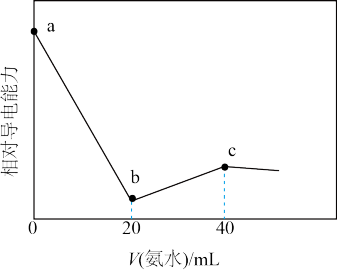

| A.a点的混合溶液中c(CH3COO-)约为1.7×10-3mol·L-1 |
B.b点的混合溶液中:c(CH3COOH)>c(NH ) ) |
C.c点的混合溶液中:c(NH )+c(NH3·H2O)=c(Cl-)+c(CH3COO-)+c(CH3COOH) )+c(NH3·H2O)=c(Cl-)+c(CH3COO-)+c(CH3COOH) |
| D.混合溶液pH=7时,加入氨水体积大于40mL |
您最近一年使用:0次
2021-02-24更新
|
301次组卷
|
6卷引用:山西省寿阳县第一中学2020—2021学年高二上学期第二次月考化学试题
7 . 化学与生产、生活、科技息息相关,下列叙述错误的是
| A.华为首款 5G 手机搭载了智能 7nm 制程 SoC“麒麟 980”手机芯片的主要成分是二氧化硅 |
| B.国产飞机 C919 用到氮化硅陶瓷是新型无机非金属材料 |
| C.小苏打是面包发酵粉的主要成分之一 |
| D.水玻璃可用作制备木材防火剂的原料 |
您最近一年使用:0次
2021-02-24更新
|
624次组卷
|
9卷引用:山西省晋中市现代双语学校2020-2021学年高一下学期第一次月考化学试题
山西省晋中市现代双语学校2020-2021学年高一下学期第一次月考化学试题江西省上饶市2020-2021学年高一上学期期末教学质量测试化学试题四川省成都外国语学校2020-2021学年高一下学期开学考试化学试题广东省普宁市华美实验学校2020-2021学年高一下学期第一次月考化学试题海南省儋州市第二中学2020-2021学年高一下学期3月月考化学试题吉林省长春市实验中学2020-2021学年高一下学期阶段考试化学试题河北省衡水市第十四中学2020-2021学年高一下学期一调考试化学试题广东省中山市第二中学2020-2021学年高一下学期第一次段考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题
8 . 铝氢化钠(NaAlH4)是有机合成中的一种重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝氢化钠的一种工艺流程如图:
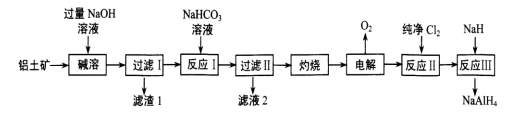
下列说法中错误的是

下列说法中错误的是
| A.为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎 |
| B.“反应I”的部分化学原理与泡沫灭火器的原理相同 |
| C.“滤渣1”的主要成分为氧化铁 |
| D.“反应III”的化学方程式为4NaH+AlCl3=NaAlH4+3NaCl |
您最近一年使用:0次
2021-02-23更新
|
1735次组卷
|
11卷引用:山西省榆次第一中学校 2022-2023学年高三上学期10 月模拟考试化学试题
山西省榆次第一中学校 2022-2023学年高三上学期10 月模拟考试化学试题湖北省武汉市武昌区2021届高三1月质量检测化学试题(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)河南省郑州市维纲中学2022届高三9月月考化学试题山西省太原师范学院附属中学2022-2023 学年高三上学期第一次月考化学试题安徽省六安第一中学2022-2023学年高三上学期第二次月考化学试题山东省威海乳山市银滩高级中学2022-2023学年高三上学期10月月考化学试题江西省丰城市第九中学2021-2022学年高三复读班上学期10月月考化学试题内蒙古自治区呼和浩特市2022-2023学年高三上学期质量普查调研考试化学试题
名校
解题方法
9 . 研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成物质的价类二维图及含硫物质相互转化的部分信息。
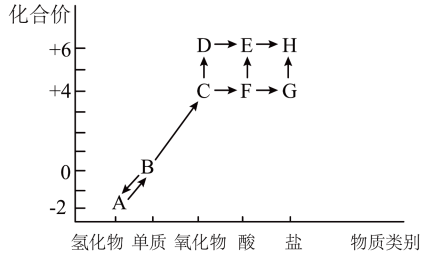
(1)B的化学式是______________ ;G是一种钠盐,它的电离方程式是_________________ 。
(2)C有毒,实验室可以用NaOH溶液吸收,反应的化学方程式是_________________ 。
(3)检验H中阴离子的实验操作及现象是_____________ 。
(4)C→D→E以及C→F→E都是造成酸雨的可能途径,请写出其中任意一条路径的化学方程式_________ 。
II.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①Na2SO3溶液 ②浓硫酸 ③Na2S溶液 ④稀硫酸 ⑤酸性KMnO4溶液 ⑥品红溶液 ⑦铜片
(5)实验i选择的试剂是①和_____ (填序号),证明实现转化的现象是______ ,该转化利用了Na2SO3的_______ 性。
(6)实验ii实现了________ 价S向__________ 价S的转化。
(7)实验iii中发生反应的化学方程式是________ ,证明实现转化的现象是___________ 。
I.以下是硫元素形成物质的价类二维图及含硫物质相互转化的部分信息。

(1)B的化学式是
(2)C有毒,实验室可以用NaOH溶液吸收,反应的化学方程式是
(3)检验H中阴离子的实验操作及现象是
(4)C→D→E以及C→F→E都是造成酸雨的可能途径,请写出其中任意一条路径的化学方程式
II.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①Na2SO3溶液 ②浓硫酸 ③Na2S溶液 ④稀硫酸 ⑤酸性KMnO4溶液 ⑥品红溶液 ⑦铜片
| 实验序号 | 预期转化 | 选择试剂(填序号) | 证明实现转化的现象 |
| i | 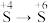 | ||
| ii | ①、③、④ | 淡黄色沉淀 | |
| iii |  | ②、⑦、⑥ |
(6)实验ii实现了
(7)实验iii中发生反应的化学方程式是
您最近一年使用:0次
2021-02-21更新
|
408次组卷
|
3卷引用:山西省榆次第一中学校2021-2022学年高一下学期期中线上测试化学试题
10 . 下述实验方案能达到实验目的的是
| 选项 | A | B | C | D |
| 方案 |  |  |  |  |
| 目的 | 收集乙烯并验证它与溴水发生加成反应 | 分离苯和CCl4 | 在强光照条件下制取纯净的一氯甲烷 | 实验室制备乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-02-19更新
|
1000次组卷
|
5卷引用:山西省晋中新大陆双语学校2021-2022学年高一下学期5月月考化学试题
山西省晋中新大陆双语学校2021-2022学年高一下学期5月月考化学试题(鲁科版2019)必修第二册 阶段性综合评估测试卷(二)(已下线)专题12 有机化学基础-备战2021届高考化学二轮复习题型专练福建省泉州科技中学2020-2021学年高一下学期期中考试化学试题广西钦州市第四中学2021-2022学年高一下学期5月月考化学试题



