1 . 运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为_______ ,该盐属于_____ (填“正盐”或“酸式盐”)。H3PO2易被氧化为 ,已知常温下
,已知常温下 的电离常数为
的电离常数为 ,
, ,
,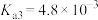 ,请利用以上数据计算推测
,请利用以上数据计算推测 溶液呈
溶液呈____ 性。
(2)常温下,用NaOH溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡______ (填“向左”“向右”或“不”)移动。试计算该溶液中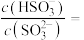
_______ (常温下, 的电离平衡常数
的电离平衡常数 ,
, )。
)。
(3)化工生产中常用FeS作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为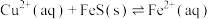
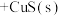 下列有关叙述正确的是_____。
下列有关叙述正确的是_____。
(1)已知
 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为 ,已知常温下
,已知常温下 的电离常数为
的电离常数为 ,
, ,
,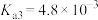 ,请利用以上数据计算推测
,请利用以上数据计算推测 溶液呈
溶液呈(2)常温下,用NaOH溶液吸收
 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡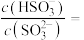
 的电离平衡常数
的电离平衡常数 ,
, )。
)。(3)化工生产中常用FeS作沉淀剂除去工业废水中的
 ,其反应原理为
,其反应原理为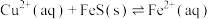
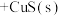 下列有关叙述正确的是_____。
下列有关叙述正确的是_____。A. |
B.达到平衡时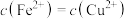 |
C.溶液中加入少量 固体后,溶液中 固体后,溶液中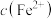 、 、 都减小 都减小 |
D.该反应平衡常数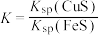 |
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组进行实验,探究影响 分解速率的因素。
分解速率的因素。
(1)该小组测量用10 mL 溶液制取150 mL
溶液制取150 mL  所需时间,下表是实验过程中记录的一组数据:
所需时间,下表是实验过程中记录的一组数据:
该小组在设计方案时,考虑了浓度和______ 、______ 等因素对过氧化氢分解速率的影响;从上述影响 分解速率的因素中任选一个,说明该因素对该反应速率的影响:
分解速率的因素中任选一个,说明该因素对该反应速率的影响:___________ 。
(2)将质量相同但颗粒大小不同的 分别加入5 mL 5%的
分别加入5 mL 5%的 溶液中,并用带火星的木条测试,结果如下:
溶液中,并用带火星的木条测试,结果如下:
写出 发生反应的化学方程式:
发生反应的化学方程式:______ 。实验结果说明,催化剂催化作用的大小还与_____ 有关。
(3)氨在国民经济中占有重要地位。合成氨工业中,
 的化学平衡常数表达式为
的化学平衡常数表达式为________ 。下图是合成氨反应平衡混合气中 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强。其中X代表的是
)、X分别代表温度或压强。其中X代表的是______ (填“温度”或“压强”)。
 分解速率的因素。
分解速率的因素。(1)该小组测量用10 mL
 溶液制取150 mL
溶液制取150 mL  所需时间,下表是实验过程中记录的一组数据:
所需时间,下表是实验过程中记录的一组数据:| 反应条件 | 时间/s | |||
30% 溶液 溶液 | 15% 溶液 溶液 | 10% 溶液 溶液 | 5% 溶液 溶液 | |
| (Ⅰ)无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| (Ⅱ)无催化剂、加热 | 360 | 480 | 540 | 720 |
(Ⅲ) 催化剂、加热 催化剂、加热 | 10 | 25 | 60 | 120 |
 分解速率的因素中任选一个,说明该因素对该反应速率的影响:
分解速率的因素中任选一个,说明该因素对该反应速率的影响:(2)将质量相同但颗粒大小不同的
 分别加入5 mL 5%的
分别加入5 mL 5%的 溶液中,并用带火星的木条测试,结果如下:
溶液中,并用带火星的木条测试,结果如下:催化剂( ) ) | 操作情况 | 观察结果 | 反应完成所需的时间/min |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30 |
 发生反应的化学方程式:
发生反应的化学方程式:(3)氨在国民经济中占有重要地位。合成氨工业中,

 的化学平衡常数表达式为
的化学平衡常数表达式为 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强。其中X代表的是
)、X分别代表温度或压强。其中X代表的是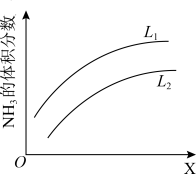
您最近一年使用:0次
解题方法
3 . 请填空:
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为______ ;B元素M能层p电子数为s电子数的一半,B的元素名称为______ 。
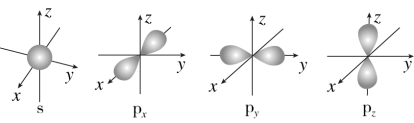
(2)下图是s能级和p能级的原子轨道图。____ 形,每个s能级有____ 个原子轨道;p电子的原子轨道呈____ 形,每个p能级有____ 个原子轨道。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为____ ,其基态原子的核外电子排布式为______ 。
(4)常温下,向100 mL 0.01 mol⋅L HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。_____ (填“强”或“弱”)酸。常温下一定浓度的MA稀溶液的 ,则a
,则a_____ (填“>”“<”或“=”)7,用离子方程式表示其原因:______ 。
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为
(2)下图是s能级和p能级的原子轨道图。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为
(4)常温下,向100 mL 0.01 mol⋅L
 HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。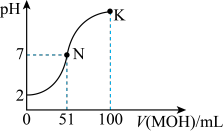
 ,则a
,则a
您最近一年使用:0次
解题方法
4 . 已知某原子结构示意图为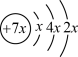 ,下列有关说法正确的是
,下列有关说法正确的是
A.原子结构示意图中 |
B.该原子的电子排布式为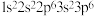 |
C.该原子的电子排布图为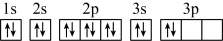 |
| D.该原子结构中共有5个能级上有电子 |
您最近一年使用:0次
解题方法
5 . 根据所学习的电化学知识,下列说法正确的是
| A.水库的钢闸门与电源正极连接可实现电化学保护 |
| B.铁表面的镀锌层破损后,就完全失去了对铁的保护作用 |
| C.酸雨后钢铁易发生析氢腐蚀、铁锅存留盐液时易发生吸氧腐蚀 |
| D.智能手机常用的锂离子电池属于一次电池 |
您最近一年使用:0次
解题方法
6 . 某温度下反应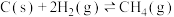 的
的 ,当各气体物质的量浓度分别为
,当各气体物质的量浓度分别为 mol·L
mol·L 、
、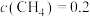 mol·L
mol·L 时,上述反应
时,上述反应
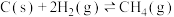 的
的 ,当各气体物质的量浓度分别为
,当各气体物质的量浓度分别为 mol·L
mol·L 、
、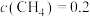 mol·L
mol·L 时,上述反应
时,上述反应| A.缺条件,无法判断 | B.逆向进行 |
| C.达到平衡状态 | D.正向进行 |
您最近一年使用:0次
7 . 下列热化学方程式中, 能正确表示物质的燃烧热的是
能正确表示物质的燃烧热的是
 能正确表示物质的燃烧热的是
能正确表示物质的燃烧热的是A.  kJ⋅mol kJ⋅mol |
B.  kJ·mol kJ·mol |
C.  kJ⋅mol kJ⋅mol |
D.  kJ·mol kJ·mol |
您最近一年使用:0次
解题方法
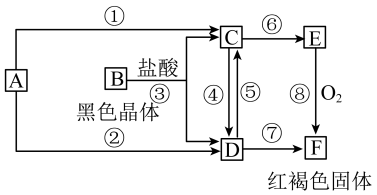
8 . 已知A为常见的金属单质,根据下图所示的关系:___________ ,B为___________ ,C为___________ ,D为___________ ,E为___________ ,F为___________ 。
(2)写出④⑤的离子方程式,⑧的化学方程式。
④___________ ,
⑤___________ ,
⑧___________ 。
(2)写出④⑤的离子方程式,⑧的化学方程式。
④
⑤
⑧
您最近一年使用:0次
解题方法
9 . 在用NaCl固体配制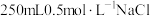 溶液的实验中,不需要使用的仪器是
溶液的实验中,不需要使用的仪器是
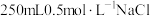 溶液的实验中,不需要使用的仪器是
溶液的实验中,不需要使用的仪器是A. | B. |
C. | D. |
您最近一年使用:0次
10 . 下列说法正确的是
A. 的质量是14g 的质量是14g | B.NaOH的摩尔质量是40g |
C. 的摩尔质量是18g/mol 的摩尔质量是18g/mol | D.1molHCl的质量是36.5g/mol |
您最近一年使用:0次



