1 . 下列说法正确的是
A. 的质量是14g 的质量是14g | B.NaOH的摩尔质量是40g |
C. 的摩尔质量是18g/mol 的摩尔质量是18g/mol | D.1molHCl的质量是36.5g/mol |
您最近一年使用:0次
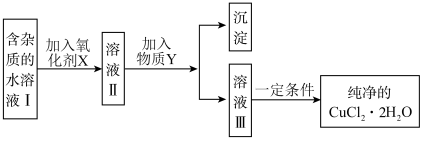
2 . 已知 H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2∙2H2O),为制取纯净的CuCl2∙2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
(1)本实验最适合的氧化剂X是___________(填序号)。
(2)物质Y可以选择以下___________。
(3)本实验用加碱沉淀法能不能达到目的?___________ (填“能”或“不能”)。
(4)加氧化剂的目的是___________ 。
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?___________ 。
(1)本实验最适合的氧化剂X是___________(填序号)。
| A.K2Cr2O7 | B.NaClO | C. H2O2 | D.KMnO4 |
(2)物质Y可以选择以下___________。
| A.CuO | B.CuSO4 | C.Cu(OH)2 | D.KOH |
(3)本实验用加碱沉淀法能不能达到目的?
(4)加氧化剂的目的是
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?
您最近一年使用:0次
解题方法
3 . 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是___________ (填“强酸”或“弱酸”)。
(2)②组情况表明,c___________ (填“大于”、“小于”或“等于”)0.2mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是:c(A-)___________ c(Na+) (“大于”、“小于”或“等于”)。
(3)从③组实验结果分析,说明HA的电离程度___________ (填“大于”、“小于”或“等于”)NaA的水解程度。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=___________ mol∙L-1。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的 pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是
(2)②组情况表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
4 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中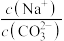
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中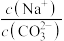
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次
解题方法
5 . 回答下列问题。
(1)在某温度下,向含有AgCl固体的AgCl饱和溶液中通入少量HCl,则AgCl的溶解度___________ (填“增大”“减小”或“不变”,下同),Ksp___________ ,c(Ag+)___________ 。
(2)在25℃时对氨水进行如下操作,若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的pH___________ 7(“大于”、“小于”或“等于”);若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中 =amol/L,则
=amol/L,则 =
=___________ 。
(3)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的___________ 极相连,铁制品应与电源的___________ 极相连。电镀过程中硫酸镍溶液中溶质的浓度会___________ (填“增大”“减小”或“不变”)。
(1)在某温度下,向含有AgCl固体的AgCl饱和溶液中通入少量HCl,则AgCl的溶解度
(2)在25℃时对氨水进行如下操作,若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的pH
 =amol/L,则
=amol/L,则 =
=(3)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的
您最近一年使用:0次
解题方法
6 . 利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯。下列叙述中正确的是
| A.电解时以精铜作阳极 |
B.电解时阴极上发生的反应为 |
C.粗铜连接电源的负极,其电极反应为 |
| D.电解后,电解槽底部会形成含有少量Ag、Pt等金属的阳极泥 |
您最近一年使用:0次
解题方法
7 . 蛟龙号载人潜水器由我国自行设计、自主集成研制,是目前世界上下潜能力最强的作业型载人潜水器。给某潜水器提供动力的电池如图所示。下列有关说法正确的是
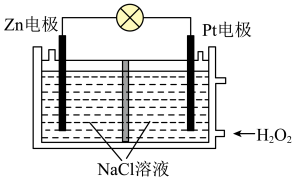
| A.Zn电极发生了还原反应 |
| B.电子从Zn电极沿导线流向Pt电极,再经溶液回到Zn电极 |
C.电池中的 向Pt电极移动 向Pt电极移动 |
D.Pt电极反应式为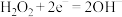 |
您最近一年使用:0次
8 . 下列说法正确的是
A.为抑制 的水解,较好地保存 的水解,较好地保存 溶液,应加少量盐酸 溶液,应加少量盐酸 |
B.配制 溶液时,将 溶液时,将 固体溶于稀盐酸中,然后稀释至所需浓度 固体溶于稀盐酸中,然后稀释至所需浓度 |
C.用加热的方法可以除去KCl溶液中的 |
D.将 溶液和 溶液和 溶液分别加热、蒸干、灼烧,所得固体成分相同 溶液分别加热、蒸干、灼烧,所得固体成分相同 |
您最近一年使用:0次
9 . 下列说法中正确的是
| A.在100℃时,pH约为6的纯水呈酸性 |
B.将1mL 盐酸稀释至1000mL,所得溶液的pH为9 盐酸稀释至1000mL,所得溶液的pH为9 |
C.在常温下,当水电离出的 为 为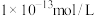 时,此溶液的pH可能为1或13 时,此溶液的pH可能为1或13 |
| D.将pH=2的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸的pH略大 |
您最近一年使用:0次
10 . 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+: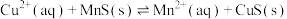 ,下列说法正确的是
,下列说法正确的是
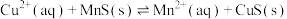 ,下列说法正确的是
,下列说法正确的是A.相同温度时,MnS的 比CuS的 比CuS的 小 小 |
B.该反应达到平衡时 |
C.设该反应的平衡常数为K,则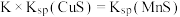 |
D.向平衡体系中加入少量 固体后, 固体后, 减小, 减小, 增大 增大 |
您最近一年使用:0次



