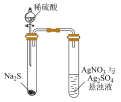
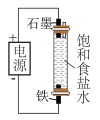
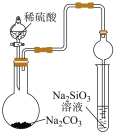
1 . 下列实验操作正确且能达到实验目的的是
|
|
A.制备 | B.验证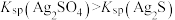 |
|
|
C.制备少量含 的消毒液 的消毒液 | D.证明非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . “宏观辨识与微观探析”是化学学科核心素养之一,已知:① 和
和 互为同素异形体,臭氧分子极性较小,利用臭氧的强氧化性可在
互为同素异形体,臭氧分子极性较小,利用臭氧的强氧化性可在 约为8时,与废水中
约为8时,与废水中 反应生成
反应生成 和两种气体;②氨水、氧化锌悬浊液等均可以吸收废气中的
和两种气体;②氨水、氧化锌悬浊液等均可以吸收废气中的 。下列离子方程式正确且符合题意的是
。下列离子方程式正确且符合题意的是
 和
和 互为同素异形体,臭氧分子极性较小,利用臭氧的强氧化性可在
互为同素异形体,臭氧分子极性较小,利用臭氧的强氧化性可在 约为8时,与废水中
约为8时,与废水中 反应生成
反应生成 和两种气体;②氨水、氧化锌悬浊液等均可以吸收废气中的
和两种气体;②氨水、氧化锌悬浊液等均可以吸收废气中的 。下列离子方程式正确且符合题意的是
。下列离子方程式正确且符合题意的是A.臭氧去除废水中 : :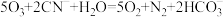 |
B.少量 通入到氧化锌悬浊液: 通入到氧化锌悬浊液: |
C.少量硫化氢气体通入到硫酸亚铁溶液: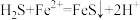 |
D.向苯酚钠溶液中通入少量 : :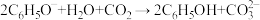 |
您最近一年使用:0次
名校
解题方法
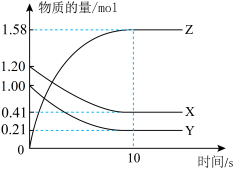
3 . 一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:____________ 。
(2)反应开始到10 s间,用Z表示的反应速率v(Z)=____________ 。
(3)反应开始到10 s时,Y的转化率=___________ (转化率是指某反应物转化的物质的量与该反应物的起始物质的量的百分比)。
(2)反应开始到10 s间,用Z表示的反应速率v(Z)=
(3)反应开始到10 s时,Y的转化率=
您最近一年使用:0次
名校
解题方法
4 . 用Cu+2Ag+ =2Ag + Cu2+反应,设计一个原电池。
(1)正极材料选用:___________ 电极反应式为:_______________
(2)电子由___________ 通过导线流向___________ 。(填材料名称)
(3)溶液中的H+向___________ 移动
(4)导线上有0.2mole-通过时,负极质量减少____________ g
(5)请画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向____________ 。
(1)正极材料选用:
(2)电子由
(3)溶液中的H+向
(4)导线上有0.2mole-通过时,负极质量减少
(5)请画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向
您最近一年使用:0次
名校
5 . 氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。回答下列问题:___________ ;B中圆底烧瓶收集氨气时,请你选择氨气的进气口___________ (填“a”或“b”)。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显___________ 性。
(3)NO2与水反应的化学方程式___________ ,其中氧化剂与还原剂的物质的量之比是___________ 。
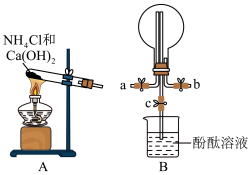
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显
(3)NO2与水反应的化学方程式
您最近一年使用:0次
6 . 已知二氧化硫可使酸性高锰酸钾溶液褪色,化学反应方程式为:5SO2 + 2KMnO4 + 2H2O=K2SO4+ 2MnSO4 + 2H2SO4
用下图装置来验证浓硫酸与木炭在加热条件下反应后的非水产物______________
(2)实验时,反应产生的气体应从_____ 端通入;从_____ 端连接盛有澄清石灰水的实验装置(用 “a”或“b” 填空)。
(3)A瓶的实验现象是______________ 。
(4)C瓶溶液的作用是_____________ 。
用下图装置来验证浓硫酸与木炭在加热条件下反应后的非水产物
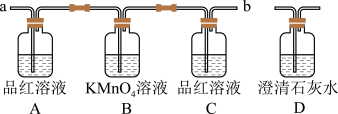
(2)实验时,反应产生的气体应从
(3)A瓶的实验现象是
(4)C瓶溶液的作用是
您最近一年使用:0次
名校
解题方法
7 . 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和2 mol/L硫酸设计实验方案来研究影响反应速率的因素。请完成下列实验报告:
该小组的实验目的是研究反应物本身的______ 对反应速率的影响。
| 实验内容 | 实验现象 | 结论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢:Mg | 反应物的性质越 |
您最近一年使用:0次
名校
8 . 一定温度下,在2L密闭容器中发生可逆反应CO(g)+H2O(g) CO2(g)+H2(g),5s内消耗的CO的物质的量为2mol,则用H2表示的该反应速率是
CO2(g)+H2(g),5s内消耗的CO的物质的量为2mol,则用H2表示的该反应速率是
 CO2(g)+H2(g),5s内消耗的CO的物质的量为2mol,则用H2表示的该反应速率是
CO2(g)+H2(g),5s内消耗的CO的物质的量为2mol,则用H2表示的该反应速率是| A.0.4mol/(L·S) | B.2mol/(L·S) |
| C.0.2mol/(L·S) | D.0.2mol/(L·min) |
您最近一年使用:0次
名校
9 . 铜锌原电池的装置如图所示,下列叙述错误的是
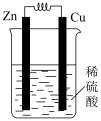
| A.锌片逐渐溶解,质量减轻 |
| B.锌片为负极, 铜片为正极 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置可以将化学能转化为电能 |
您最近一年使用:0次
名校
解题方法
10 . 有关反应 N2+3H2 2NH3的说法正确的是
2NH3的说法正确的是
 2NH3的说法正确的是
2NH3的说法正确的是| A.升高温度可减慢反应速率 | B.使用催化剂可提高反应速率 |
| C.达到平衡时,N2的v(正)=v(逆)=0 | D.达到平衡时 H2 转化率可达 100% |
您最近一年使用:0次