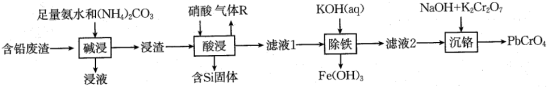
1 . 铬酸铅(PbCrO4)又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是PbSO4和ZnO,还含Fe3O4、SiO2等)为原料制备铬酸铅的流程如下:
②常温下,几种难溶电解质的溶度积如下:
回答下列问题:
(1)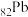 位于周期表第
位于周期表第___________ 周期___________ 族,PbCrO4中Cr的化合价为___________ 。
(2)“碱浸”中PbSO4转化反应的离子方程式为___________ 。
(3)已知:“酸浸”中6.3gHNO3作氧化剂时转移0.3mol电子。气体R在空气中的颜色变化为___________ 。
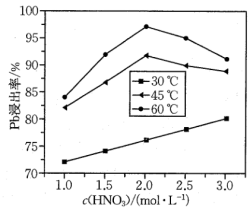
(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为___________ 。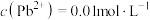 ,“除铁”中控制pH范围为
,“除铁”中控制pH范围为___________ 。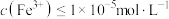 ,则表明Fe3+已完全沉淀。
,则表明Fe3+已完全沉淀。
(6)“沉铬”中生成PbCrO4反应的离子方程式为___________ 。
②常温下,几种难溶电解质的溶度积如下:
| 电解质 | PbCO3 | PbSO4 | PbCrO4 | Pb(OH)2 | Fe(OH)3 |
 | 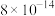 |  | 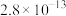 | 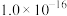 | 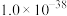 |
(1)
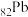 位于周期表第
位于周期表第(2)“碱浸”中PbSO4转化反应的离子方程式为
(3)已知:“酸浸”中6.3gHNO3作氧化剂时转移0.3mol电子。气体R在空气中的颜色变化为
(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为
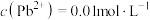 ,“除铁”中控制pH范围为
,“除铁”中控制pH范围为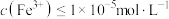 ,则表明Fe3+已完全沉淀。
,则表明Fe3+已完全沉淀。(6)“沉铬”中生成PbCrO4反应的离子方程式为
您最近一年使用:0次
2024-05-18更新
|
81次组卷
|
2卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
名校
2 . X、Y、Z、W为原子序数依次增大且互不相邻的四种短周期主族元素,X为元素周期表中原子半径最小的元素,X与W同主族,Y、Z的最外层电子数之和与W的核外电子总数相等。下列说法错误的是
| A.简单离子半径:Z>W | B.仅由X、Y形成的化合物不止一种 |
| C.Y、Z的最高价氧化物对应的水化物均为弱酸 | D.化合物WZ为离子化合物 |
您最近一年使用:0次
2024-05-18更新
|
101次组卷
|
2卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
3 . 我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是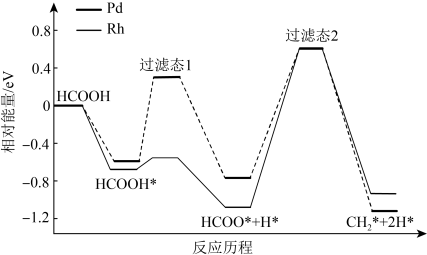
| A.参与反应的反应物总键能小于生成物总键能 |
B.Pd和Rh分别作催化剂时HCOOH分解产生 的 的 不同 不同 |
| C.HCOOH吸附在催化剂表面是一个放热过程 |
D. 是该历程的决速步骤 是该历程的决速步骤 |
您最近一年使用:0次
2024-05-17更新
|
251次组卷
|
2卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
名校
解题方法
4 . 太阳能光电催化-化学耦合分解 的装置如图所示。下列说法不正确的是
的装置如图所示。下列说法不正确的是
 的装置如图所示。下列说法不正确的是
的装置如图所示。下列说法不正确的是
| A.利用太阳能光进行电催化可以节约能源并产生清洁能源 |
| B.若接铅蓄电池进行电解,b极接Pb电极 |
C.a极的电极反应为: |
D.理论上每生成 氢气则消耗 氢气则消耗 |
您最近一年使用:0次
名校
解题方法
5 . 研究发现,以非晶态Ni( )基硫化物为催化剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理和反应机理如图所示:
)基硫化物为催化剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理和反应机理如图所示:
 )基硫化物为催化剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理和反应机理如图所示:
)基硫化物为催化剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理和反应机理如图所示:
| A.产生5.6L O2,电路中转移的电子数为2NA |
B.电极A的反应为 ,电极A附近溶液的碱性增强 ,电极A附近溶液的碱性增强 |
| C.UOR分两步进行,其中没有非极性键的形成或断裂 |
| D.若将光伏电池改为铅蓄电池,电解过程中电极B应连接铅蓄电池的Pb极 |
您最近一年使用:0次
2024-05-15更新
|
151次组卷
|
2卷引用:2024届宁夏石嘴山市大武口区石嘴山市第三中学高三下学期三模考试理综试题-高中化学
名校
解题方法
6 . 铬是人体内微量元素之一,是重要的血糖调节剂。
(1)铬在元素周期表中的位置为___________ ,其基态原子核外电子占据的原子轨道数为___________ 。
(2)已知 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。
①该配合物中提供孤电子对形成配位键的原子是___________ 。
②配体中中心原子的杂化方式为___________ (填字母)。
a. b.
b. c.sp d.
c.sp d.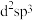
③该物质中, 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是___________ 。
(3)钛铬合金是一种高温结构材料,第二电离能
___________ (填“ ”或“
”或“ ”)
”)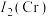 ,原因是
,原因是___________ 。
(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为 ,则B点分数坐标为
,则B点分数坐标为___________ ,已知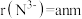 ,
,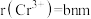 ,则AB间距离为
,则AB间距离为___________ nm。
(1)铬在元素周期表中的位置为
(2)已知
 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。①该配合物中提供孤电子对形成配位键的原子是
②配体中中心原子的杂化方式为
a.
 b.
b. c.sp d.
c.sp d.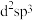
③该物质中,
 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是(3)钛铬合金是一种高温结构材料,第二电离能

 ”或“
”或“ ”)
”)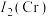 ,原因是
,原因是(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为
 ,则B点分数坐标为
,则B点分数坐标为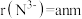 ,
,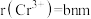 ,则AB间距离为
,则AB间距离为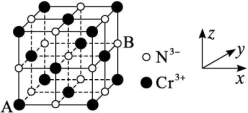
您最近一年使用:0次
名校
解题方法
7 . 氟他胺是一种可用于治疗肿瘤的药物,其分子结构如图所示,关于氟他胺,下列说法正确的是
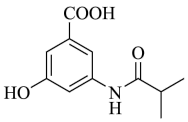
A.分子式为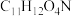 |
| B.一定条件下可以发生加成、取代、氧化等反应 |
| C.所有碳原子可能处于同一个平面上 |
D. 氟他胺最多能与 氟他胺最多能与 反应 反应 |
您最近一年使用:0次
解题方法
8 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为___________ ; 键角
键角___________ 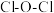 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。
(3)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体,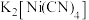 是红黄色单斜晶体。
是红黄色单斜晶体。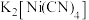 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: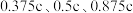 。晶胞中氢键的长度为
。晶胞中氢键的长度为___________  (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(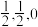 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为___________ ,该缺陷晶型的化学式可表示为___________ 。设阿伏加德罗常数的值为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为___________  (列出表达式)。
(列出表达式)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.  B.
B.
C. D.
D.
 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为 键角
键角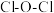 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。(3)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体,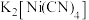 是红黄色单斜晶体。
是红黄色单斜晶体。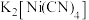 的熔点高于
的熔点高于 的原因是
的原因是(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数
 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: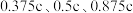 。晶胞中氢键的长度为
。晶胞中氢键的长度为 (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。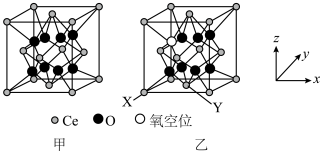
 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(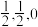 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解题方法
9 . 锌在冶金、化学电源等方面具有重要作用,是一种应用广泛的金属。以闪锌矿(主要成分为 ,还含有
,还含有 和少量
和少量 杂质)为原料,制备金属锌的流程如图所示:
杂质)为原料,制备金属锌的流程如图所示:
(1)焙烧过程排放烟气中含有大量的 ,直接排放会污染空气,可用氧化锌吸收法除去。配制
,直接排放会污染空气,可用氧化锌吸收法除去。配制 悬浊液(含少量
悬浊液(含少量 、
、 ),在吸收塔中封闭循环脱硫,发生的主要反应为
),在吸收塔中封闭循环脱硫,发生的主要反应为 ,该反应常温下能自发进行的原因是
,该反应常温下能自发进行的原因是___________ 。
(2)用稀硫酸完全溶浸后,溶液中各离子浓度如下表
①“氧化除杂”工序中发生反应的离子方程式___________ 。
②常温下,有关离子沉淀的 如下表所示(当离子浓度为
如下表所示(当离子浓度为 时认为沉淀完全):
时认为沉淀完全):
则
___________ ,“氧化”后调 的范围是
的范围是___________ 。
(3)溶液中的
___________ (填“能”或“不能”)直接在“氧化除杂”步骤中除去,其原因是___________ 。
(4)电解硫酸锌溶液制备单质锌时,电解总方程式为___________ ;沉积锌后的电解液可返回___________ 工序继续使用。
(5)下列金属冶炼的方法与本工艺电解冶炼锌方法相似的是___________。
 ,还含有
,还含有 和少量
和少量 杂质)为原料,制备金属锌的流程如图所示:
杂质)为原料,制备金属锌的流程如图所示: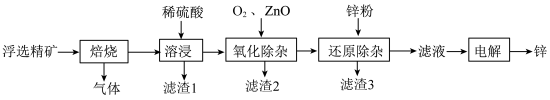
(1)焙烧过程排放烟气中含有大量的
 ,直接排放会污染空气,可用氧化锌吸收法除去。配制
,直接排放会污染空气,可用氧化锌吸收法除去。配制 悬浊液(含少量
悬浊液(含少量 、
、 ),在吸收塔中封闭循环脱硫,发生的主要反应为
),在吸收塔中封闭循环脱硫,发生的主要反应为 ,该反应常温下能自发进行的原因是
,该反应常温下能自发进行的原因是(2)用稀硫酸完全溶浸后,溶液中各离子浓度如下表
| 金属离子 |  |  |  |  |
浓度( ) ) | 1.0 | 0.01 | 1.0 | 0.01 |
②常温下,有关离子沉淀的
 如下表所示(当离子浓度为
如下表所示(当离子浓度为 时认为沉淀完全):
时认为沉淀完全): |  |  | |
开始沉淀 | 2.3 | 6.2 | 7.4 |
沉淀完全 | x | 8.7 | 9.4 |

 的范围是
的范围是(3)溶液中的

(4)电解硫酸锌溶液制备单质锌时,电解总方程式为
(5)下列金属冶炼的方法与本工艺电解冶炼锌方法相似的是___________。
| A.电解熔融的氯化钠制钠 | B.电解熔融的氯化镁制镁 |
| C.电解熔融的氧化铝制铝 | D.电镀硫酸铜废水回收金属铜 |
您最近一年使用:0次
解题方法
10 . 一种以磷铁渣(主要含 ,以及少量
,以及少量 、
、 等杂质)、
等杂质)、 为原料制备磷酸锰
为原料制备磷酸锰 的实验过程如下:
的实验过程如下:
(1)溶解。将一定量的磷铁渣加入如图所示装置的三颈烧瓶中,维持温度60℃,边搅拌边向三颈烧瓶中加入一定量的硫酸和 溶液,反应后有
溶液,反应后有 、
、 和
和 生成。反应后过滤。
生成。反应后过滤。 反应的离子方程式:
反应的离子方程式:___________ 。
②实验中当观察到某种现象时可不再加入 溶液,该现象是:
溶液,该现象是:___________ 。
③ 难溶于水,反应
难溶于水,反应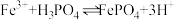 的平衡常数为
的平衡常数为___________ 。[已知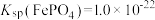 ,
, 的电离平衡常数
的电离平衡常数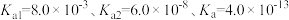 ]。
]。
④实验中需不断补充稀硫酸控制溶液的 。
。 过大会降低
过大会降低 的浸出率和消耗过多的
的浸出率和消耗过多的 ,原因是
,原因是___________ 。
(2)除铁。向所得滤液中加入萃取剂(由磷酸酯和煤油混合而成,磷酸酯易溶于煤油,难溶于水)萃取溶液中的 。萃取结束后取有机层,经过反萃取操作,可回收萃取剂重复使用。已知萃取剂中磷酸酯(用
。萃取结束后取有机层,经过反萃取操作,可回收萃取剂重复使用。已知萃取剂中磷酸酯(用 表示)萃取溶液中
表示)萃取溶液中 时发生如下反应:
时发生如下反应: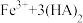 (有机层)
(有机层)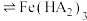 (有机层)
(有机层) ,反萃取回收萃取剂的方法是
,反萃取回收萃取剂的方法是___________ 。
(3)制 。由萃取后所得水层中
。由萃取后所得水层中 、
、 制纯净
制纯净 固体的实验方案,请补充完整:取萃取后所得水层溶液
固体的实验方案,请补充完整:取萃取后所得水层溶液 [其中
[其中 ],向其中滴加
],向其中滴加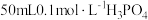 ,再滴加
,再滴加 溶液,至溶液
溶液,至溶液
___________ ,过滤,洗涤沉淀至最后一次洗涤滤液中加入盐酸和 溶液
溶液___________ ,后干燥沉淀,得 固体。(已知溶液的
固体。(已知溶液的 对所得沉淀中锰磷比
对所得沉淀中锰磷比 和
和 的沉淀率影响如图所示。)
的沉淀率影响如图所示。)
 ,以及少量
,以及少量 、
、 等杂质)、
等杂质)、 为原料制备磷酸锰
为原料制备磷酸锰 的实验过程如下:
的实验过程如下:(1)溶解。将一定量的磷铁渣加入如图所示装置的三颈烧瓶中,维持温度60℃,边搅拌边向三颈烧瓶中加入一定量的硫酸和
 溶液,反应后有
溶液,反应后有 、
、 和
和 生成。反应后过滤。
生成。反应后过滤。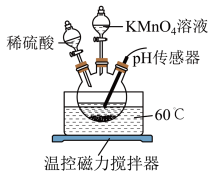
 反应的离子方程式:
反应的离子方程式:②实验中当观察到某种现象时可不再加入
 溶液,该现象是:
溶液,该现象是:③
 难溶于水,反应
难溶于水,反应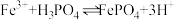 的平衡常数为
的平衡常数为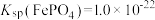 ,
, 的电离平衡常数
的电离平衡常数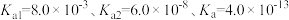 ]。
]。④实验中需不断补充稀硫酸控制溶液的
 。
。 过大会降低
过大会降低 的浸出率和消耗过多的
的浸出率和消耗过多的 ,原因是
,原因是(2)除铁。向所得滤液中加入萃取剂(由磷酸酯和煤油混合而成,磷酸酯易溶于煤油,难溶于水)萃取溶液中的
 。萃取结束后取有机层,经过反萃取操作,可回收萃取剂重复使用。已知萃取剂中磷酸酯(用
。萃取结束后取有机层,经过反萃取操作,可回收萃取剂重复使用。已知萃取剂中磷酸酯(用 表示)萃取溶液中
表示)萃取溶液中 时发生如下反应:
时发生如下反应: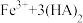 (有机层)
(有机层)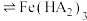 (有机层)
(有机层) ,反萃取回收萃取剂的方法是
,反萃取回收萃取剂的方法是(3)制
 。由萃取后所得水层中
。由萃取后所得水层中 、
、 制纯净
制纯净 固体的实验方案,请补充完整:取萃取后所得水层溶液
固体的实验方案,请补充完整:取萃取后所得水层溶液 [其中
[其中 ],向其中滴加
],向其中滴加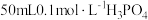 ,再滴加
,再滴加 溶液,至溶液
溶液,至溶液
 溶液
溶液 固体。(已知溶液的
固体。(已知溶液的 对所得沉淀中锰磷比
对所得沉淀中锰磷比 和
和 的沉淀率影响如图所示。)
的沉淀率影响如图所示。)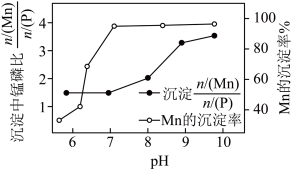
您最近一年使用:0次



