名校
1 . 硼、氮、铁、钴、镍等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
(2)硼酸( )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在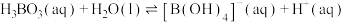 的平衡,回答下列问题。
的平衡,回答下列问题。__________ 。
②下列关于硼酸的说法正确的是__________ (填序号)。
a. 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
c.硼酸分子的稳定性与氢键有关 d.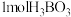 晶体中有
晶体中有 氢键
氢键
(3)叠氮化合物在化工上有重要应用, 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式__________ (写出一种即可),其立体构型为__________ 。
(4) 的结构如图所示,
的结构如图所示, 中
中 、
、 、
、 由大到小的顺序是
由大到小的顺序是____________________ 。 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于__________ 位置。
①从该晶胞中能分割出来的结构图有_______ (填标号)。 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有__________ 个,该距离为__________ pm(仅列式不计算)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
A.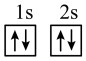 | B. |
C.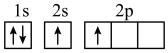 | D.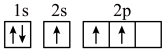 |
(2)硼酸(
 )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在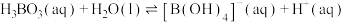 的平衡,回答下列问题。
的平衡,回答下列问题。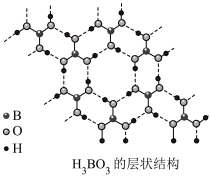
②下列关于硼酸的说法正确的是
a.
 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制c.硼酸分子的稳定性与氢键有关 d.
 晶体中有
晶体中有 氢键
氢键(3)叠氮化合物在化工上有重要应用,
 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(4)
 的结构如图所示,
的结构如图所示, 中
中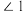 、
、 、
、 由大到小的顺序是
由大到小的顺序是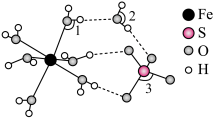
 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于
①从该晶胞中能分割出来的结构图有
a.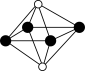 b.
b.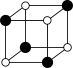 c.
c.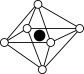 d.
d. e.
e.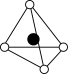
 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
您最近一年使用:0次
名校
2 . A、B、M是生活中最常见的前四周期金属元素,A元素的单质既可与强酸反应也可与强碱反应,B位于周期表的第八纵行,其+3价离子比+2价离子在水溶液中稳定,M原子的价电子排布为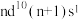 。回答下列问题:
。回答下列问题:
(1) 的价电子排布式为
的价电子排布式为___________ 。
(2) 为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。
为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。 更接近于
更接近于___________ (填晶体类型)。下列说法错误的是___________ (填标号)。 中B的化合价为0
中B的化合价为0
B.配体与B原子所形成的配位键的键能相同
C.B在周期表中位于VIII族,属于d区元素
D.制备 应在隔绝空气的条件下进行
应在隔绝空气的条件下进行
(3) 中存在的
中存在的 键有
键有___________ mol。 具有对称的空间结构,其中2个
具有对称的空间结构,其中2个 分别被
分别被 取代能得到两种不同结构的
取代能得到两种不同结构的 ,则
,则 中由4个
中由4个 围成的图形是
围成的图形是___________ 。
(4)金属A与M可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示(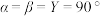 ),图乙为晶胞在z轴方向的投影。
),图乙为晶胞在z轴方向的投影。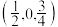 ,则b点原子的分数坐标为
,则b点原子的分数坐标为___________ 。
②该晶体的密度为___________  (用含NA的计算式回答)。
(用含NA的计算式回答)。
(5) 能与
能与 、
、 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为___________ 。
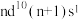 。回答下列问题:
。回答下列问题:(1)
 的价电子排布式为
的价电子排布式为(2)
 为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。
为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。 更接近于
更接近于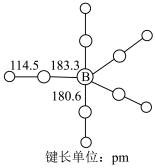
 中B的化合价为0
中B的化合价为0B.配体与B原子所形成的配位键的键能相同
C.B在周期表中位于VIII族,属于d区元素
D.制备
 应在隔绝空气的条件下进行
应在隔绝空气的条件下进行(3)
 中存在的
中存在的 键有
键有 具有对称的空间结构,其中2个
具有对称的空间结构,其中2个 分别被
分别被 取代能得到两种不同结构的
取代能得到两种不同结构的 ,则
,则 中由4个
中由4个 围成的图形是
围成的图形是(4)金属A与M可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示(
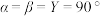 ),图乙为晶胞在z轴方向的投影。
),图乙为晶胞在z轴方向的投影。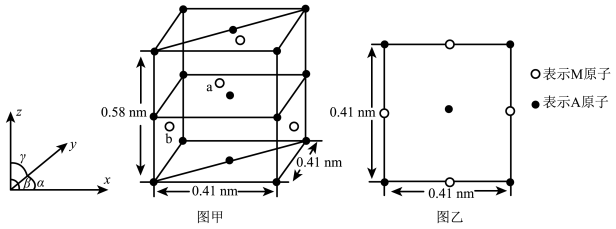
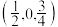 ,则b点原子的分数坐标为
,则b点原子的分数坐标为②该晶体的密度为
 (用含NA的计算式回答)。
(用含NA的计算式回答)。(5)
 能与
能与 、
、 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
您最近一年使用:0次
名校
3 . 下表是元素周期表的一部分,其中所列数字分别代表某一元素
(1)表中属于d区的元素是___________ (填编号)。
(2)⑤⑥⑦三种元素中电负性最大的是___________ (填写元素符号),在第二周期中第一电离能介于②和③之间的元素有___________ 种。
(3)元素⑨在周期表中的位置___________ 。
(4)元素⑧和⑦能形成一种常见的干燥剂,它的电子式为___________ 。
(5)⑥和⑦相比较,非金属性较弱的是___________ (填元素符号),可以验证你的结论的是下列中的___________ (填编号)。
A.气态氢化物的稳定性 B.两元素的电负性 C.含氧酸的酸性 D.最高化合价
(6)①与③的元素形成的10电子中性分子X的空间构型为___________ ,它极易溶于水中,请简要说明该物质易溶于水的原因___________ 。

(1)表中属于d区的元素是
(2)⑤⑥⑦三种元素中电负性最大的是
(3)元素⑨在周期表中的位置
(4)元素⑧和⑦能形成一种常见的干燥剂,它的电子式为
(5)⑥和⑦相比较,非金属性较弱的是
A.气态氢化物的稳定性 B.两元素的电负性 C.含氧酸的酸性 D.最高化合价
(6)①与③的元素形成的10电子中性分子X的空间构型为
您最近一年使用:0次
名校
4 . 下列说法不正确的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶规律解释 |
B.乳酸分子(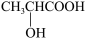 )中含有一个手性碳原子 )中含有一个手性碳原子 |
| C.亚硝酰氟(NOF)的空间构型为V形 |
D.键角大小: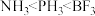 |
您最近一年使用:0次
名校
5 . 某种废弃电子元器件的主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 等,实验室中以其为原料提取金属
等,实验室中以其为原料提取金属 和胆矾的工艺流程如图。
和胆矾的工艺流程如图。 如表。
如表。
回答下列问题:
(1)基态 、
、 原子核外未成对电子数之比为
原子核外未成对电子数之比为_______ 。
(2) 为两性氧化物,
为两性氧化物, 在“碱浸”时发生反应的离子方程式为
在“碱浸”时发生反应的离子方程式为_______ 。
(3)滤渣2的主要成分为_______ , 中心原子的杂化方式是
中心原子的杂化方式是_______ 。
(4)“氧化”时 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)加试剂X调 可得
可得 沉淀和滤液2,则所加试剂X为
沉淀和滤液2,则所加试剂X为_______ ,所调 的范围为
的范围为_______ 。
(6)请你以 、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:
、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:_______ 。
可以不写满也可以自己划线继续补充:
①_______,
②_______,
③_______,
④_______,
⑤_______。
 、
、 ,还含有少量的
,还含有少量的 、
、 等,实验室中以其为原料提取金属
等,实验室中以其为原料提取金属 和胆矾的工艺流程如图。
和胆矾的工艺流程如图。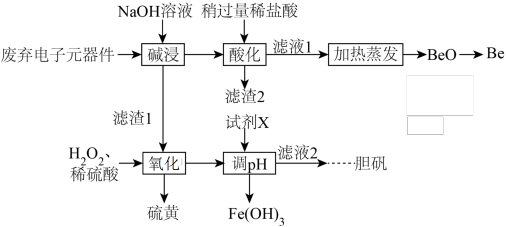
 如表。
如表。| 金属阳离子 |  |  |  |
开始沉淀的 | 2.2 | 5.8 | 4.2 |
沉淀完全的 | 3.2 | 8.8 | 7.7 |
(1)基态
 、
、 原子核外未成对电子数之比为
原子核外未成对电子数之比为(2)
 为两性氧化物,
为两性氧化物, 在“碱浸”时发生反应的离子方程式为
在“碱浸”时发生反应的离子方程式为(3)滤渣2的主要成分为
 中心原子的杂化方式是
中心原子的杂化方式是(4)“氧化”时
 发生反应的离子方程式为
发生反应的离子方程式为(5)加试剂X调
 可得
可得 沉淀和滤液2,则所加试剂X为
沉淀和滤液2,则所加试剂X为 的范围为
的范围为(6)请你以
 、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:
、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:可以不写满也可以自己划线继续补充:
①_______,
②_______,
③_______,
④_______,
⑤_______。
您最近一年使用:0次
名校
6 . 下图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。 分子的结构式为
分子的结构式为_______________ 。
(2)吸收装置中,发生的反应为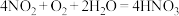 ,若用
,若用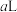
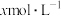 的稀硝酸作为吸收液,反应后得到
的稀硝酸作为吸收液,反应后得到
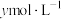 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为_______  。
。
(3)实验室常用 溶液吸收
溶液吸收 (
( 和
和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知
(已知 不能与
不能与 溶液反应,不考虑
溶液反应,不考虑 与
与 的转化)。
的转化)。
①若 能被
能被 溶液完全吸收,则
溶液完全吸收,则 的取值范围为
的取值范围为_______________ 。
②若
 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为_________  (标准状况下)。
(标准状况下)。
(4) 催化还原氯氧化物技术(
催化还原氯氧化物技术( )是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的
)是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为_______________ 。
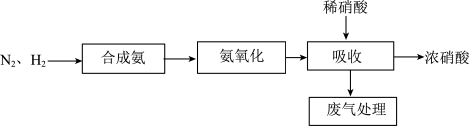
 分子的结构式为
分子的结构式为(2)吸收装置中,发生的反应为
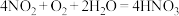 ,若用
,若用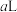
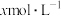 的稀硝酸作为吸收液,反应后得到
的稀硝酸作为吸收液,反应后得到
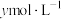 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为 。
。(3)实验室常用
 溶液吸收
溶液吸收 (
( 和
和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知
(已知 不能与
不能与 溶液反应,不考虑
溶液反应,不考虑 与
与 的转化)。
的转化)。①若
 能被
能被 溶液完全吸收,则
溶液完全吸收,则 的取值范围为
的取值范围为②若

 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为 (标准状况下)。
(标准状况下)。(4)
 催化还原氯氧化物技术(
催化还原氯氧化物技术( )是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的
)是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为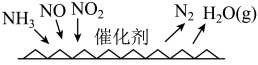
您最近一年使用:0次
名校
7 . 化学是以实验为基础的学科。
(1)某化学兴趣小组在实验室配制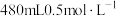 硫酸溶液。
硫酸溶液。
①在配制溶液时除了用到烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器是_______ 。
②在配制过程中,以下操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.量取浓硫酸时,仰视刻度线
B.转移前,容量瓶中含有少量蒸馏水
C.转移时,有少量液体溅出
D.未等溶液恢复至室温就转移到容量瓶中
(2)该小组同学取配制好的 的硫酸溶液
的硫酸溶液 与
与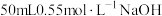 溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为
溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为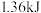 ,则该同学得到的中和热
,则该同学得到的中和热
____ 。
(3)该小组欲准确测定某市售双氧水中 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
①滴定反应的离子方程式为_______ 。
②滴定时,将高锰酸钾标准溶液注入_______ (填“酸”或“碱”)式滴定管中、滴定终点的判断是_______ 。
③根据实验测得,消耗 溶液,那么
溶液,那么 的浓度为
的浓度为_______ 。若滴定过程按以下操作会造成测定结果偏低的是_______ 。
A.滴定管未用 标准溶液润洗
标准溶液润洗
B.量取双氧水时,滴定前尖嘴有气泡,滴定后气泡消失
C.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后平视读数
D.锥形瓶未用待测液润洗
(1)某化学兴趣小组在实验室配制
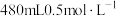 硫酸溶液。
硫酸溶液。①在配制溶液时除了用到烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器是
②在配制过程中,以下操作会导致所配溶液浓度偏高的是
A.量取浓硫酸时,仰视刻度线
B.转移前,容量瓶中含有少量蒸馏水
C.转移时,有少量液体溅出
D.未等溶液恢复至室温就转移到容量瓶中
(2)该小组同学取配制好的
 的硫酸溶液
的硫酸溶液 与
与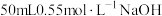 溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为
溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为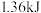 ,则该同学得到的中和热
,则该同学得到的中和热
(3)该小组欲准确测定某市售双氧水中
 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。①滴定反应的离子方程式为
②滴定时,将高锰酸钾标准溶液注入
③根据实验测得,消耗
 溶液,那么
溶液,那么 的浓度为
的浓度为A.滴定管未用
 标准溶液润洗
标准溶液润洗B.量取双氧水时,滴定前尖嘴有气泡,滴定后气泡消失
C.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后平视读数
D.锥形瓶未用待测液润洗
您最近一年使用:0次
名校
8 . Ⅰ. 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。
(1) (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是_______ 。
② 的沸点高于
的沸点高于 的可能原因是
的可能原因是_______ 。
(2)工业合成 时用到含铁催化剂。
时用到含铁催化剂。
① 元素在周期表第
元素在周期表第_______ 族,基态 原子电子的空间运动状态有
原子电子的空间运动状态有_______ 种。
②从结构的角度分析 容易被氧化成
容易被氧化成 的原因是
的原因是_______ 。
(3)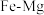 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。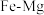 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有_______ 个。
②要储存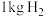 ,至少需要
,至少需要_______ 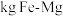 合金。
合金。
Ⅱ.钛及其化合物具有优异的物理、化学性能,相关的研究备受关注。具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:_______ 个 原子。
原子。
②该晶胞的化学式为_______ 。
 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。(1)
 (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②
 的沸点高于
的沸点高于 的可能原因是
的可能原因是(2)工业合成
 时用到含铁催化剂。
时用到含铁催化剂。①
 元素在周期表第
元素在周期表第 原子电子的空间运动状态有
原子电子的空间运动状态有②从结构的角度分析
 容易被氧化成
容易被氧化成 的原因是
的原因是(3)
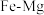 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。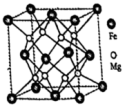
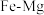 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有②要储存
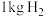 ,至少需要
,至少需要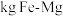 合金。
合金。Ⅱ.钛及其化合物具有优异的物理、化学性能,相关的研究备受关注。具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:

 原子。
原子。②该晶胞的化学式为
您最近一年使用:0次
名校
9 . 铍及其化合物的应用正日益被重视.
(1)最重要的含铍矿物是绿柱石,含2%铬 的绿柱石即为祖母绿.基态
的绿柱石即为祖母绿.基态 原子价电子的轨道表示式为
原子价电子的轨道表示式为_________________ 。
(2)铍与相邻主族的铝元素性质相似.下列有关铍和铝的叙述正确的有_____________(填标号)。
(3)氯化铍在气态时存在 分子(a)和二聚分子
分子(a)和二聚分子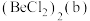 ,固态时则具有如下图所示的链状结构(c)。
,固态时则具有如下图所示的链状结构(c)。 原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为:
原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为:_______________ (标出配位键).
②c中 原子的杂化方式为
原子的杂化方式为_________________ 。
③氯化铍晶体中存在的作用力有_______________________ (填标号)。
A.范德华力 B.σ键 C.极性键 D.非极性键 E.离子键
(4) 立方晶胞如图所示。若
立方晶胞如图所示。若 晶体的密度为
晶体的密度为 ,则晶胞参数
,则晶胞参数
_____________  ,(列出计算式即可)。
,(列出计算式即可)。
(1)最重要的含铍矿物是绿柱石,含2%铬
 的绿柱石即为祖母绿.基态
的绿柱石即为祖母绿.基态 原子价电子的轨道表示式为
原子价电子的轨道表示式为(2)铍与相邻主族的铝元素性质相似.下列有关铍和铝的叙述正确的有_____________(填标号)。
| A.都属于p区主族元素 | B.电负性都比镁大 |
| C.第一电离能都比镁大 | D.氯化物的水溶液 均小于7 均小于7 |
(3)氯化铍在气态时存在
 分子(a)和二聚分子
分子(a)和二聚分子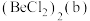 ,固态时则具有如下图所示的链状结构(c)。
,固态时则具有如下图所示的链状结构(c)。
 原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为:
原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为:②c中
 原子的杂化方式为
原子的杂化方式为③氯化铍晶体中存在的作用力有
A.范德华力 B.σ键 C.极性键 D.非极性键 E.离子键
(4)
 立方晶胞如图所示。若
立方晶胞如图所示。若 晶体的密度为
晶体的密度为 ,则晶胞参数
,则晶胞参数
 ,(列出计算式即可)。
,(列出计算式即可)。
您最近一年使用:0次
名校
10 . 对于钠的卤化物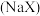 和硅的卤化物
和硅的卤化物 ,下列叙述正确的是
,下列叙述正确的是
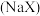 和硅的卤化物
和硅的卤化物 ,下列叙述正确的是
,下列叙述正确的是A. 难水解 难水解 | B. 是共价化合物 是共价化合物 | C. 易水解 易水解 | D. 的熔点一般低于 的熔点一般低于 |
您最近一年使用:0次



