名校
1 . 下列有关物质的性质与用途均正确,且具有对应关系的是
| A.硅酸钠易溶于水,可用作木材防火剂 |
B. 与水反应生成 与水反应生成 ,故 ,故 是酸性氧化物 是酸性氧化物 |
C. 的酸性弱于 的酸性弱于 ,故非金属性C强于Si ,故非金属性C强于Si |
| D.二氧化硅做半导体材料,故“玉兔号”月球车帆板太阳能电池片的材料主要是二氧化硅 |
您最近一年使用:0次
名校
2 . Ⅰ.部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
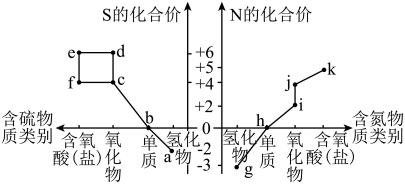
回答下列问题:
(1)j的化学名称是___________ 。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是___________ (填字母)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是___________ 。
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有___________ ,其中被氧化的元素是___________ (填元素符号)。
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是___________ 。
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是___________ (填名称)。
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案___________ (填“可行”或“不可行”),原因是___________ 。
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为___________ ,由此可知产品中___________ (填“含有”或“不含有”)SCl2杂质。

回答下列问题:
(1)j的化学名称是
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为
您最近一年使用:0次
名校
3 . 硫元素广泛存在于自然界中,是动植物生长不可缺少的元素。
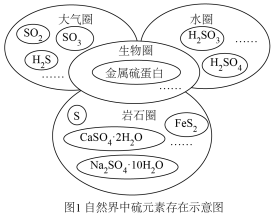
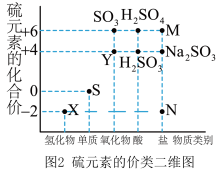
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 。
(2)工业上常以黄铁矿为原料来制备硫酸,通入空气焙烧黄铁矿的化学方程式为___________ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
II.小组同学利用图3装置测定空气中 的含量。
的含量。___________ ,该装置中发生反应的离子方程式为___________ 。
(5)若空气流速为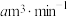 ,当观察到装置内
,当观察到装置内___________ 时,结束计时,测定耗时tmin,假定空气中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是___________  。
。
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
(2)工业上常以黄铁矿为原料来制备硫酸,通入空气焙烧黄铁矿的化学方程式为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是II.小组同学利用图3装置测定空气中
 的含量。
的含量。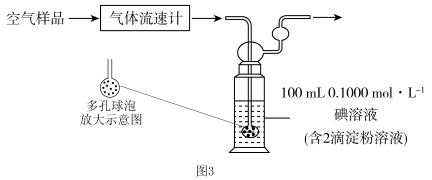
(5)若空气流速为
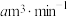 ,当观察到装置内
,当观察到装置内 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是 。
。
您最近一年使用:0次
4 . 目前世界各国都规划了碳达峰、碳中和的时间节点,以CO2为碳源,将其转化为能源物质。选择性加氢合成CH3OH,合成过程中发生下列反应:
反应i:CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H1=-akJ‧mol-1
反应ii:CO(g)+2H2(g)⇌CH3OH(g) ∆H2
反应iii:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H3=-bkJ‧mol-1
回答下列问题:
(1)根据盖斯定律,∆H2=。___________ kJ‧mol-1(用含a,b的代数式表示)。
(2)在一绝热、刚性容器中,只发生反应iii。下列说法表明反应已达到平衡状态的是___________(填序号)。
(3)中科院兰州化物所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,反应过程如图所示。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。

在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表所示:
欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加Na助剂是否效果最好?_________ (填“是”或“否”),请叙述原因:___________ 。
(4)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ∆H=-74kJ‧mol-1。该反应正反应的活化能___________ (填“>”“<”或“=”) 逆反应的活化能。
(5)在一定条件下,将1molCO和2molH2充入IL恒容密闭容器中:发生反应:CO(g)+2H2(g)⇌CH3OH(g) ∆H2,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
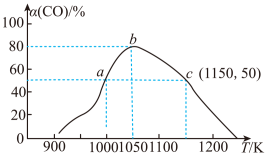
①温度为1000K时,反应开始至2min时,v(H2)=___________ mol‧L-1‧min-1
②CO的转化率随温度的升高先增大后变小的原因是___________ 。
(6)为实现CO2资源化利用,通过光电转化原理以CO2为原料制备甲酸产品(如图所示)。
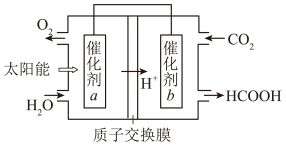
①光电转化过程中,阴极反应式为___________
②催化剂b附近生成lmolHCOOH时,标准状况下催化剂a附近理论上产生______ L气体。
反应i:CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H1=-akJ‧mol-1
反应ii:CO(g)+2H2(g)⇌CH3OH(g) ∆H2
反应iii:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H3=-bkJ‧mol-1
回答下列问题:
(1)根据盖斯定律,∆H2=。
(2)在一绝热、刚性容器中,只发生反应iii。下列说法表明反应已达到平衡状态的是___________(填序号)。
| A.混合气体的总物质的量不再变化 | B.n(CH3OH):n(H2O)=1:1 |
| C.v正(CH3OH)=3v逆(H2) | D.该反应的K不再变化 |

在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表所示:
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比 | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
(4)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ∆H=-74kJ‧mol-1。该反应正反应的活化能
(5)在一定条件下,将1molCO和2molH2充入IL恒容密闭容器中:发生反应:CO(g)+2H2(g)⇌CH3OH(g) ∆H2,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:

①温度为1000K时,反应开始至2min时,v(H2)=
②CO的转化率随温度的升高先增大后变小的原因是
(6)为实现CO2资源化利用,通过光电转化原理以CO2为原料制备甲酸产品(如图所示)。

①光电转化过程中,阴极反应式为
②催化剂b附近生成lmolHCOOH时,标准状况下催化剂a附近理论上产生
您最近一年使用:0次
名校
5 . 燃油汽车尾气中NO和CO的排放,是大气污染的主要原因之一。NSR系统( ,storage and reduction)是一种有效降低
,storage and reduction)是一种有效降低 排放的策略。
排放的策略。
Ⅰ.NSR系统热力学分析
(1)NSR系统中工作原理的方程式为 。298K,101kPa下,该反应的
。298K,101kPa下,该反应的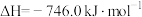 ,
,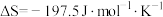 ,该反应在热力学上趋势很大,其原因是
,该反应在热力学上趋势很大,其原因是_______ 。
Ⅱ.密闭容器中NSR系统平衡研究
(2)温度 ℃时,在2L的密闭容器中,充入CO、NO各0.4mol,分别对比三种催化剂(Ⅰ、Ⅱ、Ⅲ)对NSR系统中反应的催化效果,结果如图所示:
℃时,在2L的密闭容器中,充入CO、NO各0.4mol,分别对比三种催化剂(Ⅰ、Ⅱ、Ⅲ)对NSR系统中反应的催化效果,结果如图所示:
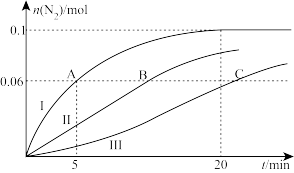
①反应开始到A点,用NO浓度变化表示的平均反应速率为_______  。
。
②B点所在体系达平衡时,放出的热量为_______ kJ。
③C点所在体系达平衡后,继续加入0.2mol NO、0.2mol CO、0.3mol 、0.2mol
、0.2mol  ,再次平衡时的
,再次平衡时的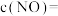
_______  。
。
Ⅲ.NSR系统机理研究
重庆一中某探究性学习小组模拟NSB系统中“吸附、储存、释放、还产物原”四个阶段的全过程。先控制气流(成分为NO、 )通过NSR反应器,待出口处浓度稳定后,通入还原性气体(CO等)。总反应为
)通过NSR反应器,待出口处浓度稳定后,通入还原性气体(CO等)。总反应为 。四个阶段与出口处浓度的时间对应关系如图所示,回答下列问题:
。四个阶段与出口处浓度的时间对应关系如图所示,回答下列问题:
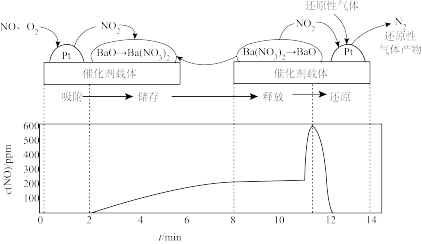
(3)吸附阶段:2min前,出口处的 浓度接近于0,原因是
浓度接近于0,原因是_______ 。
(4)释放阶段:写出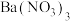 释放出
释放出 的化学反应方程式:
的化学反应方程式:_______ 。
(5)还原阶段:
①通入的还原性气体成分为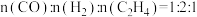 ,与
,与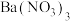 中释放的
中释放的 反应后,气体成分为
反应后,气体成分为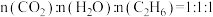 [
[ 未测定],则反应的
未测定],则反应的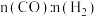

_______ 。
②有研究表明,还原性气体中若混有 ,会导致催化剂中毒,活性下降,从氧化还原反应原理和催化剂循环再生的角度分析可能原因:
,会导致催化剂中毒,活性下降,从氧化还原反应原理和催化剂循环再生的角度分析可能原因:_______ 。
 ,storage and reduction)是一种有效降低
,storage and reduction)是一种有效降低 排放的策略。
排放的策略。Ⅰ.NSR系统热力学分析
(1)NSR系统中工作原理的方程式为
 。298K,101kPa下,该反应的
。298K,101kPa下,该反应的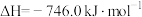 ,
,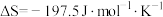 ,该反应在热力学上趋势很大,其原因是
,该反应在热力学上趋势很大,其原因是Ⅱ.密闭容器中NSR系统平衡研究
(2)温度
 ℃时,在2L的密闭容器中,充入CO、NO各0.4mol,分别对比三种催化剂(Ⅰ、Ⅱ、Ⅲ)对NSR系统中反应的催化效果,结果如图所示:
℃时,在2L的密闭容器中,充入CO、NO各0.4mol,分别对比三种催化剂(Ⅰ、Ⅱ、Ⅲ)对NSR系统中反应的催化效果,结果如图所示:
①反应开始到A点,用NO浓度变化表示的平均反应速率为
 。
。②B点所在体系达平衡时,放出的热量为
③C点所在体系达平衡后,继续加入0.2mol NO、0.2mol CO、0.3mol
 、0.2mol
、0.2mol  ,再次平衡时的
,再次平衡时的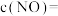
 。
。Ⅲ.NSR系统机理研究
重庆一中某探究性学习小组模拟NSB系统中“吸附、储存、释放、还产物原”四个阶段的全过程。先控制气流(成分为NO、
 )通过NSR反应器,待出口处浓度稳定后,通入还原性气体(CO等)。总反应为
)通过NSR反应器,待出口处浓度稳定后,通入还原性气体(CO等)。总反应为 。四个阶段与出口处浓度的时间对应关系如图所示,回答下列问题:
。四个阶段与出口处浓度的时间对应关系如图所示,回答下列问题:
(3)吸附阶段:2min前,出口处的
 浓度接近于0,原因是
浓度接近于0,原因是(4)释放阶段:写出
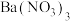 释放出
释放出 的化学反应方程式:
的化学反应方程式:(5)还原阶段:
①通入的还原性气体成分为
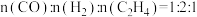 ,与
,与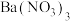 中释放的
中释放的 反应后,气体成分为
反应后,气体成分为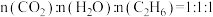 [
[ 未测定],则反应的
未测定],则反应的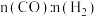

②有研究表明,还原性气体中若混有
 ,会导致催化剂中毒,活性下降,从氧化还原反应原理和催化剂循环再生的角度分析可能原因:
,会导致催化剂中毒,活性下降,从氧化还原反应原理和催化剂循环再生的角度分析可能原因:
您最近一年使用:0次
解题方法
6 . 钛被称为继铁、铝之后的第三金属。钙钛矿是一类氧化物陶瓷材料,典型代表是 晶体,是工业获取钛的重要原料。
晶体,是工业获取钛的重要原料。
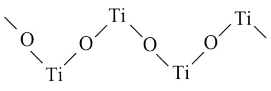
(1)基态钛原子的价层电子排布式为______ ,其原子核外共有______ 种运动状态不同的电子。
(2)六氟合钛酸钾(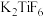 )中存在
)中存在 配离子,其中钛元素的化合价是
配离子,其中钛元素的化合价是______ ,配体是______ 。
(3)硫酸氧钛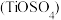 晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为
晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为______ ,阴离子中心原子的杂化轨道类型为______ 。
(4) 晶体结构如图,已知该晶体晶胞参数为anm,则与
晶体结构如图,已知该晶体晶胞参数为anm,则与 紧邻的O个数为
紧邻的O个数为______ ,O与O间的最短距离为______  。
。
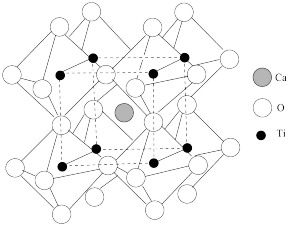
(5)钨青铜( )是一类色彩丰富的非整比化合物,其晶体结构与上述
)是一类色彩丰富的非整比化合物,其晶体结构与上述 晶体结构相同,若
晶体结构相同,若 无空缺,化学式为
无空缺,化学式为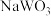 ,完全空缺则为
,完全空缺则为 ,每填入1个
,每填入1个 ,相应有1个
,相应有1个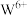 还原为
还原为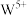 。
。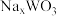 的颜色与x值的对应关系如图所示,已知某钨青铜晶体中
的颜色与x值的对应关系如图所示,已知某钨青铜晶体中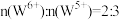 ,则其颜色为
,则其颜色为______ 色。
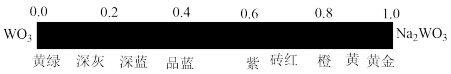
 晶体,是工业获取钛的重要原料。
晶体,是工业获取钛的重要原料。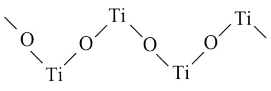
(1)基态钛原子的价层电子排布式为
(2)六氟合钛酸钾(
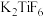 )中存在
)中存在 配离子,其中钛元素的化合价是
配离子,其中钛元素的化合价是(3)硫酸氧钛
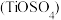 晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为
晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为(4)
 晶体结构如图,已知该晶体晶胞参数为anm,则与
晶体结构如图,已知该晶体晶胞参数为anm,则与 紧邻的O个数为
紧邻的O个数为 。
。
(5)钨青铜(
 )是一类色彩丰富的非整比化合物,其晶体结构与上述
)是一类色彩丰富的非整比化合物,其晶体结构与上述 晶体结构相同,若
晶体结构相同,若 无空缺,化学式为
无空缺,化学式为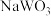 ,完全空缺则为
,完全空缺则为 ,每填入1个
,每填入1个 ,相应有1个
,相应有1个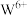 还原为
还原为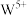 。
。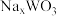 的颜色与x值的对应关系如图所示,已知某钨青铜晶体中
的颜色与x值的对应关系如图所示,已知某钨青铜晶体中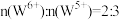 ,则其颜色为
,则其颜色为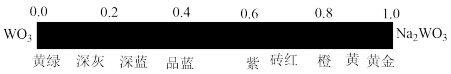
您最近一年使用:0次
解题方法
7 . 海洋是人类未来赖以生存和发展的资源宝库,合理开发和有效利用应得到重视。如从海藻灰中可得到NaI溶液。
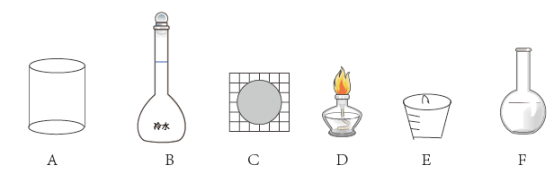
(1)以NaI溶液为原料,经过一系列变化和操作,可得到粗碘,进一步提纯粗碘时,不需要的仪器有___________ 。
(2)某学习小组以空气氧化NaI溶液为研究对象,探究溶液的酸碱性对反应的影响。
①用CCl4萃取反应后I、II、III、IV 的溶液,萃取后下层CCl4均为无色,取萃取后的上层溶液,用淀粉检验:I、Ⅱ的溶液变蓝色;III的溶液蓝色不明显、Ⅳ的溶液未变蓝。
i.写出实验Ⅰ中反应的离子方程式___________ 。
ii.查阅资料;I2易溶于NaI溶液。下列实验证实了该结论并解释Ⅰ、II的萃取现象:
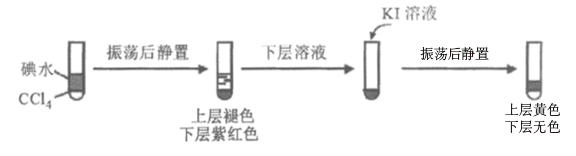
用CCl4萃取Ⅰ、II反应后的溶液,萃取后下层CCl4颜色均无色的原因是___________ 。
②查阅资料:pH <11.7时,I—能被O2氧化为I2;pH≥9.28时,I2发生歧化反应:3I2+6OH—=IO3—+5I—+3H2O,pH越大,歧化速率越快。某同学利用原电池原理设计实验证实:PH = 10的条件下实验Ⅳ确实可以发生I—能被O2氧化为I2的反应,如图所示:
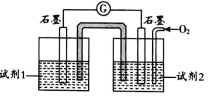
据此分析,试剂1是___________ ;试剂2是 ___________ 。
实验现象:电流表指针偏转,左侧电极附近溶液变蓝(±<30 min )。
③综合实验现象。说明I—被空气氧化的影响因素及对应关系为___________ 。
(3)测定NaI溶液中I—含量。
量取25.00 mL,NaI溶液于250mL锥形瓶中,分别加入少量稀H2SO4和稍过量的NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,用c mol· L-1酸性标准KMnO4溶液进行滴定至终点,重复3次。平均每次消耗KMnO4溶液VmL(已知反应:2Fe3+ +2I—=2Fe2++ I2 、5Fe2++ +8H+=5Fe3++Mn2+ +4H2O)。
+8H+=5Fe3++Mn2+ +4H2O)。
①该实验达到滴定终点时,现象为___________ 。
②根据滴定有关数据,该NaI溶液中I—含量是___________ g·L-1。
(1)以NaI溶液为原料,经过一系列变化和操作,可得到粗碘,进一步提纯粗碘时,不需要的仪器有

(2)某学习小组以空气氧化NaI溶液为研究对象,探究溶液的酸碱性对反应的影响。
| 实验 | 编号 | pH = a | 现象 |
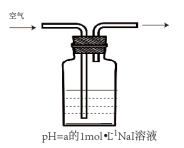 | I | 3 | 4分钟左右,溶液呈黄色 |
| Ⅱ | 7 | 60分钟左右,溶液呈浅黄色 | |
| Ⅲ | 8 | 10小时后,溶液呈很浅的黄色 | |
| Ⅳ | 10 | 10小时后,溶液颜色无明显变化 |
i.写出实验Ⅰ中反应的离子方程式
ii.查阅资料;I2易溶于NaI溶液。下列实验证实了该结论并解释Ⅰ、II的萃取现象:

用CCl4萃取Ⅰ、II反应后的溶液,萃取后下层CCl4颜色均无色的原因是
②查阅资料:pH <11.7时,I—能被O2氧化为I2;pH≥9.28时,I2发生歧化反应:3I2+6OH—=IO3—+5I—+3H2O,pH越大,歧化速率越快。某同学利用原电池原理设计实验证实:PH = 10的条件下实验Ⅳ确实可以发生I—能被O2氧化为I2的反应,如图所示:

据此分析,试剂1是
实验现象:电流表指针偏转,左侧电极附近溶液变蓝(±<30 min )。
③综合实验现象。说明I—被空气氧化的影响因素及对应关系为
(3)测定NaI溶液中I—含量。
量取25.00 mL,NaI溶液于250mL锥形瓶中,分别加入少量稀H2SO4和稍过量的NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,用c mol· L-1酸性标准KMnO4溶液进行滴定至终点,重复3次。平均每次消耗KMnO4溶液VmL(已知反应:2Fe3+ +2I—=2Fe2++ I2 、5Fe2++
 +8H+=5Fe3++Mn2+ +4H2O)。
+8H+=5Fe3++Mn2+ +4H2O)。①该实验达到滴定终点时,现象为
②根据滴定有关数据,该NaI溶液中I—含量是
您最近一年使用:0次
8 . 钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。
已知:①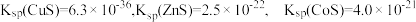 。
。
②以氢氧化物形式沉淀时,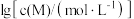 和溶液
和溶液 的关系如图所示。
的关系如图所示。
(1)“酸浸”前,需将废渣磨碎,其目的是_____ 。
(2)“酸浸”步骤中, 发生反应的化学方程式是
发生反应的化学方程式是_____ 。
(3)假设“沉铜”后得到的滤液中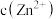 和
和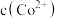 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中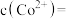
_____  ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离_____ (填“能”或“不能”)。
(4)“沉锰”步骤中,生成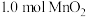 ,产生
,产生 的物质的量为
的物质的量为_____ 。
(5)“沉淀”步骤中,用 调
调 ,分离出的滤渣是
,分离出的滤渣是_____ 。
(6)“沉钴”步骤中,控制溶液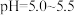 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为_____ 。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是_____ 。
 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。已知:①
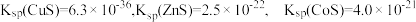 。
。②以氢氧化物形式沉淀时,
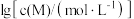 和溶液
和溶液 的关系如图所示。
的关系如图所示。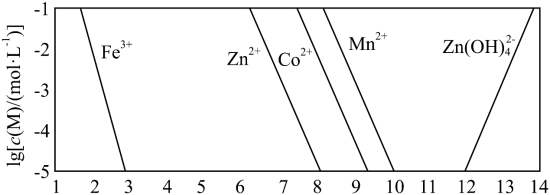
(1)“酸浸”前,需将废渣磨碎,其目的是
(2)“酸浸”步骤中,
 发生反应的化学方程式是
发生反应的化学方程式是(3)假设“沉铜”后得到的滤液中
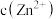 和
和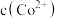 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中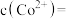
 ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离(4)“沉锰”步骤中,生成
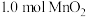 ,产生
,产生 的物质的量为
的物质的量为(5)“沉淀”步骤中,用
 调
调 ,分离出的滤渣是
,分离出的滤渣是(6)“沉钴”步骤中,控制溶液
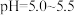 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是
您最近一年使用:0次
名校
9 . 硼、氮、铁、钴、镍等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
(2)硼酸( )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在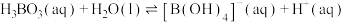 的平衡,回答下列问题。
的平衡,回答下列问题。__________ 。
②下列关于硼酸的说法正确的是__________ (填序号)。
a. 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
c.硼酸分子的稳定性与氢键有关 d.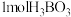 晶体中有
晶体中有 氢键
氢键
(3)叠氮化合物在化工上有重要应用, 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式__________ (写出一种即可),其立体构型为__________ 。
(4) 的结构如图所示,
的结构如图所示, 中
中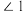 、
、 、
、 由大到小的顺序是
由大到小的顺序是____________________ 。 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于__________ 位置。
①从该晶胞中能分割出来的结构图有_______ (填标号)。 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有__________ 个,该距离为__________ pm(仅列式不计算)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
A.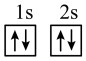 | B. |
C.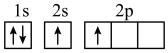 | D.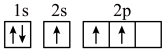 |
(2)硼酸(
 )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在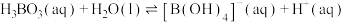 的平衡,回答下列问题。
的平衡,回答下列问题。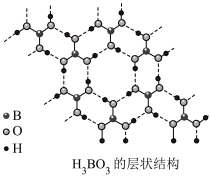
②下列关于硼酸的说法正确的是
a.
 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制c.硼酸分子的稳定性与氢键有关 d.
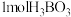 晶体中有
晶体中有 氢键
氢键(3)叠氮化合物在化工上有重要应用,
 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(4)
 的结构如图所示,
的结构如图所示, 中
中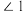 、
、 、
、 由大到小的顺序是
由大到小的顺序是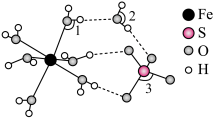
 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于
①从该晶胞中能分割出来的结构图有
a.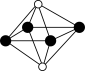 b.
b.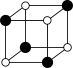 c.
c.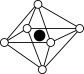 d.
d. e.
e.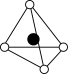
 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
您最近一年使用:0次
名校
10 . 请回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是___________ 。(填字母)
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有___________ 。(填字母)
a. b.盐酸和镁条
b.盐酸和镁条
c.盐酸和碳酸氢钠 d. 和氯化铵
和氯化铵
e. 分解
分解
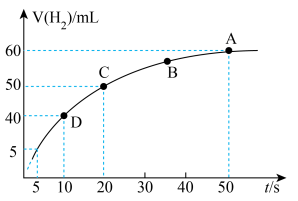
③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为___________ ;在20s内用H+浓度表示的平均反应速率
___________ (20s时溶液体积为50mL,气体摩尔体积为25L/mol)。 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。
t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:
①4-6min内 的平均反应速率
的平均反应速率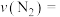
___________ 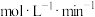
②下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.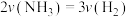 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化
C. 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变
③如表列出了在不同温度和压强下,反应达到平衡时 的百分含量
的百分含量 。
。
从表中数据得出,合成氨最优的条件是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有
a.
 b.盐酸和镁条
b.盐酸和镁条c.盐酸和碳酸氢钠 d.
 和氯化铵
和氯化铵e.
 分解
分解③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生
 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的
 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:①4-6min内
 的平均反应速率
的平均反应速率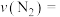
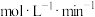
| 时间/min | 2 | 4 | 6 | 8 | 10 | 12 |
 / / | 0.04 | 0.10 | 0.14 | 0.16 | 0.16 | 0.16 |
A.
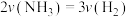 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化C.
 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变③如表列出了在不同温度和压强下,反应达到平衡时
 的百分含量
的百分含量 。
。压强/MPa % %温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
您最近一年使用:0次



