名校
解题方法
1 . 下列叙述正确的是
| A.CO2和SiO2都是酸性氧化物,所以两者物理性质相似 |
B.依据 ,推测硅酸的酸性比碳酸强 ,推测硅酸的酸性比碳酸强 |
| C.CO2和SiO2都能与碳反应,且都作氧化剂 |
| D.SiO2既能和NaOH反应,又能和HF反应,所以二氧化硅属于两性氧化物 |
您最近一年使用:0次
2023-10-07更新
|
196次组卷
|
12卷引用:山西省朔州市朔城区第一中学校2021-2022学年高一下学期开学检测化学试题
山西省朔州市朔城区第一中学校2021-2022学年高一下学期开学检测化学试题河南省南阳市六校2021-2022学年高一下学期3月份联考化学试题(已下线)第09讲 无机非金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)福建省建瓯市芝华中学2021-2022学年高一下学期第一次月考化学试题广东省中山市第一中学2022-2023学年高一下学期6月月考化学试题(已下线)第7讲 碳、硅及无机非金属材料福建省厦门第一中学2023-2024学年高三暑期复习检测化学试题陕西省西安中学2023-2024学年高三上学期第二次月考化学试题江西省丰城市第二中学2023-2024学年高一上学期11月期中考试化学试题(已下线)第03讲 无机非金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)陕西省西安市周至县第六中学2023-2024学年高三上学期11月期中化学试题(已下线)专题04 无机非金属材料(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
解题方法
2 . 利伐沙班是一种新型口服抗凝药,广泛用于血栓的预防和治疗。化合物H是合成利伐沙班的主要关键中间体,其合成路线如下:

已知:t-Bu是叔丁基团。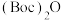 为Boc的酸酐。酰卤能与
为Boc的酸酐。酰卤能与 或-NH-、-OH上的氢原子发生取代反应。
或-NH-、-OH上的氢原子发生取代反应。
回答下列问题:
(1)A的化学名称是___________ 。B中所含官能团的名称为___________ 。
(2)C→D的反应类型是___________ 。化合物D的结构简式为___________ 。
(3)合成路线中,设计D→E的目的是___________ 。
(4)反应E→F的化学方程式为___________ 。
(5)H的同分异构体中,符合下列条件的共有___________ 种。
①分子结构中除苯环外,没有其他环;
分子中含有两个 ,属于α-氨基酸;
,属于α-氨基酸;
③苯环上有两个取代基,其中一个取代基为 。
。
其中核磁共振氢谱显示有七组峰,峰面积之比为2∶2∶2∶2∶2∶1∶1的结构简式为_______ (任写一种)。

已知:t-Bu是叔丁基团。
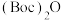 为Boc的酸酐。酰卤能与
为Boc的酸酐。酰卤能与 或-NH-、-OH上的氢原子发生取代反应。
或-NH-、-OH上的氢原子发生取代反应。回答下列问题:
(1)A的化学名称是
(2)C→D的反应类型是
(3)合成路线中,设计D→E的目的是
(4)反应E→F的化学方程式为
(5)H的同分异构体中,符合下列条件的共有
①分子结构中除苯环外,没有其他环;
分子中含有两个
 ,属于α-氨基酸;
,属于α-氨基酸;③苯环上有两个取代基,其中一个取代基为
 。
。其中核磁共振氢谱显示有七组峰,峰面积之比为2∶2∶2∶2∶2∶1∶1的结构简式为
您最近一年使用:0次
名校
解题方法
3 . 环戊烯(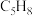 ,
, )是一种重要的有机化工原料,可用环戊二烯(
)是一种重要的有机化工原料,可用环戊二烯( ,
,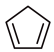 )制备。
)制备。
反应Ⅰ:
 (g,环戊二烯)
(g,环戊二烯)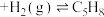 (g,环戊烯)
(g,环戊烯) 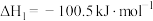
反应Ⅱ:
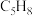 (g,环戊烯)
(g,环戊烯)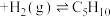 (g,环戊烷)
(g,环戊烷) 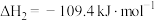
反应Ⅲ:

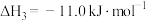
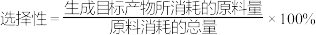
(1)某温度下,将环戊二烯和HI按物质的量之比1∶2(总物质的量为a mol)充入容积为2L的恒容密闭容器中,发生反应:
 (g,环戊二烯)
(g,环戊二烯)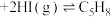 (g,环戊烯)
(g,环戊烯)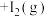 。
。①该反应的△H=
 ,该反应自发进行的条件是
,该反应自发进行的条件是②下列有关该反应的叙述正确的是
A.当气体压强不变时,说明反应已达到平衡状态
B.升高温度,有利于提高环戊烯的平衡产率
C.反应达到平衡时,环戊二烯和碘化氢的转化率相等
D.通入惰性气体,有利于提高环戊二烯的平衡转化率
(2)以Pd/
 为催化剂,如图1为25℃时环戊二烯的氢化过程,环戊烯与环戊烷的各组分含量(物质的量含量)随时间(t)的变化。为研究不同温度下的催化剂活性,测得不同温度(其他条件相同)下反应4h时环戊二烯的转化率和环戊烯的选择性的数据如图2所示。
为催化剂,如图1为25℃时环戊二烯的氢化过程,环戊烯与环戊烷的各组分含量(物质的量含量)随时间(t)的变化。为研究不同温度下的催化剂活性,测得不同温度(其他条件相同)下反应4h时环戊二烯的转化率和环戊烯的选择性的数据如图2所示。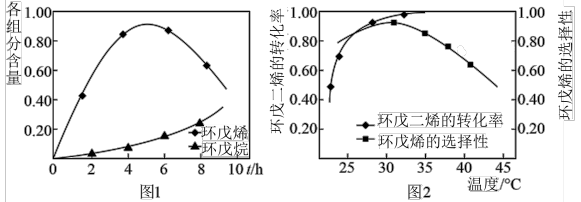
②升高温度,环戊二烯的转化率提高而环戊烯的选择性降低,其原因是
(3)已知两分子环戊二烯易发生加成反应生成二聚体双环戊二烯分子。不同温度(
 、
、 )下,在2L恒容容器中环戊二烯的物质的量与反应时间的关系如图所示(已知起始时环戊二烯的物质的量为1.5mol)。推测
)下,在2L恒容容器中环戊二烯的物质的量与反应时间的关系如图所示(已知起始时环戊二烯的物质的量为1.5mol)。推测
 (填“<”“>”或“=”);
(填“<”“>”或“=”); 时,用二聚体双环戊二烯表示0~1h的平均反应速率v=
时,用二聚体双环戊二烯表示0~1h的平均反应速率v=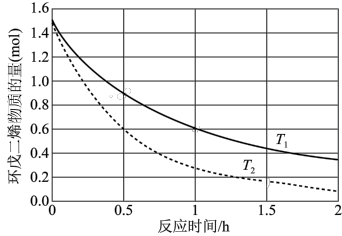


 为用各物质的平衡分压表示反应的平衡常数)。
为用各物质的平衡分压表示反应的平衡常数)。
您最近一年使用:0次
2023-08-04更新
|
190次组卷
|
3卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题
名校
解题方法
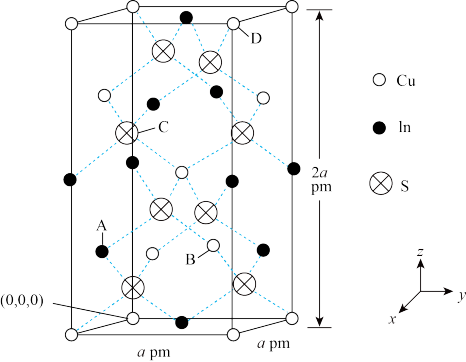
4 . 某种太阳能材料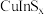 晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为
晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为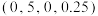 ,B处Cu原子坐标为
,B处Cu原子坐标为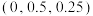 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
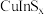 晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为
晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为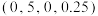 ,B处Cu原子坐标为
,B处Cu原子坐标为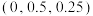 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A.C处S原子坐标为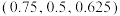 |
B.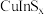 中的x=4 中的x=4 |
C.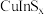 晶体中,每个D处Cu原子周围紧邻且距离相等的Cu原子共有6个 晶体中,每个D处Cu原子周围紧邻且距离相等的Cu原子共有6个 |
D.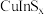 晶体的密度为 晶体的密度为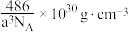 |
您最近一年使用:0次
5 . 由化合物X合成荧光探针的反应如下。已知:酰胺基、酯基均不与H2反应。下列说法正确的是
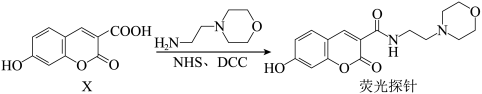

| A.1mol X最多能与3mol NaOH反应 |
| B.荧光探针与足量H2加成所得产物的1个分子中含有4个手性碳原子 |
| C.荧光探针能发生取代反应、加成反应、消去反应 |
| D.和溴水反应时,1mol荧光探针最多能消耗2mol Br2 |
您最近一年使用:0次
名校
6 . 化学与材料密切相关。下列说法错误的是
| A.毛笔中“狼毫”的主要成分是蛋白质 | B.碳纳米管、石墨烯都属于有机高分子材料 |
| C.中华瑰宝唐兽首玛瑙杯属于玉器 | D.碲化镉发电玻璃属于新型无机非金属材料 |
您最近一年使用:0次
7 . 反应A+B→C(放热)分两步进行:①A+B→X(吸热),②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是
A.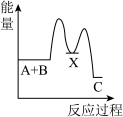 | B.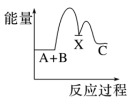 |
C.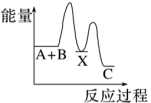 | D.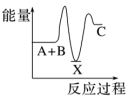 |
您最近一年使用:0次
2023-06-30更新
|
1448次组卷
|
317卷引用:山西省朔州市朔城区第一中学校2021-2022学年高一下学期开学检测化学试题
山西省朔州市朔城区第一中学校2021-2022学年高一下学期开学检测化学试题山西省太原市黄陵中学高新部2017-2018学年高二上学期开学考化学试题贵州省贵阳市2022届高三上学期8月摸底考试(开学考试)化学试题 (已下线)单科化学-2021年秋季高三开学摸底考试卷02(课标全国专用)河北正定中学2020-2021学年高一下学期第一次月考化学试题河南省南阳市第五完全中学2020-2021学年高二上学期开学考试化学试题广东省徐闻县徐闻中学2022-2023学年高二上学期开学测试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题四川省成都高新实验中学2021-2022学年高三上学期入学考试化学试题(已下线)2012-2013学年江苏省如皋中学高二10月阶段练习化学试卷(已下线)2012-2013学年福建省四地六校高二第一次月考化学试卷(已下线)2012-2013学年天津市天津一中高二上学期期中考试化学试卷(已下线)2012-2013学年吉林省长春市十一高中高二上学期期末考试化学试卷(已下线)2013学年海南省琼海市嘉积中学高一下学期教学质量监测(二)理科化学卷(已下线)2012-2013学年浙江宁波万里国际学校高一下学期期中考试化学试卷(已下线)2013届上海市虹口区高三上学期期末教学质量调研化学试卷(已下线)2013-2014学年江西省赣州市十二县高二上学期期中考试化学试卷(已下线)2013-2014学年江西省南昌市四校联考高二上学期期中考试化学试卷(已下线)2014届上海市十三校高三12月联考化学试卷(已下线)2013-2014学年内蒙古赤峰市元宝山区高二上学期期末化学试卷(已下线)2013-2014学年江苏省无锡江阴市高二下学期期中考试化学试卷2012年普通高等学校招生全国统一考试化学(大纲全国)(已下线)2014届黑龙江省哈师大附中高二上学期期末考试化学试卷(已下线)2013-2014河南省实验中学上学期期中考试高二化学试卷(已下线)2014-2015学年河北省唐山市开滦二中高二上学期第一次月考化学试卷(已下线)2015届黑龙江省牡丹江第一高中高二上学期期中考试化学(理)试卷2014-2015浙江省嘉兴一中高二上学期期中化学(理)试卷2015届福建省养正中学高三上学期第二次月考化学试卷2014-2015江苏省盐城市时杨中学高二12月月考化学试卷2014-2015学年吉林省长春市十一中高一下期中化学试卷2014-2015学年江苏省扬州市高二下学期期末考试化学试卷2015-2016学年安徽省郎溪中学高二上学期第一次月考化学试卷2016届福建省莆田市第二十五中学高三上学期期中测试化学试卷2015-2016学年湖北省宜昌市部分示范高中高二上期中测试化学试卷2015-2016学年山东枣庄三中高二10月学情调查化学卷2015-2016学年陕西省西安一中高二上10月月考化学试卷2015-2016学年河南省信阳高级中学高二12月月考化学卷2015-2016学年浙江省平阳二中高二上学期第一次质检化学试卷2015-2016学年山西省孝义市高二上学期期末考试化学试卷2015-2016学年浙江省杭州市余杭区高二上学期期末化学试卷2015-2016学年河北省邯郸市大名等四县高一下学期期中联考化学试卷2015-2016学年湖北省襄阳市老河口一中高一下期中化学试卷2015-2016学年江苏省盐城市建湖二中高二下学期期中考试化学试卷2015-2016学年河北省冀州市中学高一下期末化学试卷2015-2016学年河北省冀州市中学高一下期末理科化学A卷2015-2016学年甘肃省武威二中高一下第二次月考化学试卷2015-2016学年浙江省温州市十校联合体高二下学期期末联考化学试卷2015-2016学年安徽省阜阳市红旗中学高一下第二次月考化学试卷2015-2016学年辽宁沈阳市第二中学高一下期末考试化学卷2017届山西省重点中学协作体高三暑假第一次联考化学试卷2016-2017学年广东省潮阳实验学校高二上8月考试化学卷2016-2017学年湖南省长沙一中高一上第二次月考化学卷2016-2017学年河北省博野中学高二上学期第二次月考化学试卷2016-2017学年甘肃省天水一中高二上月考一化学试卷2016-2017学年天津市静海一中高二上9月调研化学试卷2017届湖南省益阳市高三上9月调研化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷2016-2017学年新疆生产建设兵团二中高二上期中化学卷2016-2017学年黑龙江省哈尔滨市第六中学高二3月月考化学试卷2016-2017学年贵州省都匀第一中学高二开学质检(3月)化学试卷2016-2017学年浙江省温州市“十五校联合体”高一下学期期中联考化学试卷山东省济南市第一中学2016-2017学年高一下学期期末考试化学试题山东省济南外国语学校三箭分校2016-2017学年高一下学期期末考试化学试题广西南宁市第二中学2016-2017学年高一下学期期末考试(理)化学试题江西省抚州市临川区第一中学2017-2018学年高二上学期第一次月考化学试题山西省实验中学2017-2018学年高二上学期10月月考化学试题新疆呼图壁县第一中学2017-2018学年高二上学期期中考试化学试题河南省商丘市九校2017-2018学年高二上学期期中联考化学试题宁夏六盘山高级中学2017-2018学年高二上学期期中考试化学试题河南省商丘市第一高级中学2017-2018学年高二上学期期中考试化学试题山东省枣庄市薛城区2017-2018学年高二上学期期末化学试题江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题峨山县第一中学2017-2018学年第二学期3月份月考卷(高三理综 化学部分)河南省林州一中分校(林虑中学)2017-2018学年高一4月调研考试化学试题【全国区级联考】山东省枣庄市薛城区2017-2018学年高一下学期期中考试化学试题【全国校级联考】浙江省温州市十五校联合体2017-2018学年高一下学期期中联考化学试题甘肃省甘谷县第一中学2018-2019学年高二上学期第一次月考子材班化学试题湖北省公安县车胤中学2018-2019学年高二上学期9月月考化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题浙江省杭州市建人高复2019届高三上学期第一次月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期9月模块诊断化学试题浙江省台州市书生中学2018-2019学年高二上学期第一次月考化学试题【校级联考】江西省南昌市八一中学、洪都中学2018-2019学年高二上学期10月联考化学试题浙江省杭州市西湖高级中学2017-2018学年高二12月月考化学试题【全国百强校】福建省仙游第一中学2018-2019学年高二上学期期中考试化学试题甘肃省岷县第二中学2018-2019学年高二上学期期中考试化学试题江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题河北省衡水市滁州分校2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区石河子二中2018-2019学年高二上学期第二次月考化学试题河南省正阳高中2018-2019学年高二上学期期中素质检测化学试题甘肃省靖远县第四中学2018-2019学年高二上学期第二次月考化学试题山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题【校级联考】湖南省湘西自治州四校2018-2019学年高二上学期12月联考化学试题【校级联考】江西省吉安市几所重点中学2018-2019学年高二上学期联考化学试题内蒙古乌兰察布市北京八中乌兰察布分校2018-2019学年高二上学期第二次月考调研化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高二上学期期末考试化学试题【区级联考】安徽省宿州市埇桥区2018-2019学年高二(理)上学期期末考试化学试题福建省泉州市泉港区第一中学2018-2019学年高二上学期期末考试化学试题【全国百强校】湖南省衡阳市衡阳县第一中学2018-2019学年高一下学期第一次月考化学试题山西省长治市沁县中学2018-2019学年高一下学期期中考试化学试题陕西省渭南市尚德中学2018-2019学年高一下学期期中考试化学试题甘肃省岷县第一中学2018-2019学年高一下学期第一次月考化学试题【市级联考】贵州省遵义市2018-2019学年高一下学期期中考试化学试题陕西省黄陵中学高新部2018-2019学年高一第二学期期中考试化学试题陕西省黄陵县中学2018-2019学年高一(重点班)下学期期中考试化学试题河北安平中学2018-2019学年高二下学期期末考试化学试题天津市静海区四校2019-2020学年高二上学期9月联考化学试题辽宁省六校协作体2019-2020学年高二上学期10月月考化学试题安徽省青阳县第一中学2019-2020学年高二9月月考化学试题浙江省嘉兴市第一中学2019-2020学年高二10月月考化学试题福建省永安市第三中学2019-2020学年高二10月月考化学试题甘肃省白银市会宁县第四中学2019-2020学年高二上学期期中考试化学试题(已下线)【新东方】高中化学138(已下线)2019年3月14日 《每日一题》 必修2 化学反应过程的能量变化图分析黑龙江省双鸭山市第一中学2019-2020学年高二上学期期中考试化学试题甘肃省永昌四中2019-2020学年高二上学期期中考试化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期期中考试(A班)化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期期中考试(B班)化学试题福建省泉州第十六中学2019-2020学年高二上学期期中考试化学(选考班)试题福建2020届高三化学总复习专题训练——选修四化学反应原理测试陕西省渭南市临渭区尚德中学2020届高三上学期第三次月考化学试题山东省德州市夏津县双语中学2019-2020学年高二上学期第二次月考化学试题山东省泰安市泰山国际学校2019-2020学年高二上学期第一次月考化学试题2019届上海奉贤区高考第一次模拟化学试题安徽省枞阳县浮山中学2019-2020学年高二上学期期中考试化学试题湖南省长沙市第一中学2019-2020学年高二上学期第一次月考化学试题2020届高三化学二轮冲刺新题专练——能量变化的图像分析2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷2020届高三化学选修4二轮专题练——中和热及其测定【选择精编25题】2020届高三化学知识点强化训练—化学反应中能量变化2020届上海市奉贤区高考化学一模试卷安徽省合肥市2020届高三第一次教学质量检测化学试题(已下线)【新东方】2020-4内蒙古包钢第一中学2020届高三上学期10月月考化学试题黑龙江省牡丹江市穆棱市第一中学2019-2020学年高二上学期期末考试化学试题(已下线)上海市虹口区2013年高考一模化学试题新疆哈密市第十五中学2019-2020学年高一上学期期末考试化学试题课时1 化学反应与热能——A学习区 夯实基础(人教版(2019)第二册)第1节 化学键与化学反应 易错疑难集训(一)——A学习区 夯实基础(鲁科版必修2)第2节 化学反应与能量转化 易错疑难集训(一)——A学习区 夯实基础(鲁科版(2019)第二册)(已下线)【南昌新东方】2019 进贤一中 高二上 第一次月考湖北省武汉市2019-2020学年高一下学期期中联考化学试卷吉林省长春市第二十九中学2020届高三上学期期末考试化学试题湖南省邵东县第一中学2019-2020学年高二下学期第一次月考化学试题山东省新泰市第一中学2019-2020学年高一下学期期中考试化学试题安徽省肥东县第二中学2019-2020学年高一下学期期中考试(共建班)化学试题(已下线)【南昌新东方】2019-2020 雷氏中学 高一下 周练甘肃省兰州市第一中学2019-2020学年高一4月月考化学试题黑龙江省绥化市安达市第七中学2019-2020学年高一下学期期中考试化学试题云南省昆明市寻甸县民族中学2019-2020学年高二下学期第一次月考化学试题黑龙江省牡丹江市第一高级中学2019-2020学年高一下学期期末考试化学试题(已下线)1.1.1焓变 反应热(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)1.3.2 反应热的计算(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节 化学反应的热效应 课时2 化学反应的焓变 热化学方程式高中必刷题高二选择性必修1第一章 化学反应的热效应 第一节 反应热 课时1 反应热 焓变 热化学方程式高一必修第二册(人教2019版)第六章 第一节 化学反应与能量变化 课时1 化学反应与能量变化(已下线)第1章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)陕西省西安市西北工业大学附属中学2018-2019学年高一下学期第二次月考化学试题必修第二册RJ第6章第一节 化学反应与能量变化 课时1鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时1 化学反应的反应热、内能变化与焓变吉林省长春市农安县2019-2020学年高一下学期期末考试化学试题辽宁省葫芦岛市第八高级中学2020-2021学年高二上学期实验班第一次月考化学试题陕西省咸阳百灵中学2020-2021学年高二上学期第一次月考化学试题贵州省遵义市航天高级中学2020-2021学年高二上学期第一次月考化学(理)试题安徽省宣城二中2020-2021学年高二上学期第一次月考化学试题江苏省如皋中学2020-2021学年高二上学期第一次阶段检测化学试题甘肃省岷县第二中学2020-2021学年高二上学期第一次月考化学试题福建省福州市八县(市)一中2020-2021学年高二上学期期中联考化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第一节 反应热 课时1 反应热 焓变广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题河南省原阳县第三高级中学2020-2021学年高二上学期第一次月考化学试题福建省永安市第一中学2020-2021学年高二上学期期中考试化学试题湖北省巴东县第二高级中学2020-2021学年高二上学期期中考试化学试题内蒙古巴彦淖尔市临河三中2020-2021学年高二10月考化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP415(2)】【化学】湖北随州市第一中学2020-2021学年高二上学期期中考试化学试题甘肃省天水市第六中学2019-2020学年高二上学期期末考试化学试题(普通班)江西省南昌县莲塘第三中学2020-2021学年高二上学期第一次月考化学试题西藏自治区拉萨市那曲第二高级中学2019-2020学年高一下学期期末考试化学试题云南省大理州祥云县2019-2020学年高二下学期期末统测化学试题安徽省安庆市潜山第二中学2020-2021学年高二上学期第二次月考化学试题新疆哈密市第八中学2019-2020学年高二上学期期中考试化学试题高中化学苏教2019版必修第二册-专题6 第二单元 第1课时 放热反应与吸热反应(鲁科版2019)必修第二册 第2章 化学键 化学反应规律 第2节 化学反应与能量转化 第1课时 化学反应中能量变化的本质及转化形式山西省沁县中学2020-2021学年高二上学期第一次月考化学试题云南省玉溪第二中学2020-2021学年高二上学期期中质量检测化学试题河北省唐山市丰润区第二中学2020-2021学年高二上学期1月月考化学试题河南省汤阴县五一中学2019-2020学年高二上学期期中考试化学试题浙江省山河联盟学校2020-2021学年高一下学期4月月考化学试题 (已下线)【浙江新东方】高中化学20210513-046【2021】【高一下】河南省登封市第一高级中学2019-2020学年高二上学期期中考试化学试题河北省石家庄正中实验中学2020-2021学年高一第二学期第一次月考化学试题四川省达州市大竹中学2020-2021学年高一下学期期中考试化学试题四川省内江市威远中学2020-2021学年高一下学期期中考试化学试题四川省南充市李渡中学2020-2021学年高一下学期期中考试化学试题新疆塔什库尔干塔吉克自治县深塔中学2020-2021学年高二下学期期末考试化学试题河南省许昌市2020-2021学年高二下学期期末质量检测化学试题新疆昌吉教育共同体2020-2021学年高一下学期期末质量检测化学试题选择性必修1(SJ)专题1第一单元易错疑难集训(一)(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)选择性必修1专题1第一单元 课时1 化学反应的焓变(已下线)1.1.1 焓变 反应热-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题1 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)1.1.1 化学反应的焓变(1)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)第1章 化学反应与能量(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)江西省九江一中2020-2021学年高二上学期月考化学试题湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题四川省大竹中学2021-2022学年高二上学期期中达标测化学试题(基础卷)江苏省泰州中学2021-2022学年高二上学期第一次月度检测化学试题陕西省咸阳市武功县普集高级中学2021-2022学年高二上学期第一次月考化学试题北京市中国农业大学附属中学2020-2021学年高一下学期期中学业水平调研化学试题四川省仁寿县四校联考2021-2022学年高二上学期10月月考化学试题甘肃省临夏县中学2021-2022学年高二上学期第一次月考化学(B卷)试题甘肃省临夏县中学2021-2022学年高二上学期第一次月考化学(A卷)试题广东省佛山市南海区桂城中学2021-2022学年高二上学期第一次月考化学试题上海市敬业中学2021-2022学年高三上学期期中考试化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)浙江省温州新力量联盟2021-2022学年高二上学期期中联考化学试题江西省南昌市八一中学、洪都中学等4校2021-2022学年高二上学期期中联考化学试题湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题陕西省榆林市第十二中学2021-2022学年高二上学期教学质量摸底评估化学试题(已下线)1.1.1 反应热 焓变(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第1章 化学反应的热效应(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期中考试化学(理)试题(已下线)二轮拔高卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)四川省南充市南部县第二中学2021-2022学年高二下学期3月月考化学试题课后-6.1.1 化学反应与热能-人教2019必修第二册四川师范大学附属中学安宁校区2021-2022学年高二上学期期中考试化学试题重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题广东省名校联盟2021-2022学年高一下学期4月大联考化学试题河北省衡水市武强中学2021-2022学年高二上学期第三次月考化学试题甘肃省靖远县第一中学2021-2022学年高一下学期4月月考化学试题贵州省黔东南州凯里市第一中学2021-2022学年高一下学期期中化学试题(已下线)北京市第四中学2021-2022学年高一下学期期中考试化学试题黑龙江省哈尔滨市第六中学2021-2022学年高一下学期期中考试(选考)化学试题山东省临沂市罗庄区2021-2022学年高一下学期5月期中考试化学试题广东省江门市蓬江区棠下中学2021-2022学年高一下学期期中考试化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一下学期期末线上测试化学试题四川省广安市2021-2022学年高一下学期期末考试化学试题(已下线)1.1.1 反应热 焓变-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)1.1.2 化学反应的焓变-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第15练 化学反应与能量变化-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高二上学期第一次阶段考试化学试题广东省清远市阳山县南阳中学2021-2022学年高一下学期第二次月考化学试题新疆石河子第一中学2021-2022学年高一下学期4月月考化学试题第一节 反应热 第1课时 反应热 焓变广东省广州市四校联考2022-2023学年高二上学期第一次月考化学试题内蒙古包头市第四中学2020-2021学年高二上学期期中考试化学试题内蒙古包头市第四中学2020-2021学年高二上学期第一次月考化学试题甘肃省永昌县第一高级中学2021-2022高一下学期第一次月考化学试题辽宁省营口市第二高级中学2021-2022学年高一下学期第一次月考化学试题(已下线)1.1.1 反应热(一)-同步学习必备知识黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题甘肃省镇原县第二中学2021-2022学年高二上学期第一次月考化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期末考试化学(理)试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题浙江省舟山市南海实验高中2021-2022学年高一下学期4月月考化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高一下学期期中考试化学试题河北省廊坊市三河市第三中学2021-2022学年高一下学期5月线上考试化学试题四川省凉山州宁南中学2022-2023学年高二上学期第一次月考化学试题内蒙古呼伦贝尔市满洲里远方中学2021-2022学年高一下学期期末考试化学试题广西柳州市第三中学2022-2023学年高二上学期10月月考化学试题云南省昆明市寻甸县第二中学2022-2023学年高二上学期10月月考 化学试卷天津市第九十五中学益中学校2022-2023学年高二上学期期中考试化学试题陕西省汉中市洋县中学2022-2023学年高二上学期期中考试化学试题新疆维吾尔自治区喀什市喀什第二中学2022-2023学年高三上学期网上11月月考化学试题上海市财经大学附属北郊高级中学2022-2023学年高二上学期等级班阶段性检测化学试题浙江省金华市横店高中2022-2023学年高二上学期10月份检测化学试题云南省昆明师范专科学校附属中学2022-2023学年高二上学期期中考试化学试题山东省菏泽市曹县第一中学2022-2023学年高二上学期12月份阶段检测化学试题陕西省汉滨区五里高级中学2022-2023学年高二上学期期中考试化学试题山东省济南市莱钢高级中学2022-2023学年高二上学期期中考试化学试题广西防城港市防城中学2021-2022学年高二上学期期中考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二上学期期中考试化学试题浙江省诸暨市第二高级中学2021-2022学年高二上学期期中考试化学试题山东省济宁市微山县第二中学2021-2022学年高二12月月考化学试题河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期期中考试化学试题河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期9月月考化学试题(已下线)专题十 化学能与热能-实战高考·二轮复习核心突破贵州省黔西南州金成实验学校2021-2022学年高二上学期11月月考试化学试题云南省昆明市昆明行知中学2021-2022学年高二上学期第一次质量检测(10月)化学试题江西省宜春市昌黎实验学校2021-2022学年高二上学期12月月考化学试题广东省潮州湘桥区南春中学2021-2022学年高二上学期第一次月考化学试题 河南省洛阳市第三高级中学2022-2023学年高二上学期12月月考化学试题(已下线)【知识图鉴】单元讲练测必修第二册第六单元02基础练(已下线)题型97 结合能量变化图像或反应历程图像考查能量变化湖南省岳阳市华容县2022-2023学年高二上学期期末考试化学试题四川省内江市第六中学2022-2023学年高一下期第一次月考(创新班)化学试题安徽省安庆市怀宁县第二中学2022-2023学年高二上学期期末考试化学试题福建省福州第一中学2022-2023学年高一下学期4月期中考试化学试题浙江省台州市洪家中学2022-2023学年高一下学期期中考试化学试题云南省昆明市官渡区第三中学2022-2023学年高一下学期期中考试化学试题6.2.1放热反应与吸热反应(课中)-2019苏教版必修2课前课中课后新疆塔城地区第一高级中学2022-2023学年高一下学期5月期中考试化学试题安徽省合肥市庐巢八校联考2022-2023学年高一下学期5月期中化学试题辽宁省鞍山市2023年高中学业水平考试模拟测试化学试题黑龙江省勃利县高级中学2022-2023学年高一下学期5月月考化学试题内蒙古科尔沁左翼中旗实验高级中学2022-2023学年高一下学期期中考试化学试题广东省广州市广外、铁一、广附三校2022-2023学年高一下学期期末联考化学试题广东省江门市广德实验学校2021-2022学年高一下学期期中考试化学试题陕西师范大学附属中学2022-2023学年高一下学期6月期末考试化学试题福建省莆田华侨中学2022-2023学年高一下学期5月月考化学试题云南省开远市第一中学校2022-2023学年高一下学期期末考试化学试题河北省石家庄市第二十七中学2023-2024学年高二上学期第一次月考化学试题广东省华南师范大学附属中学2023-2024学年高三上学期第一次月考化学试题广东省广州市培英中学2023-2024学年高二上学期10月学情分析化学试题四川省泸州市泸县第五中学2023-2024学年高二上学期11月期中考试化学试题江苏省泰州中学2023-2024学年高二上学期期中考试化学试卷上海戏剧学院附属高级中学2023-2024学年高二上学期(第2次)质量监测(等级)化学试卷 天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期竞赛选拔赛化学试题重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)名校期末好题汇编-化学反应与能量(选择题)四川省泸州市泸县第五中学2023-2024学年高一下学期6月月考化学试题
名校
解题方法
8 . 已知:H2X是可溶于水的二元弱酸,MX是难溶于水的盐,M2+不发生水解。25℃时,MX饱和溶液、一定浓度H2X溶液中相关粒子浓度变化的关系如图所示。下列说法正确的是

A.曲线L2表示H2X溶液中-lgc(X2-)与 的变化关系 的变化关系 |
| B.NaHX溶液呈碱性 |
| C.调节MX饱和溶液的pH=7时,溶液中一定存在2c(M2+)=2c(X2-)+c(HX-) |
| D.25℃时,MX 的溶度积Ksp(MX)的数量级为10-7 |
您最近一年使用:0次
2023-05-24更新
|
173次组卷
|
3卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题
名校
解题方法
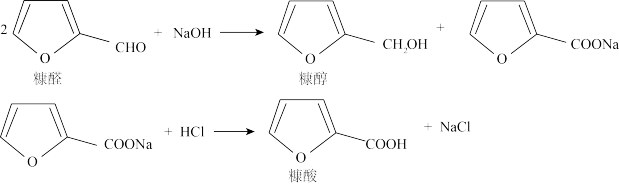
9 . 糠酸(熔点133℃,沸点231℃,在热水中溶解度较大,微溶于冷水)和糠醇(熔点29℃,沸点171℃)均为重要的化工中间体,工业上可利用糠醛(沸点161.7℃,易被氧化)发生歧化反应制取这两种物质(该反应为强放热反应),反应原理如下:
实验步骤:
步骤1:向三颈烧瓶中加入8.2mL(约0.2mol)新蒸馏的糠醛,通过仪器A向三颈烧瓶中缓慢滴加8 mL 33%的NaOH溶液。搅拌并保持反应温度为8~12℃,回流20 min,得到粗产品。
步骤2:将粗产品倒入盛有10 mL水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取4次,分液得到水层和醚层。
步骤3:向水层中分批滴加25%的盐酸,调至溶液的pH= 3,冷却、结晶、抽滤、冷水洗涤,得到糠酸粗品;向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚(乙醚的沸点为34.6℃)和糠醇。

回答下列问题:
(1)仪器A的名称为___________ 。 与直形冷凝管相比,使用仪器B的优点是___________ 。
(2)该反应必须严格控制反应温度为8~12℃ ,实验中采用了哪些保障措施?___________ 。
(3)步骤3中分离乙醚和糠醇的实验操作为___________ 。
(4)步骤3中洗涤粗糠酸用冷水的原因是___________ 。进一步将粗糠酸提纯,应采用的方法是___________ 。
(5)取1.120g提纯后的糠酸样品。配成100mL溶液,准确量取20.00mL于锥形瓶中,加入指示剂,用0.0800mol·L-1NaOH标准溶液滴定,平行滴定三次,平均消耗NaOH标准溶液24.80mL。糠酸的纯度为___________ 。若步骤1中不对糠醛进行蒸馏处理,则会使制得的糠醇的质量___________ (填“增大”或“减小”)。

实验步骤:
步骤1:向三颈烧瓶中加入8.2mL(约0.2mol)新蒸馏的糠醛,通过仪器A向三颈烧瓶中缓慢滴加8 mL 33%的NaOH溶液。搅拌并保持反应温度为8~12℃,回流20 min,得到粗产品。
步骤2:将粗产品倒入盛有10 mL水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取4次,分液得到水层和醚层。
步骤3:向水层中分批滴加25%的盐酸,调至溶液的pH= 3,冷却、结晶、抽滤、冷水洗涤,得到糠酸粗品;向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚(乙醚的沸点为34.6℃)和糠醇。

回答下列问题:
(1)仪器A的名称为
(2)该反应必须严格控制反应温度为8~12℃ ,实验中采用了哪些保障措施?
(3)步骤3中分离乙醚和糠醇的实验操作为
(4)步骤3中洗涤粗糠酸用冷水的原因是
(5)取1.120g提纯后的糠酸样品。配成100mL溶液,准确量取20.00mL于锥形瓶中,加入指示剂,用0.0800mol·L-1NaOH标准溶液滴定,平行滴定三次,平均消耗NaOH标准溶液24.80mL。糠酸的纯度为
您最近一年使用:0次
2023-05-22更新
|
124次组卷
|
2卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题
名校
解题方法
10 . 根据下列事实得出的相应结论错误的是
| 选项 | 事实 | 结论 |
| A | 25℃时分别测定浓度均为0.1mol·L-1的NaCl溶液和CH3COONH4溶液的pH,pH都等于7 | 两溶液中水的电离程度相等 |
| B | t ℃时,反应①:Br2(g)+ H2(g)  2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g) 2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g)  2HI(g) K=43 2HI(g) K=43 | 相同条件下。平衡体系中卤化氢所占的比例:反应①>反应② |
| C | 向漂白粉溶液中通入足量SO2气体,产生白色沉淀 | 还原性:SO2>Cl- |
| D | 常温下,将50mL苯与50mLCH3COOH混合,所得混合液的体积为101 mL | 混合过程中削弱了CH3COOH分子间的氢键。且苯与CH3COOH分子间的范德华力弱于CH3COOH分子间的氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-22更新
|
92次组卷
|
2卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题



