1 . 一种由烯烃合成环氧烷烃的流程如下:
(1)氨的沸点为-33.5℃,氨易液化的原因是_______ 。
(2)钠熔化时破坏的作用力为_______ ;C分子中 键、π键数目之比为
键、π键数目之比为_______ 。
(3)比较熔点:A_______ B(填“高于”或“低于”),判断依据是_______ 。
(4)A和D互为_______ (填“同分异构体”“同素异形体”或“同系物”),A→B的反应类型是_______ 。
(5)E的分子式为_______ ,其所含元素中第一电离能由大到小的顺序为_______ 。

(1)氨的沸点为-33.5℃,氨易液化的原因是
(2)钠熔化时破坏的作用力为
 键、π键数目之比为
键、π键数目之比为(3)比较熔点:A
(4)A和D互为
(5)E的分子式为
您最近一年使用:0次
名校
2 .  、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)与氮氧化物有关的全球或区域性大气环境问题有___________ (填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为___________ 。
(3)NO的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性溶液中,
溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性溶液中, 氧化NO生成
氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
(4)NO和 的处理。工业上用石灰乳吸收已除去
的处理。工业上用石灰乳吸收已除去 的硝酸尾气(含NO、
的硝酸尾气(含NO、 ),既能净化尾气,又能获得应用广泛的
),既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下: 被
被 吸收,反应的化学方程式为
吸收,反应的化学方程式为___________ 。上述工艺中采用气—液逆流接触吸收(尾气从吸收塔底进入,石灰乳从塔顶喷淋),其目的是___________ 。
②生产中溶液需保持弱碱性,在酸性溶液中 会发生分解,产物之一是NO,其反应的离子方程式为
会发生分解,产物之一是NO,其反应的离子方程式为___________ 。
③过滤后的滤液经___________ 、___________ 、过滤、洗涤、干燥,得到无水 。
。
 、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)与氮氧化物有关的全球或区域性大气环境问题有
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(3)NO的氧化吸收。用
 溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性溶液中,
溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性溶液中, 氧化NO生成
氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为(4)NO和
 的处理。工业上用石灰乳吸收已除去
的处理。工业上用石灰乳吸收已除去 的硝酸尾气(含NO、
的硝酸尾气(含NO、 ),既能净化尾气,又能获得应用广泛的
),既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下: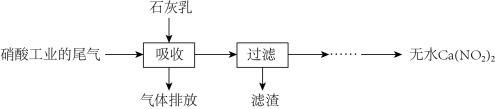
 被
被 吸收,反应的化学方程式为
吸收,反应的化学方程式为②生产中溶液需保持弱碱性,在酸性溶液中
 会发生分解,产物之一是NO,其反应的离子方程式为
会发生分解,产物之一是NO,其反应的离子方程式为③过滤后的滤液经
 。
。
您最近一年使用:0次
3 . 按要求回答下列问题:
(1)已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO +H2O
+H2O H2SO3+OH- ①
H2SO3+OH- ①
HSO
 H++SO
H++SO ②
②
向0.1 mol·L-1的NaHSO3溶液中加入少量NaOH固体,则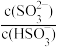
_______ (填“增大”“减小”或“不变”)。
(2)氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。
25 ℃时氯气—氯水体系中存在以下平衡关系:
Cl2(g) Cl2(aq) ①
Cl2(aq) ①
Cl2(aq) + H2O HClO + H+ + Cl- ②
HClO + H+ + Cl- ②
HClO H+ + ClO- ③
H+ + ClO- ③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。_______ ,
由图可知该常数值为_______ 。
②用氯处理饮用水时,夏季的杀菌效果比冬季_______ (填“好”或“差”)。
(1)已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO
 +H2O
+H2O H2SO3+OH- ①
H2SO3+OH- ①HSO

 H++SO
H++SO ②
②向0.1 mol·L-1的NaHSO3溶液中加入少量NaOH固体,则
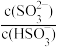
(2)氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。
25 ℃时氯气—氯水体系中存在以下平衡关系:
Cl2(g)
 Cl2(aq) ①
Cl2(aq) ①Cl2(aq) + H2O
 HClO + H+ + Cl- ②
HClO + H+ + Cl- ②HClO
 H+ + ClO- ③
H+ + ClO- ③其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
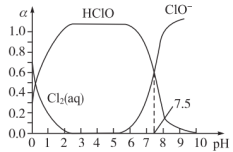
由图可知该常数值为
②用氯处理饮用水时,夏季的杀菌效果比冬季
您最近一年使用:0次
解题方法
4 . 草酸亚铁晶体 ,黄色,难溶于水,可溶于稀
,黄色,难溶于水,可溶于稀 ,有较强还原性。某化学兴趣小组用下列装置制备草酸亚铁晶体并检测其纯度。
,有较强还原性。某化学兴趣小组用下列装置制备草酸亚铁晶体并检测其纯度。 。实验步骤如下:
。实验步骤如下:
第一步:按图连接好装置,检查装置气密性,
第二步:打开______,关闭______(填 或
或 )开始反应,
)开始反应,
第三步:……
第四步:打开 ,关闭
,关闭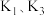 ,使
,使 中溶液进入到
中溶液进入到 中反应,
中反应,
第五步:对B中所得溶液蒸发浓缩,冷却结晶,过滤,洗涤和干燥可得 。
。
请回答下列问题:
(1)请把实验步骤补充完整.
第二步:打开______ ,关闭______ (填 或
或 ;
;
第三步:______ 。
(2)装置 的作用是
的作用是______ 。
II.样品纯度检测
该方法制得的 中可能含有
中可能含有 杂质。
杂质。
(3)写出生成 的化学反应方程式
的化学反应方程式______ 。
采用 滴定法滴定该样品的纯度,步骤如下:
滴定法滴定该样品的纯度,步骤如下:
①取ag样品于锥形瓶中,加入稀 溶解,水浴加热至
溶解,水浴加热至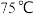 ,用
,用 的
的 溶液趁热滴定至终点,消耗
溶液趁热滴定至终点,消耗 溶液
溶液 。
。
②向上述溶液中加入适量还原剂将 全部还原成
全部还原成 ,加入稀
,加入稀 酸化后,在
酸化后,在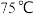 继续用该
继续用该 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。
(4)步骤①中,滴定终点的现象为______ 。
(5)样品中 的质量分数
的质量分数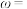
______  。
。
(6)当 和
和 满足
满足______ 关系时,样品中不含 。
。
 ,黄色,难溶于水,可溶于稀
,黄色,难溶于水,可溶于稀 ,有较强还原性。某化学兴趣小组用下列装置制备草酸亚铁晶体并检测其纯度。
,有较强还原性。某化学兴趣小组用下列装置制备草酸亚铁晶体并检测其纯度。
 。实验步骤如下:
。实验步骤如下:第一步:按图连接好装置,检查装置气密性,
第二步:打开______,关闭______(填
 或
或 )开始反应,
)开始反应,第三步:……
第四步:打开
 ,关闭
,关闭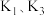 ,使
,使 中溶液进入到
中溶液进入到 中反应,
中反应,第五步:对B中所得溶液蒸发浓缩,冷却结晶,过滤,洗涤和干燥可得
 。
。请回答下列问题:
(1)请把实验步骤补充完整.
第二步:打开
 或
或 ;
;第三步:
(2)装置
 的作用是
的作用是II.样品纯度检测
该方法制得的
 中可能含有
中可能含有 杂质。
杂质。(3)写出生成
 的化学反应方程式
的化学反应方程式采用
 滴定法滴定该样品的纯度,步骤如下:
滴定法滴定该样品的纯度,步骤如下:①取ag样品于锥形瓶中,加入稀
 溶解,水浴加热至
溶解,水浴加热至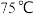 ,用
,用 的
的 溶液趁热滴定至终点,消耗
溶液趁热滴定至终点,消耗 溶液
溶液 。
。②向上述溶液中加入适量还原剂将
 全部还原成
全部还原成 ,加入稀
,加入稀 酸化后,在
酸化后,在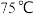 继续用该
继续用该 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。(4)步骤①中,滴定终点的现象为
(5)样品中
 的质量分数
的质量分数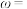
 。
。(6)当
 和
和 满足
满足 。
。
您最近一年使用:0次
5 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是_______ 。
(2)检查装置气密性后加入药品,打开 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到_______ 时,再打开 。
。
(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是_______ ;装置D中除生成硫脲外,还生成一种碱,写出该过程D中发生反应的化学方程式:_______ 。
实验(二):探究硫脲的性质。
(4)①取少量 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加_______ ,可检验是否有 生成。
生成。
②取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
③取少量 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为_______ 。
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为_______ (用含m、c、V的代数式表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: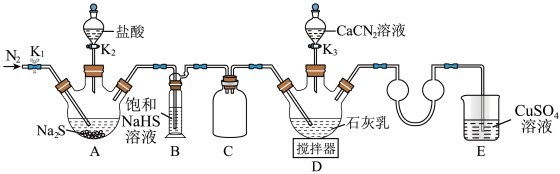
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是
(2)检查装置气密性后加入药品,打开
 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到 。
。(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是
实验(二):探究硫脲的性质。
(4)①取少量
 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加 生成。
生成。②取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成③取少量
 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为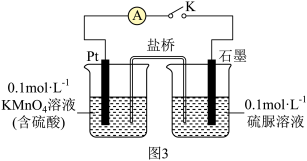
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性
 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
您最近一年使用:0次
2024-06-02更新
|
201次组卷
|
2卷引用:2024届江西省吉安市第一中学高三下学期三模化学试题
名校
解题方法
6 . 根据要求,回答下列问题:
(1)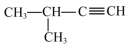 的系统命名是
的系统命名是___________ 。
(2)有机物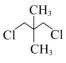 的核磁共振氢谱出现的峰面积之比为
的核磁共振氢谱出现的峰面积之比为___________ 。
(3)画出丁烯C4H8的顺式结构的结构简式___________ 。
(4)某芳香烃的结构为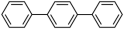 ,一氯代物有
,一氯代物有___________ 种。
(5)梯恩梯(TNT)结构简式为___________ 。
(6)某卤代烃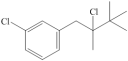 与氢氧化钠醇溶液加热反应,会生成
与氢氧化钠醇溶液加热反应,会生成___________ 种有机产物;通常情况下 该卤代烃与氢氧化钠水溶液加热反应,会消耗
该卤代烃与氢氧化钠水溶液加热反应,会消耗___________ 
 。
。
(7)胡椒酚是一种植物挥发油,它的结构简式为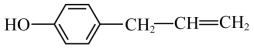 ,回答下列问题。
,回答下列问题。
① 胡椒酚与足量饱和溴水发生反应,理论上最多消耗
胡椒酚与足量饱和溴水发生反应,理论上最多消耗___________ mol 。
。
②若要制备胡椒酚钠,可以选择的试剂有___________ (填序号)。
A.Na B. C.
C. D.
D.
(8)已知: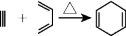 ,如果要合成
,如果要合成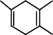 ,所用的原料可以是(双选)___________。
,所用的原料可以是(双选)___________。
(1)
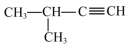 的系统命名是
的系统命名是(2)有机物
 的核磁共振氢谱出现的峰面积之比为
的核磁共振氢谱出现的峰面积之比为(3)画出丁烯C4H8的顺式结构的结构简式
(4)某芳香烃的结构为
 ,一氯代物有
,一氯代物有(5)梯恩梯(TNT)结构简式为
(6)某卤代烃
 与氢氧化钠醇溶液加热反应,会生成
与氢氧化钠醇溶液加热反应,会生成 该卤代烃与氢氧化钠水溶液加热反应,会消耗
该卤代烃与氢氧化钠水溶液加热反应,会消耗
 。
。(7)胡椒酚是一种植物挥发油,它的结构简式为
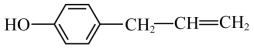 ,回答下列问题。
,回答下列问题。①
 胡椒酚与足量饱和溴水发生反应,理论上最多消耗
胡椒酚与足量饱和溴水发生反应,理论上最多消耗 。
。②若要制备胡椒酚钠,可以选择的试剂有
A.Na B.
 C.
C. D.
D.
(8)已知:
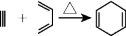 ,如果要合成
,如果要合成 ,所用的原料可以是(双选)___________。
,所用的原料可以是(双选)___________。| A.2-甲基-l,3-丁二烯和2-丁炔 |
| B.1,3-戊二烯和2-丁炔 |
| C.2,3-二甲基-1,3-戊二烯和乙炔 |
| D.2,3-二甲基-l,3-丁二烯和1-丙炔 |
您最近一年使用:0次
7 . 利用反应: 设计了如图所示的原电池。回答下列问题:
设计了如图所示的原电池。回答下列问题:___________ ,电极方程式为:___________ ,发生___________ 反应。
(2)X是___________ ,Y是___________ 。
(3)正极上出现的现象是___________ ;电极方程式为:___________ 。
 设计了如图所示的原电池。回答下列问题:
设计了如图所示的原电池。回答下列问题: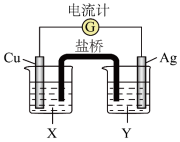
(2)X是
(3)正极上出现的现象是
您最近一年使用:0次
8 . 根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
名校
9 . 已知有烃分子:① ;②
;②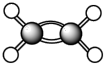 ;③
;③ ;④
;④ ;⑤
;⑤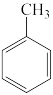 ;⑥
;⑥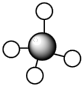 。
。
(2)写出②在一定条件下与水反应的化学方程式为:
(3)与④互为同系物的是
(4)③的二氯代物有
(5)写出⑤的分子式:
(6)乙烯能发生聚合反应,该反应产物的用途之一是
您最近一年使用:0次
名校
10 . 请按要求回答下列问题:
(1)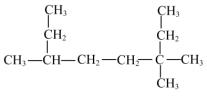 系统命名为
系统命名为________ 。
(2)三元乙丙橡胶的一种单体的键线式为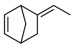 ,它的分子式为
,它的分子式为_______ 。
(3)A的化学式为 ,已知A只有一种类型的氢原子:则A的结构简式为
,已知A只有一种类型的氢原子:则A的结构简式为_______ 。
(4)某烃的分子式为 ,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式
,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式______ ,此反应类型为______ 。
(5)请写出环己烷(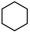 )与
)与 在光照条件下生成一氯环己烷的化学方程式
在光照条件下生成一氯环己烷的化学方程式_______ 。
(6)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系: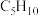 ,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是______ 。
(1)
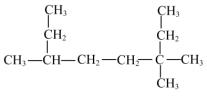 系统命名为
系统命名为(2)三元乙丙橡胶的一种单体的键线式为
 ,它的分子式为
,它的分子式为(3)A的化学式为
 ,已知A只有一种类型的氢原子:则A的结构简式为
,已知A只有一种类型的氢原子:则A的结构简式为(4)某烃的分子式为
 ,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式
,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式(5)请写出环己烷(
 )与
)与 在光照条件下生成一氯环己烷的化学方程式
在光照条件下生成一氯环己烷的化学方程式(6)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
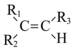
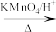
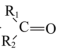 +R3COOH
+R3COOH
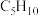 ,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
您最近一年使用:0次



