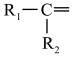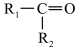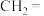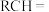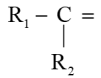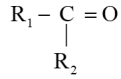名校
解题方法
1 . 回答下列问题:
I.下表中的数据是破坏1 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题
(1)下列氢化物中最稳定的是___________ (填标号)。
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI___________ (填“吸收”或“放出”)的热量为___________ kJ。
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)
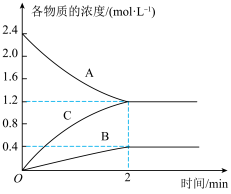
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:___________ ;
(5)从开始至2min末,A的平均反应速率为___________ ;
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________ 。
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
I.下表中的数据是破坏1
 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题| 物质 |  |  |  |  |  |  |  |
| 键能/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列氢化物中最稳定的是
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)

| A.NaOH+HCl=NaCl+H2O |
| B.Fe+H2SO4=FeSO4+H2↑ |
| C.2Na2O2+2H2O=4NaOH+O2↑ |
| D.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O |
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:
(5)从开始至2min末,A的平均反应速率为
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近一年使用:0次
名校
2 . 合理开发和利用自然资源是人类赖以生存的基础。回答下列问题:
Ⅰ.金属矿物的开发利用。
(1)金属的冶炼有多种方法,工业炼铁可采用___________ (填“电解法”“热还原法”或“热分解法”)。
(2)已知MgO、 的熔、沸点数据如表所示:
的熔、沸点数据如表所示:
通过电解法冶炼镁时应选用熔融的___________ (填化学式),不选用另一种物质的原因为___________ 。
Ⅱ.海水资源的开发利用。
(3)任写一种工业上海水淡化的方法:___________ 。
(4)NaCl是海水的主要溶质,可用于制备很多重要的化工原料,制备物质___________ (填选项字母)的主要过程中不涉及氧化还原反应。
A.纯碱 B.氯气 C.钠
Ⅲ.化石能源的综合利用。
(5)煤、石油和天然气(主要成分为甲烷)是重要的化石能源,其中石油分馏后的产物进行裂解后可得到 、
、 、
、 、
、 等重要的化工原料。
等重要的化工原料。
①煤的干馏和石油的分馏均是从化石能源中获得重要化工原料的手段,其中不涉及化学变化的是___________ 。
②上述四种有机物中与甲烷互为同系物的是___________ (填化学式)。
③ 燃料碱性电池工作原理如图所示。乙电极为电源的
燃料碱性电池工作原理如图所示。乙电极为电源的___________ (填“正极”或“负极”),甲电极上的电极反应式为___________ ;电池工作时,当外电路中通过0.3mol电子时,理论上消耗 在标准状况下的体积为
在标准状况下的体积为___________ L。
Ⅰ.金属矿物的开发利用。
(1)金属的冶炼有多种方法,工业炼铁可采用
(2)已知MgO、
 的熔、沸点数据如表所示:
的熔、沸点数据如表所示:| 物质 | MgO |  |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
Ⅱ.海水资源的开发利用。
(3)任写一种工业上海水淡化的方法:
(4)NaCl是海水的主要溶质,可用于制备很多重要的化工原料,制备物质
A.纯碱 B.氯气 C.钠
Ⅲ.化石能源的综合利用。
(5)煤、石油和天然气(主要成分为甲烷)是重要的化石能源,其中石油分馏后的产物进行裂解后可得到
 、
、 、
、 、
、 等重要的化工原料。
等重要的化工原料。①煤的干馏和石油的分馏均是从化石能源中获得重要化工原料的手段,其中不涉及化学变化的是
②上述四种有机物中与甲烷互为同系物的是
③
 燃料碱性电池工作原理如图所示。乙电极为电源的
燃料碱性电池工作原理如图所示。乙电极为电源的 在标准状况下的体积为
在标准状况下的体积为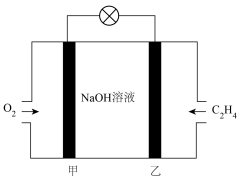
您最近一年使用:0次
名校
解题方法
3 . 请回答下列问题:
(1)脱落酸是一种植物激素,结构简式为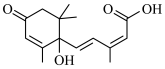 ,其中含有的官能团有
,其中含有的官能团有___________ 种。
(2)烷烃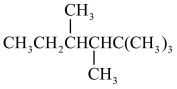 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为___________ ,其一氯代物有___________ 种。若该烃由一种炔烃加氢而成,则该炔烃的结构简式为___________ 。
(3)以烯烃A( )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:
ⅱ.共轭二烯烃可发生1,2-加成和1,4-加成。
①物质A的系统命名为___________ ;B的同分异构体中,与其碳骨架相同的共有___________ 种。
②物质C与氢气反应,得到的产物最多可能有___________ 种。
③C与适量酸性KMnO4溶液作用后得到的有机氧化产物的结构简式为___________ 。
(1)脱落酸是一种植物激素,结构简式为
 ,其中含有的官能团有
,其中含有的官能团有(2)烷烃
 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为(3)以烯烃A(
 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示: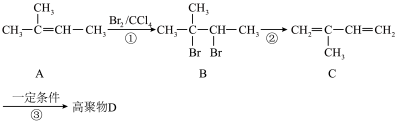
| 烯烃被氧化的部位 | 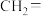 | 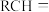 |
|
| 对应的氧化产物 |  | RCOOH |
|
①物质A的系统命名为
②物质C与氢气反应,得到的产物最多可能有
③C与适量酸性KMnO4溶液作用后得到的有机氧化产物的结构简式为
您最近一年使用:0次
名校
4 . 请回答下列问题:
(1)脱落酸是一种植物激素,结构简式为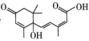 ,其中含有的官能团有
,其中含有的官能团有______ 种。
(2)烷烃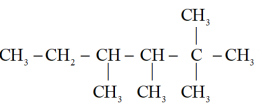 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为______ ,其一氯代物有______ 种。若该烃由一种炔烃加氢而成,则该炔烃的结构简式为______ 。
(3)以烯烃A(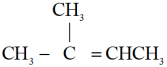 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:
已知:ⅰ.烯烃中的不饱和键在酸性高锰酸钾溶液作用下对应的产物如下表所示。
ⅱ.共轭二烯烃可发生1,2-加成和1,4-加成。
①物质A的系统命名为______ ;B的同分异构体中,与其碳骨架相同的共有______ 种。
②物质C与氢气反应,得到的产物最多可能有______ 种;C→D通过1,4-加成的方式聚合,该反应的化学方程式为______ 。
③C与适量酸性 溶液作用后得到的有机氧化产物的结构简式为
溶液作用后得到的有机氧化产物的结构简式为______ 。
(1)脱落酸是一种植物激素,结构简式为
 ,其中含有的官能团有
,其中含有的官能团有(2)烷烃
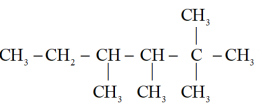 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为(3)以烯烃A(
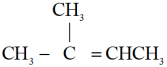 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:

已知:ⅰ.烯烃中的不饱和键在酸性高锰酸钾溶液作用下对应的产物如下表所示。
烯烃被氧化的部位 |
|
|
|
对应的氧化产物 |
| RCOOH |
|
①物质A的系统命名为
②物质C与氢气反应,得到的产物最多可能有
③C与适量酸性
 溶液作用后得到的有机氧化产物的结构简式为
溶液作用后得到的有机氧化产物的结构简式为
您最近一年使用:0次
5 . 将锌粒放入含有 、
、 、
、 三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
(1)请写出反应过程中一定发生反应的化学方程式____ 。
(2)若某次实验后小强对滤液中溶质的成分小强作出了以下猜想: 、
、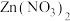 、
、 ,老师说小强的猜想不合理。请你写出该猜想不合理的原因
,老师说小强的猜想不合理。请你写出该猜想不合理的原因________ 。
 、
、 、
、 三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。(1)请写出反应过程中一定发生反应的化学方程式
(2)若某次实验后小强对滤液中溶质的成分小强作出了以下猜想:
 、
、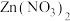 、
、 ,老师说小强的猜想不合理。请你写出该猜想不合理的原因
,老师说小强的猜想不合理。请你写出该猜想不合理的原因
您最近一年使用:0次
名校
解题方法
6 . 按要求填空:
(1)现有8个微粒: ;
; ;
;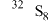 ;
;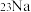 ;
; ;
; ;
; ;
; ;
;
表示核素的符号共_________ 种;互为同位素的是_____________ ;
(2)现有以下物质:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;
;
其中由离子键和非极性共价键构成的物质是_____________ (填序号,下同);属于共价化合物的是_____________ ;
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水;
化学键未被破坏的是_____________ (填序号,下同);离子键被破坏是_____________ ;
(4)以下物质:①金刚石与 ;②
;② 与
与 ;③
;③ 和
和 ;④
;④ 和
和 ;⑤乙烯和乙烷;⑥乙醇
;⑤乙烯和乙烷;⑥乙醇 和甲醚
和甲醚 ;
;
互为同素异形体的是_____________ (填序号,下同);
互为同系物是_____________ ;
互为同分异构体的是_____________ 。
(1)现有8个微粒:
 ;
; ;
;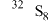 ;
;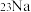 ;
; ;
; ;
; ;
; ;
;表示核素的符号共
(2)现有以下物质:①
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;
;其中由离子键和非极性共价键构成的物质是
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水;
化学键未被破坏的是
(4)以下物质:①金刚石与
 ;②
;② 与
与 ;③
;③ 和
和 ;④
;④ 和
和 ;⑤乙烯和乙烷;⑥乙醇
;⑤乙烯和乙烷;⑥乙醇 和甲醚
和甲醚 ;
;互为同素异形体的是
互为同系物是
互为同分异构体的是
您最近一年使用:0次
解题方法
7 . 元素周期表可以用于探寻各种元素间的内在联系。
(1)下列关于元素周期表的说法错误的是______ 。
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是______ 。
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式_______ 。
②写出Si在元素周期表中的位置_______ 。由碳族元素结构特点,可推测Pb3O4中Pb的化合价为_____ 。
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为______ 。
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=____ 。向其中通入一定量的氯气发生反应,当c(Fe2+):c(Cl﹣)=1:4时,离子方程式为_____ 。
(1)下列关于元素周期表的说法错误的是
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式
②写出Si在元素周期表中的位置
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=
您最近一年使用:0次
8 . 短周期主族元素T的一种氧化物为TO2。根据下列信息回答相关问题:
(1)若T位于第三周期ⅣA族,则T的简单氢化物的电子式为________ 。含有TO2的材料在碱性土壤中会“短路”,其原因是______________ (用离子方程式表示)。
(2)若TO2气体具有刺激性气味,通入酸性KMnO4溶液中,溶液由紫红色变为无色。食品中添加适量TO2可起到防腐和抗氧化作用,则TO2的化学式为_________ ,常温下,TO2与T的简单氢化物不能大量共存,原因是__________________ (用化学方程式表示)。
(3)常温下,若TO2是红棕色气体。在针管实验中,乙管中充满TO2,使甲管中物质和乙管中物质反应。_________ (填标号)。
A.若甲管中充满KI–淀粉溶液,则溶液变蓝
B.若甲管中充满FeCl2溶液,则溶液变黄色
C.若甲管中充满H2S,则颜色无明显变化
(4)若将无色无味的TO2气体持续通入澄清石灰水中,石灰水先变浑浊,后变澄清。TO2和T的单质的反应是________ (填“吸热”或“放热”)反应。将TO2通入棉花包裹的Na2O2粉末中,过一会儿,棉花燃烧起来。由此推知,TO2和Na2O2反应的能量变化符合图_________ (填“Ⅰ”或“Ⅱ”)。
(1)若T位于第三周期ⅣA族,则T的简单氢化物的电子式为
(2)若TO2气体具有刺激性气味,通入酸性KMnO4溶液中,溶液由紫红色变为无色。食品中添加适量TO2可起到防腐和抗氧化作用,则TO2的化学式为
(3)常温下,若TO2是红棕色气体。在针管实验中,乙管中充满TO2,使甲管中物质和乙管中物质反应。

A.若甲管中充满KI–淀粉溶液,则溶液变蓝
B.若甲管中充满FeCl2溶液,则溶液变黄色
C.若甲管中充满H2S,则颜色无明显变化
(4)若将无色无味的TO2气体持续通入澄清石灰水中,石灰水先变浑浊,后变澄清。TO2和T的单质的反应是

您最近一年使用:0次
解题方法
9 . 硫酸是一种重要的化工产品。回答下列问题:
Ⅰ.实验室利用硫酸可以制备一系列气体。
(1)常温下,实验室制备下列气体选择的药品正确的是______(填标号)。
(2)实验室常用食盐和浓硫酸共热500℃制备HCl,另一种产物为正盐,该反应的化学方程式为________ 。不能用浓硫酸制备HBr、HI,其原因是__________________ 。
Ⅱ.硫酸是一种常用的酸性电解质。
(3)在Cu-Zn-H2SO4溶液构成的原电池中,物理量Y与转移电子的关系如图所示。
(4)铅蓄电池的装置如图所示。放电过程的电池反应:PbO2+Pb+2H2SO4=2PbSO4(难溶)+2H2O。________ (填化学式),该极发生_______ (填“氧化”或“还原”)反应。
②正极的电极反应式为______________ 。
③放电时,电解质溶液的pH________ (填“升高”“降低”或“不变”)。
Ⅰ.实验室利用硫酸可以制备一系列气体。
(1)常温下,实验室制备下列气体选择的药品正确的是______(填标号)。
| 选项 | 药品 | 气体 |
| A | FeS、稀硫酸 | H2S |
| B | Na2SO3、10%硫酸 | SO2 |
| C | 粗锌、浓硫酸 | H2 |
| D | 大理石、硫酸 | CO2 |
| A.A | B.B | C.C | D.D |
(2)实验室常用食盐和浓硫酸共热500℃制备HCl,另一种产物为正盐,该反应的化学方程式为
Ⅱ.硫酸是一种常用的酸性电解质。
(3)在Cu-Zn-H2SO4溶液构成的原电池中,物理量Y与转移电子的关系如图所示。
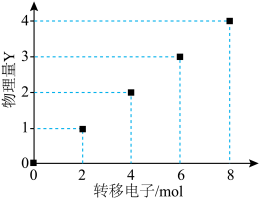
| A.n(Zn) | B.n(H2) | C.n( ) ) | D.n(Zn2+) |
(4)铅蓄电池的装置如图所示。放电过程的电池反应:PbO2+Pb+2H2SO4=2PbSO4(难溶)+2H2O。
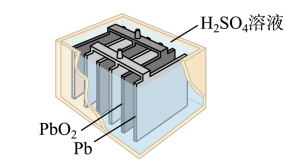
②正极的电极反应式为
③放电时,电解质溶液的pH
您最近一年使用:0次
10 . 某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同,并说明原因?_______ 。
(2)指出铝和石墨的电极并写出实验3中的电极反应式和电池总反应方程式。铝为___ 极,2Al-6e-=2Al3+;石墨为___ 极,6H++6e-=3H2↑;电池总反应:____ 。
(3)实验4中的铝作正极还是负极?_______ ,为什么? _______ 。
(4)根据实验结果总结:在原电池中金属铝作正极还是负极受到哪些因素的影响?_____ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中Al所作的电极是否相同,并说明原因?
(2)指出铝和石墨的电极并写出实验3中的电极反应式和电池总反应方程式。铝为
(3)实验4中的铝作正极还是负极?
(4)根据实验结果总结:在原电池中金属铝作正极还是负极受到哪些因素的影响?
您最近一年使用:0次