名校
1 . 根据所学知识,回答下列问题。
(1)已知反应: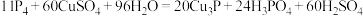 在该反应中,氧化剂是
在该反应中,氧化剂是_______ (填化学式),被氧化的元素是_______ (填元素符号)。
(2)下列状态的物质,既属于电解质又能导电的是_______。(填标号)
(3) 是人体必需的微量元素,其中
是人体必需的微量元素,其中 的中子数是
的中子数是_______ ,其氢化物 的结构式为
的结构式为_______ 。
(4)写出炽热的碳与浓硫酸反应的化学方程式_______ 。
(5)已知反应: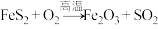 (未配平),若生成标准状况下
(未配平),若生成标准状况下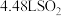 ,则转移的电子数为
,则转移的电子数为_______ 。
(6)往碘化钾溶液中通入少量 ,所发生的离子方程式
,所发生的离子方程式_______ 。
(1)已知反应:
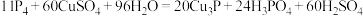 在该反应中,氧化剂是
在该反应中,氧化剂是(2)下列状态的物质,既属于电解质又能导电的是_______。(填标号)
| A.氯化镁晶体 | B.氯化钠溶液 | C.液态氯化氢 | D.熔融氢氧化钾 |
 是人体必需的微量元素,其中
是人体必需的微量元素,其中 的中子数是
的中子数是 的结构式为
的结构式为(4)写出炽热的碳与浓硫酸反应的化学方程式
(5)已知反应:
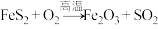 (未配平),若生成标准状况下
(未配平),若生成标准状况下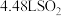 ,则转移的电子数为
,则转移的电子数为(6)往碘化钾溶液中通入少量
 ,所发生的离子方程式
,所发生的离子方程式
您最近一年使用:0次
名校
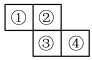
2 . 如图所示为元素周期表前三周期的一部分,①②③④各代表一种元素,其中②的单质约占空气体积的21%。
(1)①的元素符号是______ 。
(2)②和③的原子半径大小关系为:②______ ③(填“>”或“<”)。
(3)③和④的最高价氧化物对应水化物的酸性强弱关系为:③______ ④(填“>”或“<”)。
(4)①的简单氢化物和④的氢化物反应的化学方程式为______ 。
(1)①的元素符号是
(2)②和③的原子半径大小关系为:②
(3)③和④的最高价氧化物对应水化物的酸性强弱关系为:③
(4)①的简单氢化物和④的氢化物反应的化学方程式为
您最近一年使用:0次
名校
3 . 甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
(1)从物质分类标准看,“铜绿”属于______(填字母)。
(2)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式______ 。
(3)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应: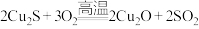 ;
; 第一个反应中生成2molSO2时,转移的电子数是
第一个反应中生成2molSO2时,转移的电子数是______ mol,第二个反应中氧化剂有______ 。如把红色的Cu2O固体放入稀硫酸中,溶液显蓝色,反应的离子方程式如⁻下: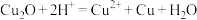 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目______ 。
(4)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为______ 。
 ,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
,“铜绿”能跟酸反应生成铜盐、CO2和H2O。(1)从物质分类标准看,“铜绿”属于______(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
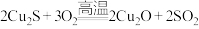 ;
; 第一个反应中生成2molSO2时,转移的电子数是
第一个反应中生成2molSO2时,转移的电子数是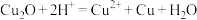 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目(4)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近一年使用:0次
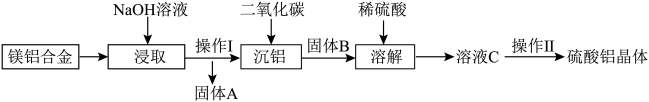
4 . 镁铝合金废料转化为硫酸铝晶体流程如下:
(1) 属于
属于________ (填“酸雨”或“温室效应”)气体。
(2)操作Ⅰ的名称为________ (填“过滤”或“分液”)。
(3)固体A的主要成分为________ (填“Mg”或“Al”)。
(4) 和
和 在一定条件下可转化为甲烷,其反应方程式为
在一定条件下可转化为甲烷,其反应方程式为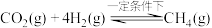
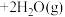 。一定条件下,将
。一定条件下,将
 和
和
 充入2L密闭容器中,10s后测得
充入2L密闭容器中,10s后测得 为0.6mol。则:
为0.6mol。则:
①0~10s内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为________  ;
;
②其他条件不变时,升高温度,该反应的反应速率将________ (填“增大”或“减小”)。
(1)
 属于
属于(2)操作Ⅰ的名称为
(3)固体A的主要成分为
(4)
 和
和 在一定条件下可转化为甲烷,其反应方程式为
在一定条件下可转化为甲烷,其反应方程式为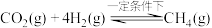
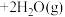 。一定条件下,将
。一定条件下,将
 和
和
 充入2L密闭容器中,10s后测得
充入2L密闭容器中,10s后测得 为0.6mol。则:
为0.6mol。则:①0~10s内,用
 表示该反应的平均反应速率为
表示该反应的平均反应速率为 ;
;②其他条件不变时,升高温度,该反应的反应速率将
您最近一年使用:0次
解题方法
5 . 糖类、油脂和蛋白质均为重要的营养物质。请回答下列问题:
(1)葡萄糖、花生油、蛋白质中属于高分子的是___________ 。
(2)油脂水解后可得到高级脂肪酸和甘油,硬脂酸(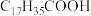 )是一种常见的高级脂肪酸,其官能团名称为
)是一种常见的高级脂肪酸,其官能团名称为___________ 。
(3)若糖代谢功能紊乱,其血液和尿液中葡萄糖含量会超过正常范围,通常可用于检验葡萄糖的试剂为___________ (填“新制氢氧化铜”或“稀硫酸”)。
(1)葡萄糖、花生油、蛋白质中属于高分子的是
(2)油脂水解后可得到高级脂肪酸和甘油,硬脂酸(
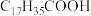 )是一种常见的高级脂肪酸,其官能团名称为
)是一种常见的高级脂肪酸,其官能团名称为(3)若糖代谢功能紊乱,其血液和尿液中葡萄糖含量会超过正常范围,通常可用于检验葡萄糖的试剂为
您最近一年使用:0次
6 . 铁是重要的常见金属材料,也是人类较早使用的金属之一。完成下列问题:
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,配平其化学方程式: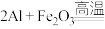
______ 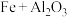 。
。
(2)向20 mL的沸水中逐滴滴加5~6滴FeCl3饱和溶液,继续煮沸至观察到透明的红褐色。此分散系分散质中粒子直径的范围是______ (填“<1”或“1~100”)nm。
(3)电子工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。上述事实利用了FeCl3溶液的______ (填“氧化性”或“还原性”)。
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,配平其化学方程式:
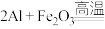
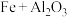 。
。(2)向20 mL的沸水中逐滴滴加5~6滴FeCl3饱和溶液,继续煮沸至观察到透明的红褐色。此分散系分散质中粒子直径的范围是
(3)电子工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。上述事实利用了FeCl3溶液的
您最近一年使用:0次
解题方法
7 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是________ (填“ ”或“
”或“ ”)。
”)。
(1)钠在空气中燃烧生成
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
8 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是_______ 。
(2)检查装置气密性后加入药品,打开 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到_______ 时,再打开 。
。
(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是_______ ;装置D中除生成硫脲外,还生成一种碱,写出该过程D中发生反应的化学方程式:_______ 。
实验(二):探究硫脲的性质。
(4)①取少量 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加_______ ,可检验是否有 生成。
生成。
②取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
③取少量 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为_______ 。
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为_______ (用含m、c、V的代数式表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: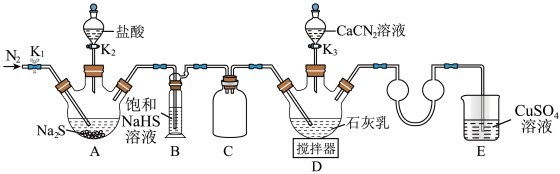
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是
(2)检查装置气密性后加入药品,打开
 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到 。
。(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是
实验(二):探究硫脲的性质。
(4)①取少量
 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加 生成。
生成。②取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成③取少量
 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为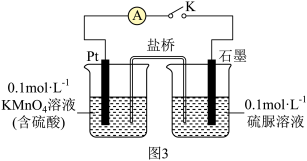
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性
 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
您最近一年使用:0次
2024-06-02更新
|
206次组卷
|
2卷引用:湖南省长沙市雅礼中学2024届高三下学期模拟考卷(二)化学试题
9 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次
10 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维,用于制造光导纤维的基本原料是___________ (填“SiO2”或“Si”);
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用,已知“84”消毒液的制备原理为Cl2+2NaOH=NaCl+NaClO+H2O,则“84”消毒液的有效成分为___________ (填“NaCl”或“NaClO”);
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成该反应的化学方程式:2CO+2NO 2CO2+
2CO2+___________ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维,用于制造光导纤维的基本原料是
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用,已知“84”消毒液的制备原理为Cl2+2NaOH=NaCl+NaClO+H2O,则“84”消毒液的有效成分为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成该反应的化学方程式:2CO+2NO
 2CO2+
2CO2+
您最近一年使用:0次



