名校
解题方法
1 . 现有一定量(NH4)2SO4和NH4NO3的混合溶液,向该混合溶液中逐滴加入Ba(OH)2溶液,加热使之充分反应,直至Ba(OH)2溶液过量。图甲表示产生沉淀的质量与加入Ba(OH)2溶液的体积之间的关系,图乙表示放出NH3的体积(标准状况下)与加入Ba(OH)2溶液的体积之间的关系(假设NH3全部放出)。

(1)混合溶液中NH 的物质的量为
的物质的量为_____ mol。
(2)混合溶液中NO 的物质的量为
的物质的量为_____ mol。
(3)当加入的Ba(OH)2溶液的体积在100~200mL之间时,发生反应的离子方程式为______ 。
(4)若向原混合溶液中一次性加入同浓度的Ba(OH)2溶液200mL,则发生反应的离子方程式为______ 。

(1)混合溶液中NH
 的物质的量为
的物质的量为(2)混合溶液中NO
 的物质的量为
的物质的量为(3)当加入的Ba(OH)2溶液的体积在100~200mL之间时,发生反应的离子方程式为
(4)若向原混合溶液中一次性加入同浓度的Ba(OH)2溶液200mL,则发生反应的离子方程式为
您最近一年使用:0次
2023-04-03更新
|
265次组卷
|
2卷引用:四川省资阳市乐至中学2022-2023学年高一下学期3月月考化学试题
解题方法
2 . 把1mol X气体和0.5mol Y气体混合于2L密闭容器中,发生如下反应:3X(g)+Y(g) nZ(g)+2W(g),2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2min内,用X表示的平均反应速率________ ;
(2)2min末时Y的转化率_______ ;
(3)化学方程式中Z的化学计量数n=______ 。
 nZ(g)+2W(g),2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:(1)前2min内,用X表示的平均反应速率
(2)2min末时Y的转化率
(3)化学方程式中Z的化学计量数n=
您最近一年使用:0次
2020-10-15更新
|
507次组卷
|
12卷引用:2014-2015学年四川省资阳市高一下学期期末质量检测化学试卷
2014-2015学年四川省资阳市高一下学期期末质量检测化学试卷甘肃省镇原县二中2018-2019学年高二上学期期末考试化学试题新疆昌吉回族自治州玛纳斯县第一中学2018-2019学年高二上学期第一次月考化学试题课时1 化学反应的速率——A学习区 夯实基础(人教版必修2)课时1 化学反应的速率——A学习区 夯实基础(人教版(2019)第二册)课时1 化学反应的快慢——A学习区 夯实基础(鲁科版(2019)第二册)课时1 化学反应的快慢——A学习区 夯实基础(鲁科版必修2)黑龙江省海林市朝鲜族中学2019-2020学年高一下学期期末考试化学试题必修第二册RJ第6章第二节 化学反应的速率与限度 课时1黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题黑龙江省绥化市青冈县第一中学2020-2021学年高二上学期10月月考(筑梦班)化学试题(已下线)第13讲 化学反应速率(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
3 . 将一定质量的铁粉加入装有100 mL某浓度稀硝酸的容器中充分反应。试回答:
(1)容器中剩余mg铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中溶质的化学式为__________ 。
②原稀硝酸的物质的量浓度为__________ 。
(2)向(1)中所得的固液混合物中逐滴滴加稀硫酸至刚好不再产生遇空气变成红棕色的气体为止,此时容器中剩余铁粉ng。
①此时溶液中溶质的化学式为__________ 。
②m-n的值为_______ (精确到0.1)。
(1)容器中剩余mg铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中溶质的化学式为
②原稀硝酸的物质的量浓度为
(2)向(1)中所得的固液混合物中逐滴滴加稀硫酸至刚好不再产生遇空气变成红棕色的气体为止,此时容器中剩余铁粉ng。
①此时溶液中溶质的化学式为
②m-n的值为
您最近一年使用:0次
2018-04-22更新
|
388次组卷
|
6卷引用:2016-2017学年四川省资阳中学高一下学期3月月考化学试卷
2016-2017学年四川省资阳中学高一下学期3月月考化学试卷2015-2016学年青海省平安县第一高中高一入学化学试卷辽宁省六校协作体2017-2018学年高一下学期开学考试化学试题甘肃省武威市第六中学2017-2018学年高一下学期第一次学段考试(理)化学试题2019年广东省汕头市高三第一次模拟考试化学试题(已下线)3.3.3 硝酸的性质 人类活动对氮循环和环境的影响练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)
4 . 某有机物含C、H、O中的两种或三种元素,为了测定A的结构,做如下实验:
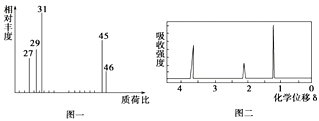
①将2.3g该有机物在足量O2中完全燃烧,将所得混合气体依次通过足量浓硫酸和碱石灰,分别增重2.7 g和4.4 g ;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物得如图二所示图谱,图中三个峰的面积之比是1∶2∶3。(要有计算过程)
(1)有机物A的分子式。
(2)写出A的结构简式。

①将2.3g该有机物在足量O2中完全燃烧,将所得混合气体依次通过足量浓硫酸和碱石灰,分别增重2.7 g和4.4 g ;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物得如图二所示图谱,图中三个峰的面积之比是1∶2∶3。(要有计算过程)
(1)有机物A的分子式。
(2)写出A的结构简式。
您最近一年使用:0次
解题方法
5 . 3.84 g Fe和Fe2O3的混合物溶于100 mL某浓度的盐酸中,恰好使混合物溶解,生成0.03 mol H2,向反应后的溶液中加入KSCN检验,溶液无明显现象,设HCl无挥发,反应后溶液的体积不变。(已知:氧化性Fe3+>H+,还原性Fe>Cl-)
(1)求标准状况下生成氢气的体积______ ?
(2)求反应后Cl-的物质的量浓度_______ ?
(1)求标准状况下生成氢气的体积
(2)求反应后Cl-的物质的量浓度
您最近一年使用:0次
6 . 某温度下,将H2(g)和I2(g)各1 mol的气态混合物充入2 L的密闭容器中,充分反应,5 min后达到平衡,测得c(HI)=0.2 mol/L。
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率。
(2)求该反应的平衡常数。
(3)保持温度不变,若向上述容器中充入H2(g)和I2(g)各2 mol,求达到平衡时I2(g)的物质的量浓度。
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率。
(2)求该反应的平衡常数。
(3)保持温度不变,若向上述容器中充入H2(g)和I2(g)各2 mol,求达到平衡时I2(g)的物质的量浓度。
您最近一年使用:0次
2017-02-17更新
|
887次组卷
|
4卷引用:2016-2017学年四川省资阳市高二上学期期末化学试卷
7 . 把5.1 g镁铝合金的粉末放入过量的300 mL 2 mol·L-1盐酸中,得到5.6 L H2(标准状况下)。试计算:
(1)该合金中铝和镁的物质的量之比。
(2)在反应后的溶液中加入4 mol·L-1 NaOH溶液,若要使沉淀量达到最大值,则加入的NaOH溶液的体积为多少?
(1)该合金中铝和镁的物质的量之比。
(2)在反应后的溶液中加入4 mol·L-1 NaOH溶液,若要使沉淀量达到最大值,则加入的NaOH溶液的体积为多少?
您最近一年使用:0次
8 .
(1)将117 g NaCl溶于水配制成1 L溶液,该溶液中NaCl的物质的量浓度为___________ 。
(2)在标准状况下,将V L A气体(摩尔质量为M)溶于0.1 L水中,所得溶液的密度为ρ,则此溶液的物质的量浓度为_____________ 。
(3)某硫酸溶液的物质的量浓度为c1,密度为ρ1;另一种硫酸溶液的物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为______________ 。
(1)将117 g NaCl溶于水配制成1 L溶液,该溶液中NaCl的物质的量浓度为
(2)在标准状况下,将V L A气体(摩尔质量为M)溶于0.1 L水中,所得溶液的密度为ρ,则此溶液的物质的量浓度为
(3)某硫酸溶液的物质的量浓度为c1,密度为ρ1;另一种硫酸溶液的物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为
A.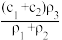 | B.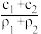 | C.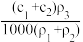 | D. |
您最近一年使用:0次
9 . 将一定质量的镁铝合金投入100 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5 mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示。
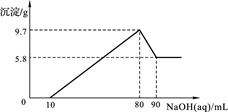
(1)当沉淀达到最大值时,Al(OH)3的质量;
(2)原合金中Mg的质量;
(3)盐酸的物质的量浓度。

(1)当沉淀达到最大值时,Al(OH)3的质量;
(2)原合金中Mg的质量;
(3)盐酸的物质的量浓度。
您最近一年使用:0次
2016-12-09更新
|
1362次组卷
|
5卷引用:2014-2015四川省资阳市高一上学期学期期末化学试卷
9-10高一下·福建宁德·期末
名校
10 . 某有机物A与氢气的相对密度是30,取有机物A 6.0g完全燃烧后,生成0.2mol CO2和0.2mol H2O。此有机物既可与金属钠反应,又可与氢氧化钠和碳酸钠反应。
(1)计算该有机物的分子式为___________ 。
(2)根据该有机物的性质,其结构简式为___________ 。
(1)计算该有机物的分子式为
(2)根据该有机物的性质,其结构简式为
您最近一年使用:0次
2016-12-09更新
|
1178次组卷
|
4卷引用:2012-2013学年四川省资阳市高一下学期期末检测化学试卷
(已下线)2012-2013学年四川省资阳市高一下学期期末检测化学试卷(已下线)2010年福建省宁德市高一下学期期末考试化学试题2016-2017学年河北省定州中学高二下学期第一次月考化学试卷江西省上饶中学2018-2019学年高二(奥赛、实验、重点)上学期开学检测化学试题



