名校
1 . 回答问题:
(1)常温下,浓度为0.005mol/L的 溶液pH值为
溶液pH值为___________ ; 的NaOH溶液中水电离出的心
的NaOH溶液中水电离出的心 为
为___________ mol/L。
(2)常温下, 的盐酸和
的盐酸和 的NaOH等体积混合,溶液的pH值为
的NaOH等体积混合,溶液的pH值为___________ ;求 的
的 溶液与
溶液与 的NaOH溶液的等体积混合,溶液的pH值为
的NaOH溶液的等体积混合,溶液的pH值为___________ 。
(3)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是___________ 。(用a、b、c表示,下同)。
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)由大到小的顺序为___________ 。
(1)常温下,浓度为0.005mol/L的
 溶液pH值为
溶液pH值为 的NaOH溶液中水电离出的心
的NaOH溶液中水电离出的心 为
为(2)常温下,
 的盐酸和
的盐酸和 的NaOH等体积混合,溶液的pH值为
的NaOH等体积混合,溶液的pH值为 的
的 溶液与
溶液与 的NaOH溶液的等体积混合,溶液的pH值为
的NaOH溶液的等体积混合,溶液的pH值为(3)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)由大到小的顺序为
您最近一年使用:0次
2022-03-15更新
|
270次组卷
|
2卷引用:四川省南充市南部县第二中学2021-2022学年高二下学期3月月考化学试题
名校
2 . 物质的量是高中化学中常用的物理量,请完成以下内容。(注意:用NA表示阿伏加德罗常数)
(1)3.01×1023个NH3分子中含有氢原子的个数为_______ 。
(2)常温常压下,92gNO2气体含有的原子数为_______ 。
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(SO )=
)=_______ 。
(4)32gSO2标况下的体积为_______ L
(5)实验室有密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸,其物质的量浓度为_______ 某同学需要0.10mol/L的硫酸500mL,需量取98%浓硫酸的体积为_______ mL
(1)3.01×1023个NH3分子中含有氢原子的个数为
(2)常温常压下,92gNO2气体含有的原子数为
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(SO
 )=
)=(4)32gSO2标况下的体积为
(5)实验室有密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸,其物质的量浓度为
您最近一年使用:0次
名校
解题方法
3 . 计算(要求写出计算过程)
(1)常温下某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,求酸溶液体积V(酸)和碱溶液体积V(碱)的关系。
(2)已知在室温时,Mg(OH)2的溶度积Ksp=4.0×10-12(mol/L)3,求室温下Mg(OH)2饱和溶液中Mg2+和OH-的物质的量浓度。
(1)常温下某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,求酸溶液体积V(酸)和碱溶液体积V(碱)的关系。
(2)已知在室温时,Mg(OH)2的溶度积Ksp=4.0×10-12(mol/L)3,求室温下Mg(OH)2饱和溶液中Mg2+和OH-的物质的量浓度。
您最近一年使用:0次
解题方法
4 . 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求:
(1)此时A的浓度c(A)=_______ mol/L
(2)前5min内用B表示的平均反应速率v(B)=_______ mol/(L·min);
(3)化学反应方程式中x的值为_______ 。
(1)此时A的浓度c(A)=
(2)前5min内用B表示的平均反应速率v(B)=
(3)化学反应方程式中x的值为
您最近一年使用:0次
5 . Ⅰ.25℃时,0.1 mol/L的HA溶液中 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。
(1)BOH是_____ (填“强电解质”或“弱电解质”),HA的电离方程式是____
(2)在加水稀释HA的过程中,随着水量的增加而减小的是_____ (填字母)。
A.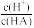 B.
B.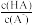 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)
(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体____ (填“多”、“少”或“相等”)。
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要____ mL。 如果加入pH=4的HCl溶液,需加入此HCl溶液____ mL。
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=_____ 。
 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。(1)BOH是
(2)在加水稀释HA的过程中,随着水量的增加而减小的是
A.
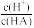 B.
B.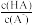 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=
您最近一年使用:0次
2021-05-09更新
|
674次组卷
|
2卷引用:四川省阆中中学2020-2021学年高二下学期期中教学质量检测化学试题
名校
6 . 物质的量是高中化学中常用的物理量,请完成以下内容。(注意:用NA表示阿伏加 德罗常数)
(1)3.01×1023个SO2分子中含有氧原子的个数为_____ 。
(2)常温常压下,92gNO2气体含有的原子数为______ 。
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c( )=
)=_______ 。
(4)将2.86gNa2CO3·10H2O溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为____ g。向上述溶液中加入足量稀盐酸,反应产生的气体在标准状况下体积为___ mL。
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_ 。(用a、b、d表示)
(1)3.01×1023个SO2分子中含有氧原子的个数为
(2)常温常压下,92gNO2气体含有的原子数为
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(
 )=
)=(4)将2.86gNa2CO3·10H2O溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
您最近一年使用:0次
7 . (1)标准状况下,0.2mol NH3与_________________ g H2O的电子数相等。
(2)含有相同氧原子数的CO和CO2,其质量比为_________________________ 。
(3)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量__________ 。
(4)已知V mLAl2(SO4)3溶液中含Al3+ a g,则溶液中SO42-的物质的量浓度是_____________ 。
(5)下列8种化学符号:11H2、12H2、614C、36Li、1123Na、714N、37Li、1224Mg。
①表示核素的符号共________ 种。
②互为同位素的是________ 。
③中子数相等,但质子数不相等的核素是_______________ 。
(2)含有相同氧原子数的CO和CO2,其质量比为
(3)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量
(4)已知V mLAl2(SO4)3溶液中含Al3+ a g,则溶液中SO42-的物质的量浓度是
(5)下列8种化学符号:11H2、12H2、614C、36Li、1123Na、714N、37Li、1224Mg。
①表示核素的符号共
②互为同位素的是
③中子数相等,但质子数不相等的核素是
您最近一年使用:0次
名校
8 . 如图所示是“足球稀”分子中含有12个五边形,20个六边形,30个双键。
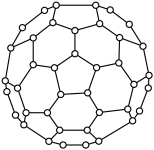
(1)平均每个五边形所含碳原子为______ 个,平均每个六边形所含的碳原子为_________ 个。
(2)“足球烯”分子的分子式为___________ 。
(3)“足球烯”分子含有的化学键单键数为___________ 。
(4)若某“足球烯”分子含12个正五边,25个正六边形,则其分子式为_________ 。

(1)平均每个五边形所含碳原子为
(2)“足球烯”分子的分子式为
(3)“足球烯”分子含有的化学键单键数为
(4)若某“足球烯”分子含12个正五边,25个正六边形,则其分子式为
您最近一年使用:0次
9 . 回答下列问题。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是___ 。属于电解质的是___ 。属于非电解质的是___ 。
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为___ mol/L。
(3)1.204×1024个H2SO4分子的物质的量为___ mol,共含___ 个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___ mol/L。
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是___ 。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为
(3)1.204×1024个H2SO4分子的物质的量为
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是
您最近一年使用:0次
名校
10 . 一定条件下,将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)  mC(g)+2D(g),经过5 min后,反应达到平衡。此时测得,D的浓度为0.5 mol/L,c(A)∶c(B)=1∶3,C的反应速率是0.1 mol·L-1·min-1.求:
mC(g)+2D(g),经过5 min后,反应达到平衡。此时测得,D的浓度为0.5 mol/L,c(A)∶c(B)=1∶3,C的反应速率是0.1 mol·L-1·min-1.求:
①m的值为多少?_____________
②A在5 min末的浓度。__________
③B的平衡转化率。___________
④该反应的平衡常数。___________
 mC(g)+2D(g),经过5 min后,反应达到平衡。此时测得,D的浓度为0.5 mol/L,c(A)∶c(B)=1∶3,C的反应速率是0.1 mol·L-1·min-1.求:
mC(g)+2D(g),经过5 min后,反应达到平衡。此时测得,D的浓度为0.5 mol/L,c(A)∶c(B)=1∶3,C的反应速率是0.1 mol·L-1·min-1.求:①m的值为多少?
②A在5 min末的浓度。
③B的平衡转化率。
④该反应的平衡常数。
您最近一年使用:0次
2019-11-05更新
|
156次组卷
|
2卷引用:四川省阆中东风中学校2020-2021学年高二上学期第三学月调研监测化学试题



