名校
1 . 回答下列问题。
(1)BN晶体有多种结构,其中立方氮化硼具有金刚石型结构(如图)。___________ 个B原子;B原子周围距离最近且相等的N原子数为___________ ,构成的空间结构为___________ 。
②原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0,0,0),则距离该B原子最近的N原子坐标参数为___________ 。若该密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中最近的B原子和N原子之间的距离为
,则晶胞中最近的B原子和N原子之间的距离为___________ cm(用代数式表示即可)。
(2)钇钡铜氧是一种新型节能高温超导体,其晶胞结构如图所示。研究发现,此高温超导体中的Cu元素有两种价态,分别为+2和+3,Y元素的化合价为+3,Ba元素的化合价为+2。___________ 。(按题目中元素顺序书写);
②该物质中 与
与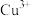 的个数比为
的个数比为___________ 。
(1)BN晶体有多种结构,其中立方氮化硼具有金刚石型结构(如图)。

②原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0,0,0),则距离该B原子最近的N原子坐标参数为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中最近的B原子和N原子之间的距离为
,则晶胞中最近的B原子和N原子之间的距离为(2)钇钡铜氧是一种新型节能高温超导体,其晶胞结构如图所示。研究发现,此高温超导体中的Cu元素有两种价态,分别为+2和+3,Y元素的化合价为+3,Ba元素的化合价为+2。

②该物质中
 与
与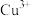 的个数比为
的个数比为
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题。
(1) 、
、 、
、 、
、 对应的简单离子的半径由大到小的顺序是
对应的简单离子的半径由大到小的顺序是___________ (用离子符号表示)。
(2) 、
、 、
、 、KCl的熔点由小到大的顺序为:
、KCl的熔点由小到大的顺序为:___________ 。
(3)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。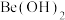 和
和 可用试剂NaOH溶液鉴别。涉及的化学方程式为:
可用试剂NaOH溶液鉴别。涉及的化学方程式为:___________ 。
(4)已知下列化学键的键能:
过氧化氢不稳定,易发生分解反应 ,利用键能数据计算该反应的反应热为
,利用键能数据计算该反应的反应热为
___________ 。
(5)下列关于晶体结构和性质的叙述中都正确的是___________ 。
①金刚石晶体中最小的环为六元环,环上最多有4个碳原子共面
②金属阳离子只能存在于离子晶体中
③熔点1070℃,易溶于水,其水溶液和熔融状态均能导电的晶体为离子晶体
④因金属性 ,所以熔点:
,所以熔点:
⑤干冰晶体中,每个二氧化碳分子周围等距且紧邻的二氧化碳分子有12个
⑥因为1molSi晶体中含有2molSi—Si键,所以1molSiC晶体中也含有2molSi—C键
⑦NaCl晶胞中每个 周围距离最近且相等的
周围距离最近且相等的 数为8
数为8
⑧干冰和冰的晶胞结构相同
(1)
 、
、 、
、 、
、 对应的简单离子的半径由大到小的顺序是
对应的简单离子的半径由大到小的顺序是(2)
 、
、 、
、 、KCl的熔点由小到大的顺序为:
、KCl的熔点由小到大的顺序为:(3)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。
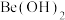 和
和 可用试剂NaOH溶液鉴别。涉及的化学方程式为:
可用试剂NaOH溶液鉴别。涉及的化学方程式为:(4)已知下列化学键的键能:
| 化学键 | C—C | N—N | O—O | O=O | O—H |
 | 347.7 | 193 | 142 | 497.3 | 462.8 |
 ,利用键能数据计算该反应的反应热为
,利用键能数据计算该反应的反应热为
(5)下列关于晶体结构和性质的叙述中都正确的是
①金刚石晶体中最小的环为六元环,环上最多有4个碳原子共面
②金属阳离子只能存在于离子晶体中
③熔点1070℃,易溶于水,其水溶液和熔融状态均能导电的晶体为离子晶体
④因金属性
 ,所以熔点:
,所以熔点:
⑤干冰晶体中,每个二氧化碳分子周围等距且紧邻的二氧化碳分子有12个
⑥因为1molSi晶体中含有2molSi—Si键,所以1molSiC晶体中也含有2molSi—C键
⑦NaCl晶胞中每个
 周围距离最近且相等的
周围距离最近且相等的 数为8
数为8⑧干冰和冰的晶胞结构相同
您最近一年使用:0次
名校
3 . 按题意要求填空:
(1)已知 己烷完全燃烧生成液态水放出
己烷完全燃烧生成液态水放出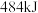 的热量,写出表示己烷燃烧热的热化学方程
的热量,写出表示己烷燃烧热的热化学方程_______ 。
(2)已知在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
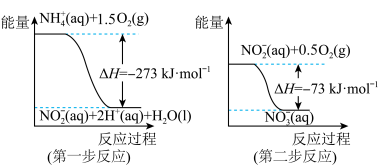
则 全部被氧化成
全部被氧化成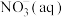 的热化学方程式为:
的热化学方程式为:_______ 。
(3)化学键的键能是原子间形成(或断裂) 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: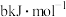 ;S=O:
;S=O: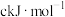 ;H-O:
;H-O: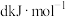 。
。
已知反应:
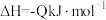 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即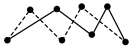 ),试根据这些数据计算已知反应的反应热:则
),试根据这些数据计算已知反应的反应热:则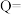
_______ (用a、b、c、d表示)。若已知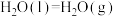
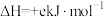 ,试写出
,试写出 和
和 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:_______ 。
(4)已知 (金刚石,s)
(金刚石,s)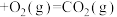
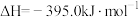
 (石墨,s)
(石墨,s)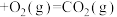
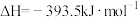
①石墨和金刚石相比,石墨的稳定性_______ 金刚石的稳定性。(填“大于”“小于”或“等于”,下同)
②石墨中 键键能
键键能_______ 金刚石中 键键能。
键键能。
(5)把煤作为燃料有下列两种途径:
途径I:
 ①
①
途径II:先制成水煤气:
 ②
②
再燃烧水煤气:
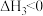 ③
③

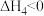 ④
④
则途径I放出的热量_______ (填“大于”“等于”或“小于”)途径II放出的热量; 、
、 、
、 、
、 的数学关系式是
的数学关系式是_______ 。
(6)某学生在测定稀盐酸和氢氧化钠稀溶液发生中和反应的反应热的实验前,先配制 的
的 溶液:若实验中大约要使用
溶液:若实验中大约要使用 溶液需要用托盘天平称量
溶液需要用托盘天平称量 固体
固体_______  ,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和_______ 。
(1)已知
 己烷完全燃烧生成液态水放出
己烷完全燃烧生成液态水放出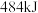 的热量,写出表示己烷燃烧热的热化学方程
的热量,写出表示己烷燃烧热的热化学方程(2)已知在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
则
 全部被氧化成
全部被氧化成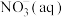 的热化学方程式为:
的热化学方程式为:(3)化学键的键能是原子间形成(或断裂)
 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: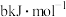 ;S=O:
;S=O: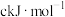 ;H-O:
;H-O: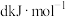 。
。已知反应:

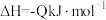 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即 ),试根据这些数据计算已知反应的反应热:则
),试根据这些数据计算已知反应的反应热:则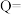
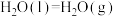
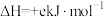 ,试写出
,试写出 和
和 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:(4)已知
 (金刚石,s)
(金刚石,s)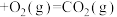
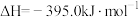
 (石墨,s)
(石墨,s)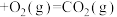
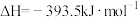
①石墨和金刚石相比,石墨的稳定性
②石墨中
 键键能
键键能 键键能。
键键能。(5)把煤作为燃料有下列两种途径:
途径I:

 ①
①途径II:先制成水煤气:

 ②
②再燃烧水煤气:

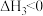 ③
③
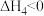 ④
④则途径I放出的热量
 、
、 、
、 、
、 的数学关系式是
的数学关系式是(6)某学生在测定稀盐酸和氢氧化钠稀溶液发生中和反应的反应热的实验前,先配制
 的
的 溶液:若实验中大约要使用
溶液:若实验中大约要使用 溶液需要用托盘天平称量
溶液需要用托盘天平称量 固体
固体 ,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
您最近一年使用:0次
2023-08-17更新
|
206次组卷
|
2卷引用:河北省新乐市第一中学2022-2023学年高二上学期11月期中考试化学试题
解题方法
4 . 4-溴环己烯(W)在不同条件所发生的相关反应如图:
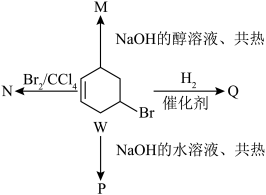
已知:①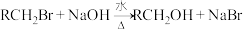 ;
;
②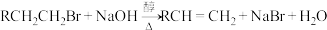 。
。
回答下列问题:
(1)W中所含官能团的名称为___________ 。
(2)M的结构简式可能为___________ 。
(3)Q的核磁共振氢谱中,有___________ 组峰,且峰面积之比为___________ 。
(4)N与NaOH的水溶液在共热条件下发生反应的化学方程式为___________ ,该反应的反应类型为___________ 。
(5)化合物L与P互为同分异构体,同时满足下列条件的L的结构有___________ 种(不包含P和不考虑立体异构)。
①除含一个六元环外不含其他环;
②能使酸性高锰酸钾溶液褪色;
③无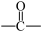 和
和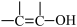 结构。
结构。

已知:①
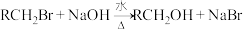 ;
;②
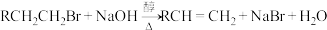 。
。回答下列问题:
(1)W中所含官能团的名称为
(2)M的结构简式可能为
(3)Q的核磁共振氢谱中,有
(4)N与NaOH的水溶液在共热条件下发生反应的化学方程式为
(5)化合物L与P互为同分异构体,同时满足下列条件的L的结构有
①除含一个六元环外不含其他环;
②能使酸性高锰酸钾溶液褪色;
③无
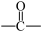 和
和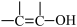 结构。
结构。
您最近一年使用:0次
5 . 有机化合物(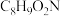 )分子的苯环上同时含有
)分子的苯环上同时含有 、
、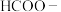 和
和 3个取代基,符合上述条件且属于芳香族的结构有
3个取代基,符合上述条件且属于芳香族的结构有
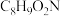 )分子的苯环上同时含有
)分子的苯环上同时含有 、
、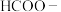 和
和 3个取代基,符合上述条件且属于芳香族的结构有
3个取代基,符合上述条件且属于芳香族的结构有| A.6种 | B.8种 | C.10种 | D.12种 |
您最近一年使用:0次
2023-08-08更新
|
141次组卷
|
2卷引用:河北省承德市部分学校2022-2023学年高二上学期11月期中考试化学试题
6 . 重水是含有较多 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:
(1)画出Ca原子的原子结构示意图___________ ,硫元素在元素周期表的位置___________ ,属于___________ 区。
(2)写出基态N原子的电子排布式___________ ,画出基态O原子的价电子排布图___________ 。基态N原子的第一电离能比O原子的要大的原因是___________ 。
(3)若将基态镁原子最高能级的电子排布图表示为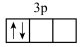 ,则它违背的电子排布规律是
,则它违背的电子排布规律是___________ 、___________ ,基态硫原子核外电子所处最高能级轨道的形状为___________ 。
(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
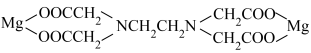
其中C、N、O、Mg四种元素的电负性由大到小的顺序是___________ ,原子半径最大的是___________ (填元素符号,下同),四种元素中基态原子核外单电子数最多的是___________ 。
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式___________ 、___________ 。
 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:(1)画出Ca原子的原子结构示意图
(2)写出基态N原子的电子排布式
(3)若将基态镁原子最高能级的电子排布图表示为
 ,则它违背的电子排布规律是
,则它违背的电子排布规律是(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
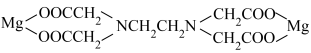
其中C、N、O、Mg四种元素的电负性由大到小的顺序是
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式
您最近一年使用:0次
解题方法
7 . 某兴趣小组用如图所示装置研究电化学相关问题。电解质溶液都是足量的,当闭合该装置的电键时,观察到电流表的指针发生了偏转。

回答下面问题:
(1)甲池是___________ (填“原电池”或“电解池”),其中通入甲烷( )的Pt电极是
)的Pt电极是___________ (填“正极”“负极”“阳极”或“阴极”),通入氧气的Pt电极上发生的电极反应___________ 。
(2)乙池电极A石墨碳棒上发生的电极反应___________ ,电极B银棒上发生___________ (填“氧化”或“还原”)反应,开始时 溶液呈酸性,用离子方程式表示呈酸性的原因
溶液呈酸性,用离子方程式表示呈酸性的原因___________ 。电解一段时间后溶液的pH将___________ (填“增大”“减小”或“不变”)。
(3)丙池中C和D电极均为石墨电极,U形管中的现象是___________ 。丙池两个烧杯中溶液变为蓝色的是___________ (填“a”或“b”),若U形管中盛有100mL溶液,电解一段时间断开电键K,两个电极上一共收集到224mL气体(标准状况下,忽略溶液体积的变化),此时U形管中溶液的
___________ 。
(4)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

写出活性吸附电极N上的电极反应___________ , 在溶液中移动方向
在溶液中移动方向___________ (填序号)。
A.从左室穿过交换膜进入右室 B.从右室穿过交换膜进入左室

回答下面问题:
(1)甲池是
 )的Pt电极是
)的Pt电极是(2)乙池电极A石墨碳棒上发生的电极反应
 溶液呈酸性,用离子方程式表示呈酸性的原因
溶液呈酸性,用离子方程式表示呈酸性的原因(3)丙池中C和D电极均为石墨电极,U形管中的现象是

(4)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

写出活性吸附电极N上的电极反应
 在溶液中移动方向
在溶液中移动方向A.从左室穿过交换膜进入右室 B.从右室穿过交换膜进入左室
您最近一年使用:0次
名校
解题方法
8 . 合成氨是人类科学技术上的一项重大突破,是化学与技术对社会发展与进步的巨大贡献之一,氨在生产生活中起到了非常重要的作用。回答下列问题:
(1)已知相关化学键的键能数据
反应

___________  。已知该反应的
。已知该反应的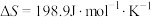 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?___________ (填标号)
A.25℃ B.125℃ C.225℃ D.325℃
(2)工业生成氨气的热化学方程式:
 ,
,
①下列说法正确的是___________ 。
A.升高温度既能加快化学反应速率又一定能提高催化剂的活性
B.工业生成的条件是500℃和200个大气压,此时催化剂活性最强,反应速率较快
C.实际工业生产中要及时抽出 这样既能提高平衡转化率又能加快化学反应速率
这样既能提高平衡转化率又能加快化学反应速率
D.实际生产中开始通入气体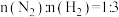 ,达到平衡时三种混合气体中
,达到平衡时三种混合气体中 的百分含量最多。
的百分含量最多。
②已知绝热体积不变的刚性容器中发生上述反应,下列说法不能够判断反应达到化学平衡状态的是___________ (填字母)。
A.容器内气体的密度保持不变 B.容器中气体的平均相对分子质量保持不变
C.容器内三种气体的分压保持不变 D.容器内气体的温度保持不变
(3)在容积相同的三个密闭刚性容器中,分别投入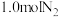 和
和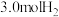 ,在不同温度(500K和600K)、不同催化剂表面积(
,在不同温度(500K和600K)、不同催化剂表面积(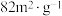 和
和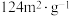 )条件下,反应体系总压强(P)随时间变化关系如图所示。
)条件下,反应体系总压强(P)随时间变化关系如图所示。
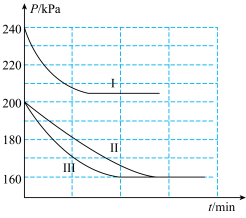
①曲线Ⅲ对应的反应条件可能为___________ 。
②在500K时该反应的压强平衡常数
___________ (保留二位有效数字)。
③在曲线Ⅲ对应条件下,某反应容器中 、
、 和
和 的分压依次是20kPa,10kPa、10kPa,此时反应速率
的分压依次是20kPa,10kPa、10kPa,此时反应速率
___________  (填“<”“=”或“>”)。
(填“<”“=”或“>”)。
(4)工业上利用CO和 制备
制备 ,利用计算机模拟
,利用计算机模拟 的反应历程如下,其中吸附在
的反应历程如下,其中吸附在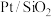 催化剂表面用“·”标注,Ts表示过渡态。
催化剂表面用“·”标注,Ts表示过渡态。
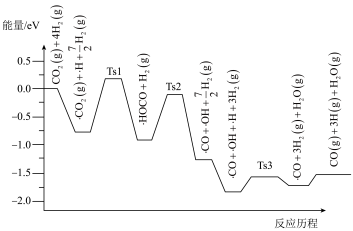
反应历程中最小能垒(活化能)步骤的化学方程式为___________ 。反应

___________ 0(填“>”或“<”)。
(1)已知相关化学键的键能数据
| 化学键 |  | H-H | N-H |
键能( ) ) | 946 | 436.0 | 390.8 |


 。已知该反应的
。已知该反应的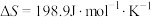 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?A.25℃ B.125℃ C.225℃ D.325℃
(2)工业生成氨气的热化学方程式:

 ,
,①下列说法正确的是
A.升高温度既能加快化学反应速率又一定能提高催化剂的活性
B.工业生成的条件是500℃和200个大气压,此时催化剂活性最强,反应速率较快
C.实际工业生产中要及时抽出
 这样既能提高平衡转化率又能加快化学反应速率
这样既能提高平衡转化率又能加快化学反应速率D.实际生产中开始通入气体
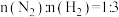 ,达到平衡时三种混合气体中
,达到平衡时三种混合气体中 的百分含量最多。
的百分含量最多。②已知绝热体积不变的刚性容器中发生上述反应,下列说法不能够判断反应达到化学平衡状态的是
A.容器内气体的密度保持不变 B.容器中气体的平均相对分子质量保持不变
C.容器内三种气体的分压保持不变 D.容器内气体的温度保持不变
(3)在容积相同的三个密闭刚性容器中,分别投入
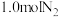 和
和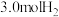 ,在不同温度(500K和600K)、不同催化剂表面积(
,在不同温度(500K和600K)、不同催化剂表面积(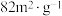 和
和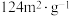 )条件下,反应体系总压强(P)随时间变化关系如图所示。
)条件下,反应体系总压强(P)随时间变化关系如图所示。
①曲线Ⅲ对应的反应条件可能为
②在500K时该反应的压强平衡常数

③在曲线Ⅲ对应条件下,某反应容器中
 、
、 和
和 的分压依次是20kPa,10kPa、10kPa,此时反应速率
的分压依次是20kPa,10kPa、10kPa,此时反应速率
 (填“<”“=”或“>”)。
(填“<”“=”或“>”)。(4)工业上利用CO和
 制备
制备 ,利用计算机模拟
,利用计算机模拟 的反应历程如下,其中吸附在
的反应历程如下,其中吸附在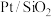 催化剂表面用“·”标注,Ts表示过渡态。
催化剂表面用“·”标注,Ts表示过渡态。
反应历程中最小能垒(活化能)步骤的化学方程式为


您最近一年使用:0次
2023-08-02更新
|
244次组卷
|
2卷引用:河北省邢台市襄都区等5地2022-2023学年高二上学期12月月考化学试题
解题方法
9 . 中和滴定是工业生产和研究中最常见的一种测量方法,回答下面问题:
(1)①中和滴定常用玻璃仪器有:酸式滴定管、碱式滴定管、锥形瓶、___________ 等。
②量取20.00mL1.00mol/LNaOH溶液时,下列滴定管排气泡的方法正确的是___________ 。

(2)①用1.00mol/LNaOH标准溶液测定市售白醋(主要成分是 )的总酸量(
)的总酸量( ),用酸式滴定管取20.00mL待测白醋溶液于锥形瓶中,滴加2滴酚酞作指示剂,用离子方程式表示采用酚酞指示剂的原因
),用酸式滴定管取20.00mL待测白醋溶液于锥形瓶中,滴加2滴酚酞作指示剂,用离子方程式表示采用酚酞指示剂的原因___________ 。
②用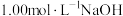 标准溶液滴定,当
标准溶液滴定,当___________ 时,停止滴定,并记录NaOH溶液的终读数。重复滴定4次。
③实验记录
市售白醋总酸度___________  。
。
(3)①某实验小组为了分析补血剂 中铁元素的质量分数,用
中铁元素的质量分数,用 标准溶液在酸性条件下进行氧化还原滴定,写出该反应的离子方程式
标准溶液在酸性条件下进行氧化还原滴定,写出该反应的离子方程式___________ 。
②某同学设计的下列滴定方式中,最合理的是___________ (填字母)。

③滴定前不需要滴加指示剂,理由是___________ 。
(4)莫尔法是一种沉淀滴定法,用标准 溶液滴定待测液可以测定溶液中
溶液滴定待测液可以测定溶液中 的浓度。已知:
的浓度。已知: 、
、 、
、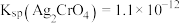 ,AgCl(白色)、AgI(黄色)、
,AgCl(白色)、AgI(黄色)、 (红色)。莫尔法测定
(红色)。莫尔法测定 浓度时所用指示剂是
浓度时所用指示剂是___________ (填“KI”或“ ”)。
”)。
(1)①中和滴定常用玻璃仪器有:酸式滴定管、碱式滴定管、锥形瓶、
②量取20.00mL1.00mol/LNaOH溶液时,下列滴定管排气泡的方法正确的是

(2)①用1.00mol/LNaOH标准溶液测定市售白醋(主要成分是
 )的总酸量(
)的总酸量( ),用酸式滴定管取20.00mL待测白醋溶液于锥形瓶中,滴加2滴酚酞作指示剂,用离子方程式表示采用酚酞指示剂的原因
),用酸式滴定管取20.00mL待测白醋溶液于锥形瓶中,滴加2滴酚酞作指示剂,用离子方程式表示采用酚酞指示剂的原因②用
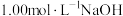 标准溶液滴定,当
标准溶液滴定,当③实验记录
次数 体积(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
 。
。(3)①某实验小组为了分析补血剂
 中铁元素的质量分数,用
中铁元素的质量分数,用 标准溶液在酸性条件下进行氧化还原滴定,写出该反应的离子方程式
标准溶液在酸性条件下进行氧化还原滴定,写出该反应的离子方程式②某同学设计的下列滴定方式中,最合理的是

③滴定前不需要滴加指示剂,理由是
(4)莫尔法是一种沉淀滴定法,用标准
 溶液滴定待测液可以测定溶液中
溶液滴定待测液可以测定溶液中 的浓度。已知:
的浓度。已知: 、
、 、
、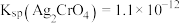 ,AgCl(白色)、AgI(黄色)、
,AgCl(白色)、AgI(黄色)、 (红色)。莫尔法测定
(红色)。莫尔法测定 浓度时所用指示剂是
浓度时所用指示剂是 ”)。
”)。
您最近一年使用:0次
解题方法
10 . 碳酸锰( )可用作瓷釉、肥料和饲料添加剂,还应用于医药,电焊条辅料等。某含锰废水中主要含有
)可用作瓷釉、肥料和饲料添加剂,还应用于医药,电焊条辅料等。某含锰废水中主要含有 、
、 、
、 、
、 、
、 、
、 ,以该废液为原料制备碳酸锰、回收硫酸铵的工艺流程如图所示(部分操作和条件已略,
,以该废液为原料制备碳酸锰、回收硫酸铵的工艺流程如图所示(部分操作和条件已略, 沉淀完全的pH为3.7、
沉淀完全的pH为3.7、 沉淀完全的pH为5.2)。下列说法不正确的是
沉淀完全的pH为5.2)。下列说法不正确的是

 )可用作瓷釉、肥料和饲料添加剂,还应用于医药,电焊条辅料等。某含锰废水中主要含有
)可用作瓷釉、肥料和饲料添加剂,还应用于医药,电焊条辅料等。某含锰废水中主要含有 、
、 、
、 、
、 、
、 、
、 ,以该废液为原料制备碳酸锰、回收硫酸铵的工艺流程如图所示(部分操作和条件已略,
,以该废液为原料制备碳酸锰、回收硫酸铵的工艺流程如图所示(部分操作和条件已略, 沉淀完全的pH为3.7、
沉淀完全的pH为3.7、 沉淀完全的pH为5.2)。下列说法不正确的是
沉淀完全的pH为5.2)。下列说法不正确的是
A.试剂X可能是 |
B.滤渣1主要成分为 、 、 |
C.除重金属时发生的离子方程式为: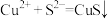 |
D.反应中加入稍过量的 ,碳化过程中发生的离子方程式为 ,碳化过程中发生的离子方程式为 |
您最近一年使用:0次



