1 . 二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:
已知:
(1)为研究该反应,某同学设计了如图所示的三种密闭容器装置(已装入固体V2O3催化剂)。

在初始体积与温度相同的条件下,甲、乙、丙三个容器中均按2molSO2、1molO2进行投料,达到平衡时,三个容器中SO2的转化率由大到小的顺序为___________ (用“甲”“乙”“丙”表示)。
(2)在恒温恒压下不能说明该反应已达平衡的是___________ (填序号)。
①
②n(SO3):n(O2):n(SO2)=2:1:2
③混合气体的平均相对分子质量不再改变
④氧气的平衡分压不再改变
(3)某温度,在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,t1时刻达到平衡,测得容器中含SO3(g)0.18mol。

①计算该温度下,平衡常数K=___________ 。
②t1时刻达到平衡后,改变一个条件使化学反应速率发生如图所示的变化,则改变的条件是___________ 。
A.体积不变,向容器中通入少量氮气
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
③若继续通入0.02molSO3和0.010molO2,则平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(4)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如图所示。

反应在5.0MPa、550℃时的α=___________ 。判断的依据是___________ 。
已知:

(1)为研究该反应,某同学设计了如图所示的三种密闭容器装置(已装入固体V2O3催化剂)。

在初始体积与温度相同的条件下,甲、乙、丙三个容器中均按2molSO2、1molO2进行投料,达到平衡时,三个容器中SO2的转化率由大到小的顺序为
(2)在恒温恒压下不能说明该反应已达平衡的是
①

②n(SO3):n(O2):n(SO2)=2:1:2
③混合气体的平均相对分子质量不再改变
④氧气的平衡分压不再改变
(3)某温度,在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,t1时刻达到平衡,测得容器中含SO3(g)0.18mol。

①计算该温度下,平衡常数K=
②t1时刻达到平衡后,改变一个条件使化学反应速率发生如图所示的变化,则改变的条件是
A.体积不变,向容器中通入少量氮气
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
③若继续通入0.02molSO3和0.010molO2,则平衡
(4)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如图所示。

反应在5.0MPa、550℃时的α=
您最近一年使用:0次
2 . 锂系电池包括锂电池和锂离子电池,锂电池是一类由锂金属或锂合金为正/负极材料、使用非水电解质溶液的电池。1912年锂金属电池最早由GilbertN。Lewis提出并研究。20世纪70年代时,M。S。Whittingham提出并开始研究锂离子电池。
(1)全固态锂离子电池放电时电池发生反应: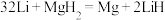 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为___________ 。
(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。
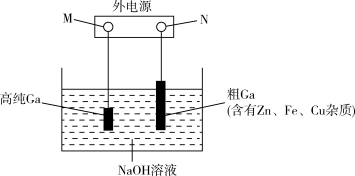
已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的___________ 极,电解精炼镓时产生的,阳极泥的主要成分是___________ 。
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式___________ 。
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=___________ (η=生成目标产物消耗的电子数÷转移的电子总数)。
(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择___________ 。少量的 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是___________ 。

(1)全固态锂离子电池放电时电池发生反应:
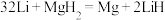 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。

已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过
 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成
 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是
您最近一年使用:0次
3 . 某兴趣小组探究金属腐蚀条件,设计了以下实验装置。下列说法不正确的是
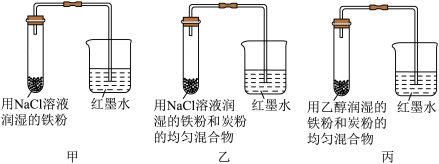

| A.铁粉腐蚀速率:乙>甲>丙 |
| B.甲、乙、丙三个装置均构成原电池,发生吸氧腐蚀 |
C.乙装置发生电化学腐蚀时正极反应式: |
| D.对比甲、乙、丙三个实验,金属放在有些有机溶剂中可防腐蚀 |
您最近一年使用:0次
名校
4 . 弱电解质的研究是重要课题。室温下,H2SeO3电离平衡体系中含Se微粒的物质的量分数与溶液PH的关系如图所示,回答下列问题:
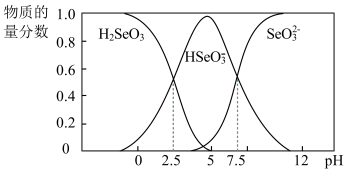
(1)写出NaHSeO3水解常数的表达式___________
(2)写出将将少量氢氧化钠溶液滴入H2SeO3溶液中的离子方程式:___________
(3)NaHSeO3溶液显___________ 性,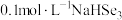 溶液中,离子浓度由大到小的顺序为
溶液中,离子浓度由大到小的顺序为___________ 。
(4)计算,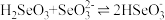 的平衡常数K=
的平衡常数K=___________

(1)写出NaHSeO3水解常数的表达式
(2)写出将将少量氢氧化钠溶液滴入H2SeO3溶液中的离子方程式:
(3)NaHSeO3溶液显
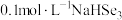 溶液中,离子浓度由大到小的顺序为
溶液中,离子浓度由大到小的顺序为(4)计算,
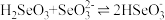 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
2023-09-02更新
|
321次组卷
|
2卷引用:山东省聊城第一中学2022-2023学年高二上学期11月期中考试化学试题
名校
5 . 根据要求,回答下列问题:
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:___________ (M或N)。
Ⅱ.已知: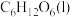 的燃烧热
的燃烧热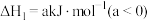 ;
; ,
,
(2)则
___________ a(填“>”“<”或“=”)。
Ⅲ.用如图所示的装置测定中和反应反应热。
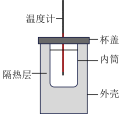
(3)从实验装置上看,还缺少___________ ,其能否用铁质材料替代?___________ (填“能”或“不能”)
(4)装置中隔热层的作用是___________
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将___________ (填偏大、偏小或无影响)
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:
Ⅱ.已知:
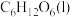 的燃烧热
的燃烧热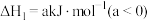 ;
; ,
,(2)则

Ⅲ.用如图所示的装置测定中和反应反应热。

(3)从实验装置上看,还缺少
(4)装置中隔热层的作用是
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将
您最近一年使用:0次
名校
解题方法
6 . 下列实验操作会使结果偏大的是
| A.用玻璃棒蘸取少量氯化钠溶液滴在湿润的pH试纸上 |
| B.中和滴定时,溶液颜色刚刚变色便立即读数 |
| C.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,碱式滴定管未润洗 |
| D.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,酸式滴定管刚开始有气泡,读数时,气泡消失 |
您最近一年使用:0次
名校
7 . 下列说法正确的是
A.向 溶液加水稀释时会引起溶液中 溶液加水稀释时会引起溶液中 减小 减小 |
| B.用pH值相等的盐酸和醋酸去中和等体积等浓度的氢氧化钠溶液,消耗酸的体积为:V(盐酸)<V(醋酸) |
| C.加入电解质,一定会破坏水的电离平衡 |
| D.25℃时,NH4Cl溶液的Kw等于盐酸溶液的Kw |
您最近一年使用:0次
2023-09-02更新
|
309次组卷
|
2卷引用:山东省聊城第一中学2022-2023学年高二上学期11月期中考试化学试题
8 . 利用图示可以从不同角度研究含氮物质的性质及其转化关系。

回答下列问题:
(1)a溶于水所得溶液呈_______ (填“酸性”或“碱性”)。
(2)a与e反应生成的化合物为_______ (填化学式),该化合物属于_______ (填“共价化合物”或“离子化合物”)。
(3)b→c的化学方程式为_______ 。
(4)d的化学式为_______ 。

回答下列问题:
(1)a溶于水所得溶液呈
(2)a与e反应生成的化合物为
(3)b→c的化学方程式为
(4)d的化学式为
您最近一年使用:0次
2023-06-05更新
|
293次组卷
|
4卷引用:山东省普通高中2021-2022学年高二下学期学业水平合格性考试化学试题
9 . 下列有关常见气体成分检验的结论正确的是
| 选项 | 仪器或试剂 | 实验现象 | 结论 |
| A | 湿润的红色石蕊试纸 | 试纸变蓝 | 一定含 |
| B | 灼热CuO | 黑色固体变为红色 | 一定含 |
| C | 澄清石灰水 | 溶液中出现浑浊 | 一定含 |
| D | 湿润的淀粉-KI试纸 | 试纸变蓝 | 一定含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-05更新
|
162次组卷
|
2卷引用:山东省普通高中2021-2022学年高二下学期学业水平合格性考试化学试题
10 . 根据所学知识,回答下列问题
(1)在25℃、101kPa下,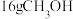 完全燃烧生成
完全燃烧生成 气体和液态水时放出363.25kJ的热量,则表示甲醇燃烧热的热化学方程式为
气体和液态水时放出363.25kJ的热量,则表示甲醇燃烧热的热化学方程式为_______ 。
(2)将二氧化碳转化为高附加值碳基燃料有利于实现人类活动的“碳中和”。
已知:①
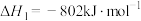 ;
;
②
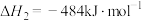 ;
;
③

又知相关化学键的键能数据如下表所示。
则a=_______ ,x=_______ 。
(3)用如图所示的装置测定中和反应反应热。
实验药品: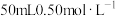 盐酸、
盐酸、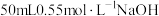 溶液。
溶液。

实验步骤:略。回答下列问题。
①从实验装置上看,还缺少_______ 。
②加入NaOH溶液的正确操作是_______ (填字母)。
A.沿玻璃棒缓慢加入 B.分三次均匀加入
C.一次迅速加入 D.用滴定管小心滴加
③若实验中改用60mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),若实验操作均正确,则生成1mol水时的反应热_______ (填“相等”或“不相等”)。
④强酸与强碱的稀溶液发生中和反应的热化学方程式:
 。
。
a.向NaOH溶液中加入稀醋酸;
b.向 溶液中加入稀硫酸;
溶液中加入稀硫酸;
c.向NaOH溶液中加入稀硝酸;
当反应均生成1mol水时的热效应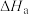 、
、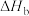 、
、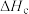 由大到小的关系
由大到小的关系_______ 。
(1)在25℃、101kPa下,
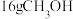 完全燃烧生成
完全燃烧生成 气体和液态水时放出363.25kJ的热量,则表示甲醇燃烧热的热化学方程式为
气体和液态水时放出363.25kJ的热量,则表示甲醇燃烧热的热化学方程式为(2)将二氧化碳转化为高附加值碳基燃料有利于实现人类活动的“碳中和”。
已知:①

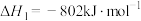 ;
;②

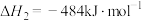 ;
;③


又知相关化学键的键能数据如下表所示。
| 化学键 | H-H | C=O | H-O | C-H |
 | 436 | 745 | 463 | x |
(3)用如图所示的装置测定中和反应反应热。
实验药品:
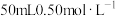 盐酸、
盐酸、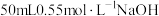 溶液。
溶液。
实验步骤:略。回答下列问题。
①从实验装置上看,还缺少
②加入NaOH溶液的正确操作是
A.沿玻璃棒缓慢加入 B.分三次均匀加入
C.一次迅速加入 D.用滴定管小心滴加
③若实验中改用60mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量
④强酸与强碱的稀溶液发生中和反应的热化学方程式:

 。
。a.向NaOH溶液中加入稀醋酸;
b.向
 溶液中加入稀硫酸;
溶液中加入稀硫酸;c.向NaOH溶液中加入稀硝酸;
当反应均生成1mol水时的热效应
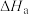 、
、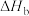 、
、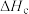 由大到小的关系
由大到小的关系
您最近一年使用:0次
2023-03-06更新
|
320次组卷
|
2卷引用:山东省聊城市2022-2023学年高二上学期期末考试化学试题



