解题方法
1 . 硒是人体必需微量元素之一,可用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。粗硒经过下列流程可获得亚硒酸钠( )。
)。
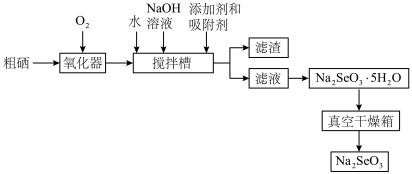
(1)298K、 ,
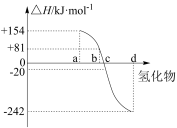
, 、S、Se、Te分别与
、S、Se、Te分别与 化合的反应热数据如下图所示。写出Se与
化合的反应热数据如下图所示。写出Se与 化合的热化学反应方程式:
化合的热化学反应方程式:___________ 。
(2)硒与硫是同主族的相邻元素,硒的原子序数为___________ 。
(3)已知在氧化器中粗硒转化为 ,在搅拌槽中与NaOH发生反应的离子方程式为
,在搅拌槽中与NaOH发生反应的离子方程式为______ 。
(4)由滤液获取 晶体的操作为
晶体的操作为___________ 、过滤、洗涤。
(5) 转化为
转化为 的过程中存在平衡
的过程中存在平衡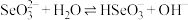 ,下列粒子中不会影响该平衡的是___________(填字母)。
,下列粒子中不会影响该平衡的是___________(填字母)。
(6)常温下,向 溶液中逐滴加入NaOH溶液,混合溶液中
溶液中逐滴加入NaOH溶液,混合溶液中 [X为
[X为 或
或 ]与pH的变化关系如图所示。
]与pH的变化关系如图所示。
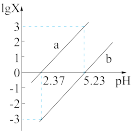
①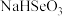 溶液呈
溶液呈___________ 性(填“酸”“碱”或“中”)。
② 时,溶液中
时,溶液中
___________ 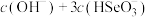 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 )。
)。
(1)298K、
 ,
, 、S、Se、Te分别与
、S、Se、Te分别与 化合的反应热数据如下图所示。写出Se与
化合的反应热数据如下图所示。写出Se与 化合的热化学反应方程式:
化合的热化学反应方程式:
(2)硒与硫是同主族的相邻元素,硒的原子序数为
(3)已知在氧化器中粗硒转化为
 ,在搅拌槽中与NaOH发生反应的离子方程式为
,在搅拌槽中与NaOH发生反应的离子方程式为(4)由滤液获取
 晶体的操作为
晶体的操作为(5)
 转化为
转化为 的过程中存在平衡
的过程中存在平衡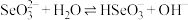 ,下列粒子中不会影响该平衡的是___________(填字母)。
,下列粒子中不会影响该平衡的是___________(填字母)。A. | B. | C. | D.O=C=O |
 溶液中逐滴加入NaOH溶液,混合溶液中
溶液中逐滴加入NaOH溶液,混合溶液中 [X为
[X为 或
或 ]与pH的变化关系如图所示。
]与pH的变化关系如图所示。
①
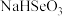 溶液呈
溶液呈②
 时,溶液中
时,溶液中
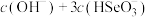 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
2 . 研究发现百多种植物富含草酸,尤以菠菜、苋菜、甜菜、马齿苋、芋头、甘薯和大黄等植物中含量最高,由于草酸可降低矿质元素的生物利用率,在人体中容易与钙离子形成草酸钙导致肾结石,草酸往往被认为是一种矿质元素吸收利用的拮抗物。
已知:草酸( )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。
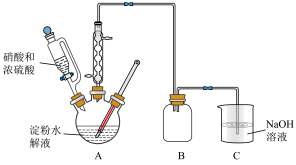
①55~60℃时,装置A中生成 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:___________ 。
②该实验中催化剂浓硫酸用量不宜过量的原因是___________ 。(答出一点即可)
③装置C的作用是___________ 。
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
(3)向10mL
 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
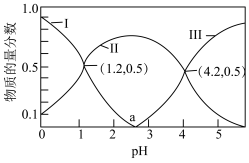
①写出草酸的一级电离方程式:___________ 。
②25℃时,碳酸电离平衡常数分别是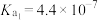 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:___________ 。
已知:草酸(
 )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。

①55~60℃时,装置A中生成
 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:②该实验中催化剂浓硫酸用量不宜过量的原因是
③装置C的作用是
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
A.草酸能使酸性 溶液褪色 溶液褪色 |
B.常温下,0.1mol/L的 溶液的pH=2 溶液的pH=2 |
C.相同条件下,浓度均为0.1mol/L的 溶液的导电能力比硫酸的导电能力弱 溶液的导电能力比硫酸的导电能力弱 |
D. 溶液中存在 溶液中存在 分子,呈酸性 分子,呈酸性 |

 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
①写出草酸的一级电离方程式:
②25℃时,碳酸电离平衡常数分别是
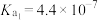 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:
您最近一年使用:0次
3 . 开发利用二氧化碳和甲烷资源,生产用途广泛、附加值高的烃类氧化物,对于环境保护,合成化学和资源利用均有重要意义。甲烷和二氧化碳可催化合成乙酸,其中一步为甲烷在催化剂表面脱氢,其方式有两种:甲烷分子单独脱氢,甲烷分子与二氧化碳共吸附脱氢,反应历程如下。下列说法正确的是
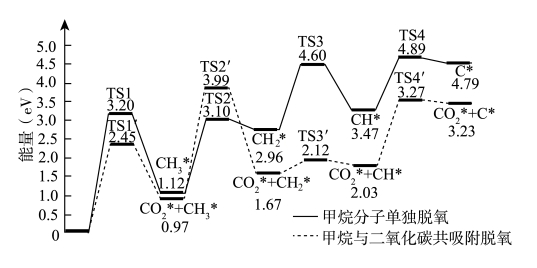

| A.电负性由大到小的顺序是O>C>H |
| B.单独脱氢的过程吸收能量,共吸附脱氢的过程释放能量 |
C.共吸附脱氢的决速步为由 转化为 转化为 的过程 的过程 |
| D.共吸附脱氢过程中,有极性键和非极性键的断裂 |
您最近一年使用:0次
名校
4 . 一定条件下,0.3mol 和0.9mol
和0.9mol 在体积为1L的密闭容器中发生反应:
在体积为1L的密闭容器中发生反应:
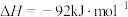 ,反应进行2min,
,反应进行2min, 的物质的量增加了0.4mol。
的物质的量增加了0.4mol。
下列说法正确的是
 和0.9mol
和0.9mol 在体积为1L的密闭容器中发生反应:
在体积为1L的密闭容器中发生反应:
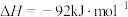 ,反应进行2min,
,反应进行2min, 的物质的量增加了0.4mol。
的物质的量增加了0.4mol。下列说法正确的是
A.平衡后再充入 ,既能加快反应速率又能提高 ,既能加快反应速率又能提高 的平衡转化率 的平衡转化率 |
| B.将容器的体积压缩,可增大单位体积活化分子数,增大活化分子的百分数,加快反应速率 |
| C.反应进行2min,放出的热量值小于18.4kJ |
D. 的体积分数保持不变,能说明反应达到平衡 的体积分数保持不变,能说明反应达到平衡 |
您最近一年使用:0次
2023-08-05更新
|
376次组卷
|
3卷引用:湖南省邵阳市2022-2023学年高二上学期12月月考化学试题
5 . 自然界中,各种原生铜的硫化物经氧化,淋滤作用后可变成 溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
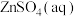 。下列说法不正确的是
。下列说法不正确的是
已知:常温下, ,
, ,
,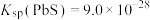
 溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
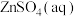 。下列说法不正确的是
。下列说法不正确的是已知:常温下,
 ,
, ,
,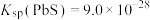
A.该反应达到平衡时, |
B.向含 、 、 、 、 均为 均为 的溶液中通入 的溶液中通入 气体,产生沉淀的顺序依次为CuS、PbS、ZnS 气体,产生沉淀的顺序依次为CuS、PbS、ZnS |
C.饱和PbS溶液中,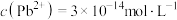 |
D.CuS溶解的条件是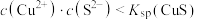 |
您最近一年使用:0次
解题方法
6 . 化学与生活、生产及科技密切相关,下列有关说法正确的是
| A.明矾溶液不仅可以清除铜锈,又可以吸附杂质,杀菌消毒 |
| B.“嫦娥五号”使用的太阳能电池和锂离子电池组,均可将化学能转变成电能 |
C. 和 和 溶液均显碱性,均可用作食用碱和抗酸胃药 溶液均显碱性,均可用作食用碱和抗酸胃药 |
| D.水库的钢闸门与电源负极相连可防止其生锈,该法叫外加电流法 |
您最近一年使用:0次
7 . 综合利用CO2是实现“碳中和”的重要途径。
(1)由合成气(组成为H2、CO和少量的CO2)直接制备甲醇,其中的主要过程包括以下两个反应:
i.
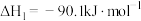
ii.
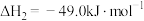
则反应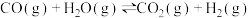

_______ 
(2)某温度下, 和
和 投入2L恒容容器中发生反应ii,该反应的速率方程为
投入2L恒容容器中发生反应ii,该反应的速率方程为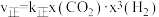 ,
,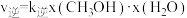 ,
, 、
、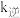 为速率常数且只与温度有关,x为物质的量分数。
为速率常数且只与温度有关,x为物质的量分数。
①反应1min时,测得容器中CH3OH(g)为0.32g,则0~1min内
_______  。
。
②达到平衡时,升高温度, 、
、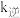 均增大,增大倍数较大的是
均增大,增大倍数较大的是_______ ,由此请总结当温度改变时,正、逆反应活化能( )的大小与
)的大小与 、
、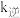 变化程度的关系
变化程度的关系_______ 。
③利用计算机模拟,合成 反应历程如图所示(*表示被催化剂吸附的物种)。
反应历程如图所示(*表示被催化剂吸附的物种)。

该历程中最大活化能
_______ eV,下列叙述正确的是_______ (填标号)。
A.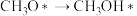 过程中形成了O-H
过程中形成了O-H
B.任何分子均可发生有效碰撞
C.一般情况下,不同催化剂下最大活化能不同
(1)由合成气(组成为H2、CO和少量的CO2)直接制备甲醇,其中的主要过程包括以下两个反应:
i.

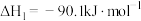
ii.

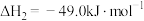
则反应
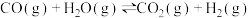


(2)某温度下,
 和
和 投入2L恒容容器中发生反应ii,该反应的速率方程为
投入2L恒容容器中发生反应ii,该反应的速率方程为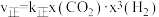 ,
,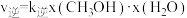 ,
, 、
、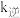 为速率常数且只与温度有关,x为物质的量分数。
为速率常数且只与温度有关,x为物质的量分数。①反应1min时,测得容器中CH3OH(g)为0.32g,则0~1min内

 。
。②达到平衡时,升高温度,
 、
、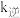 均增大,增大倍数较大的是
均增大,增大倍数较大的是 )的大小与
)的大小与 、
、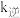 变化程度的关系
变化程度的关系③利用计算机模拟,合成
 反应历程如图所示(*表示被催化剂吸附的物种)。
反应历程如图所示(*表示被催化剂吸附的物种)。
该历程中最大活化能

A.
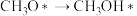 过程中形成了O-H
过程中形成了O-HB.任何分子均可发生有效碰撞
C.一般情况下,不同催化剂下最大活化能不同
您最近一年使用:0次
名校
解题方法
8 . 弱电解质、盐类在生活、生产中应有广泛。回答下列问题:
(1)公元前8世纪晋阳已有醋坊,春秋时期遍及城乡。可利用NaOH标准溶液测定食醋中的酸度(除 外其余物质不与NaOH反应)。
外其余物质不与NaOH反应)。
①滴定管使用前需_______ 和润洗。
②使用_______ (填“酸式”或“碱式”)滴定管量取食醋25.00mL,配制250mL样品溶液。
③量取一定量样品于锥形瓶中,滴加少量_______ (填“甲基橙”或“酚酞”),然后进行滴定。指出滴定终点的现象是_______ ,若滴定过程中有样品液滴溅出锥形瓶,则所测酸度将_______ (填“偏大”、“偏小”或“无影响”)。
④ 溶液中存在关系:
溶液中存在关系:
_______ 。
(2)将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是_______ (写化学式)。
(3)某小组同学探究饱和NaClO和 溶液混合反应的实验。向烧瓶中的NaClO溶液加入饱和
溶液混合反应的实验。向烧瓶中的NaClO溶液加入饱和 溶液,产生大量的白色沉淀。出现上述现象的原因是
溶液,产生大量的白色沉淀。出现上述现象的原因是_______ (请用反应的离子方程式表示)。
(1)公元前8世纪晋阳已有醋坊,春秋时期遍及城乡。可利用NaOH标准溶液测定食醋中的酸度(除
 外其余物质不与NaOH反应)。
外其余物质不与NaOH反应)。①滴定管使用前需
②使用
③量取一定量样品于锥形瓶中,滴加少量
④
 溶液中存在关系:
溶液中存在关系:
(2)将
 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是(3)某小组同学探究饱和NaClO和
 溶液混合反应的实验。向烧瓶中的NaClO溶液加入饱和
溶液混合反应的实验。向烧瓶中的NaClO溶液加入饱和 溶液,产生大量的白色沉淀。出现上述现象的原因是
溶液,产生大量的白色沉淀。出现上述现象的原因是
您最近一年使用:0次
名校
解题方法
9 . 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡: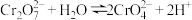
回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积 溶液进行实验,完成下列表格中的填空。
溶液进行实验,完成下列表格中的填空。
(2)利用(1)中所得溶液A、B探究pH对 溶液的氧化性强弱的影响。完成表格中的填空。
溶液的氧化性强弱的影响。完成表格中的填空。
(3)在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中 时,此时溶液中
时,此时溶液中 等于
等于_______  。[已知
。[已知 ]
]
 (橙红色)、
(橙红色)、 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡: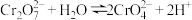
回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积
 溶液进行实验,完成下列表格中的填空。
溶液进行实验,完成下列表格中的填空。| 实验操作 | 实验现象 | 实验结论 |
| 向试管1中加入几滴浓NaOH溶液,得溶液A | 溶液变为① | 其他条件不变时,减小② |
| 向试管2中加入几滴较浓H2SO4溶液,得溶液B | 溶液变为④ | 其他条件不变时,增大生成物浓度,平衡向逆反应方向移动 |
| 向试管2中加入FeSO4,再加入适量NaOH溶液 | 先形成蓝紫色溶液,加入NaOH溶液后产生红褐色沉淀和⑤ | K2Cr2O7溶液具有氧化性,产物不溶于适量NaOH溶液 |
 溶液的氧化性强弱的影响。完成表格中的填空。
溶液的氧化性强弱的影响。完成表格中的填空。| 实验操作 | 实验现象 | 实验结论 |
| 相同量的溶液A、B中分别加入相同量甲醇溶液 | 向溶液A无明显现象,溶液B形成蓝紫色溶液 |
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中 时,此时溶液中
时,此时溶液中 等于
等于 。[已知
。[已知 ]
]
您最近一年使用:0次
名校
10 . 下列叙述正确的是
A.已知 的电离方程式为 的电离方程式为 ,则 ,则 是一元弱酸 是一元弱酸 |
B.pH=2的盐酸和硫酸溶液,硫酸溶液中 是盐酸中 是盐酸中 的2倍 的2倍 |
C.将CO中毒的人转至高压氧仓促使反应 逆向移动 逆向移动 |
D.向 的 的 溶液中加氨水至中性,此时溶液含 溶液中加氨水至中性,此时溶液含 数目小于 数目小于 |
您最近一年使用:0次



