1 . 已知反应 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是
 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是A.转移的电子数目为 |
B. 是由非极性共价键形成的非极性分子 是由非极性共价键形成的非极性分子 |
C.参与反应的 含有孤电子对数为 含有孤电子对数为 |
| D.生成的还原产物质量为56g |
您最近一年使用:0次
2 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4L乙烯含有的 键数目为 键数目为 |
B.58g正丁烷和异丁烷的混合物中共价键数目为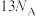 |
C.1mol基态碳原子核外电子占据的原子轨道数目为 |
D.12g金刚石含碳碳单键的数目为 |
您最近一年使用:0次
3 . 下列化学用语表示正确的是
A. 分子的空间填充模型: 分子的空间填充模型: |
B.基态 的价层电子轨道表示式: 的价层电子轨道表示式: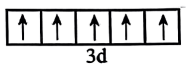 |
C. 的价层电子对互斥模型(VSEPR)模型: 的价层电子对互斥模型(VSEPR)模型: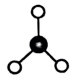 |
D.用原子轨道描述氢原子形成氢分子的过程: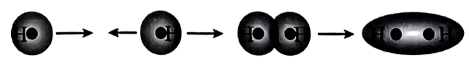 |
您最近一年使用:0次
4 .  表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.1molAl分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子数均为 |
| B.0.2mol的SO2和O2反应,生成的气体体积为4.48L |
C. 的Na2SO4溶液中含有Na+数目为 的Na2SO4溶液中含有Na+数目为 |
D.7.8gNa2O2和Na2S的混合物中含有的阴离子数目为 |
您最近一年使用:0次
解题方法
5 . 在某无色透明的酸性溶液中,能共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
6 . 下列方程式正确的是
A.铜与硫反应: |
B.红热的木炭与浓硫酸反应: |
C.二氧化硫通入氯化钡溶液中: |
D.过量的二氧化硫通入氢氧化钠溶液: |
您最近一年使用:0次
名校
7 . 综合利用废弃物,对资源利用和环境保护具有现实意义。以废铁屑(含少量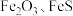 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
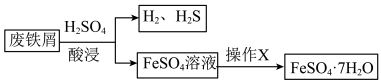
(1)酸浸过程中, 的作用是
的作用是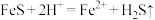 、
、 、
、___________ (用离子方程式表示)。
(2)酸浸时间对所得溶液的成分影响如下表所示。
①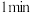 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式___________
② 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因___________ 。
③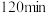 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因___________ 。
(3)已知: 受热易失水。操作X为:
受热易失水。操作X为: ___________ 。
(4)测定所得硫酸亚铁晶体中 的含量,步骤如下:
的含量,步骤如下:
Ⅰ.称取 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。
Ⅱ.取出 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入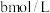 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液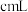 。
。
①依题意完善Ⅱ中 氧化
氧化 的离子方程式
的离子方程式________

 ___________
___________
 ___________
___________
②计算硫酸亚铁晶体样品中 的质量分数
的质量分数___________ 。
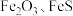 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
(1)酸浸过程中,
 的作用是
的作用是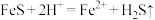 、
、 、
、(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 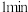 |  |  |
用 溶液检验 溶液检验 | 变红 | 未变红 | 变红 |
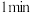 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式②
 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因③
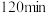 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因(3)已知:
 受热易失水。操作X为:
受热易失水。操作X为: (4)测定所得硫酸亚铁晶体中
 的含量,步骤如下:
的含量,步骤如下:Ⅰ.称取
 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。Ⅱ.取出
 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入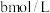 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液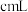 。
。①依题意完善Ⅱ中
 氧化
氧化 的离子方程式
的离子方程式
 ___________
___________
 ___________
___________②计算硫酸亚铁晶体样品中
 的质量分数
的质量分数
您最近一年使用:0次
2024-03-27更新
|
219次组卷
|
4卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 生活处处有化学。下列有关说法错误的是
| A.傍晚看到万丈霞光穿云而过是因为丁达尔效应带来的美景 |
| B.食品包装袋内的铁粉起干燥、抗氧化的作用 |
C.豆科植物的根瘤菌能将空气中的 转化成氨,实现氮的固定 转化成氨,实现氮的固定 |
| D.氧化铁是质地疏松的红色固体,用做颜料为生活带来一抹红 |
您最近一年使用:0次
2024-03-15更新
|
1001次组卷
|
5卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题
河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题(已下线)5.2.1氮气和氮的氧化物课后作业基础篇2024届广东省汕头市高三下学期一模化学试题(已下线)选择题1-5广东省汕头市2024届高三一化学试题
名校
解题方法
9 . 亚硝酸钙[ ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。

①已知: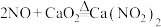 ;
;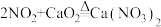 ;
;
②酸性条件下,NO能与 溶液反应生成
溶液反应生成 和
和 。
。
回答下列问题:
(1)检查装置的气密性,装入药品,实验开始前通入一段时间 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是___________ 。
(2)为达到实验目的,请把上述装置按气流方向进行连接:______
A→___________→B→___________→___________
(3)E装置的作用是___________ 。
(4)C装置中反应的离子方程式为___________ 。
(5)工业上可用石灰乳和硝酸工业的尾气(含 ,NO)反应,既能净化尾气,又能获得广泛的
,NO)反应,既能净化尾气,又能获得广泛的 ,反应原理为
,反应原理为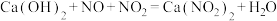 ,若
,若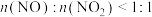 ,则会导致
,则会导致___________ 。
(6)将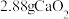 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为___________ mol。
 ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
①已知:
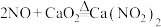 ;
;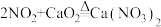 ;
;②酸性条件下,NO能与
 溶液反应生成
溶液反应生成 和
和 。
。回答下列问题:
(1)检查装置的气密性,装入药品,实验开始前通入一段时间
 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是(2)为达到实验目的,请把上述装置按气流方向进行连接:
A→___________→B→___________→___________
(3)E装置的作用是
(4)C装置中反应的离子方程式为
(5)工业上可用石灰乳和硝酸工业的尾气(含
 ,NO)反应,既能净化尾气,又能获得广泛的
,NO)反应,既能净化尾气,又能获得广泛的 ,反应原理为
,反应原理为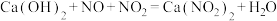 ,若
,若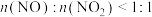 ,则会导致
,则会导致(6)将
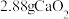 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为
您最近一年使用:0次
2024-03-15更新
|
577次组卷
|
3卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
10 .  、
、 、
、 、
、 、
、 等是氮重要的化合物。
等是氮重要的化合物。 中的一个
中的一个 原子若被
原子若被 取代可形成
取代可形成 (联氨),
(联氨), 经过一定的转化可以形成
经过一定的转化可以形成 、
、 、
、 、
、 (无色)、
(无色)、 等,
等, 与
与 能相互转化。在题给条件下,下列物质间的转化可以实现的是
能相互转化。在题给条件下,下列物质间的转化可以实现的是
 、
、 、
、 、
、 、
、 等是氮重要的化合物。
等是氮重要的化合物。 中的一个
中的一个 原子若被
原子若被 取代可形成
取代可形成 (联氨),
(联氨), 经过一定的转化可以形成
经过一定的转化可以形成 、
、 、
、 、
、 (无色)、
(无色)、 等,
等, 与
与 能相互转化。在题给条件下,下列物质间的转化可以实现的是
能相互转化。在题给条件下,下列物质间的转化可以实现的是A. | B. |
C. | D. |
您最近一年使用:0次
2024-03-15更新
|
351次组卷
|
2卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题



