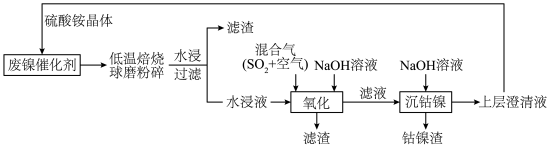
1 . 一种废镍催化剂回收镍、钴元素的工艺流程图如下,流程图中水浸液中含有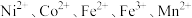 。
。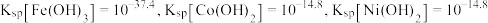 。
。
回答下列问题。
(1)球磨粉碎的作用是_______ 。
(2)“氧化”中,混合气在金属离子的催化作用下,生成具有强氧化性的过一硫酸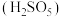 ,其反应的化学方程式为
,其反应的化学方程式为_______ 。
(3)“氧化”中, 被过一硫酸氧化为
被过一硫酸氧化为 沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:
沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:_______ (已知 的电离第一步完全,第二步微弱);用
的电离第一步完全,第二步微弱);用 溶液调节
溶液调节 ,还有
,还有_______ (写离子符号)也会形成沉淀而除去。
(4)“氧化”中保持空气通入速率不变, 的氧化率与
的氧化率与 的体积分数的关系如图所示。
的体积分数的关系如图所示。 的体积分数为9.0%时,
的体积分数为9.0%时, 的氧化率最大;当
的氧化率最大;当 的体积分数大于9.0%时,继续增大
的体积分数大于9.0%时,继续增大 的体积分数,
的体积分数, 的氧化率减小的原因可能是
的氧化率减小的原因可能是_______ 。 沉淀完全,需控制溶液的
沉淀完全,需控制溶液的 不低于
不低于_______ (说明:当溶液中的 浓度均小于
浓度均小于 时,认为已沉淀完全)。
时,认为已沉淀完全)。
(6)铬、钴、镍都属于副族金属元素,其中铬与氮气在一定条件下可以合成氨化铬,且氮化铬的晶体结构及类型与氯化钠的相似,其晶胞结构如图所示。A点的分数坐标为 ,则B点的分数坐标为
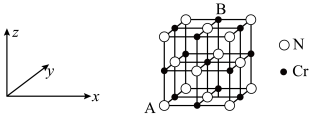
,则B点的分数坐标为_______ 。已知氮化铬的晶胞参数为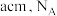 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为_______  。
。
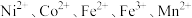 。
。
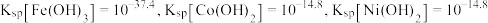 。
。回答下列问题。
(1)球磨粉碎的作用是
(2)“氧化”中,混合气在金属离子的催化作用下,生成具有强氧化性的过一硫酸
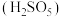 ,其反应的化学方程式为
,其反应的化学方程式为(3)“氧化”中,
 被过一硫酸氧化为
被过一硫酸氧化为 沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:
沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式: 的电离第一步完全,第二步微弱);用
的电离第一步完全,第二步微弱);用 溶液调节
溶液调节 ,还有
,还有(4)“氧化”中保持空气通入速率不变,
 的氧化率与
的氧化率与 的体积分数的关系如图所示。
的体积分数的关系如图所示。 的体积分数为9.0%时,
的体积分数为9.0%时, 的氧化率最大;当
的氧化率最大;当 的体积分数大于9.0%时,继续增大
的体积分数大于9.0%时,继续增大 的体积分数,
的体积分数, 的氧化率减小的原因可能是
的氧化率减小的原因可能是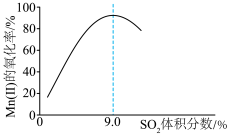
 沉淀完全,需控制溶液的
沉淀完全,需控制溶液的 不低于
不低于 浓度均小于
浓度均小于 时,认为已沉淀完全)。
时,认为已沉淀完全)。(6)铬、钴、镍都属于副族金属元素,其中铬与氮气在一定条件下可以合成氨化铬,且氮化铬的晶体结构及类型与氯化钠的相似,其晶胞结构如图所示。A点的分数坐标为
 ,则B点的分数坐标为
,则B点的分数坐标为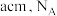 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为 。
。
您最近一年使用:0次
2 . 纳米级硒化锰(MnSe)是一种半导体材料,难溶于水。以锰渣(主要成分是 ,含少量
,含少量 、CuO)为原料制备硒化锰的流程如图所示:
、CuO)为原料制备硒化锰的流程如图所示:
(1)为了提高“酸溶”速率,宜采取的措施有___________ (填两条)。
(2)滤渣1的主要成分之一是单质,“还原”得到的滤液中溶质为 和
和 。写出“还原”反应的离子方程式:
。写出“还原”反应的离子方程式:___________ 。
(3)“氧化”中还原剂、氧化剂的物质的量之比为___________ 。
(4)滤渣2的主要成分是___________ (填化学式)。常温下,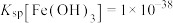 。离子浓度
。离子浓度 时认为该离子已沉淀完全。“除铁”调节pH的最小值为
时认为该离子已沉淀完全。“除铁”调节pH的最小值为___________ 。
(5)“合成”中分离MnSe的操作名称是___________ 。
 ,含少量
,含少量 、CuO)为原料制备硒化锰的流程如图所示:
、CuO)为原料制备硒化锰的流程如图所示: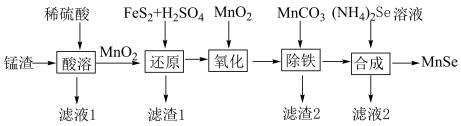
(1)为了提高“酸溶”速率,宜采取的措施有
(2)滤渣1的主要成分之一是单质,“还原”得到的滤液中溶质为
 和
和 。写出“还原”反应的离子方程式:
。写出“还原”反应的离子方程式:(3)“氧化”中还原剂、氧化剂的物质的量之比为
(4)滤渣2的主要成分是
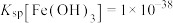 。离子浓度
。离子浓度 时认为该离子已沉淀完全。“除铁”调节pH的最小值为
时认为该离子已沉淀完全。“除铁”调节pH的最小值为(5)“合成”中分离MnSe的操作名称是
您最近一年使用:0次
名校
解题方法
3 . 已知反应: ,
, 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 ,下列叙述的错误的是
,下列叙述的错误的是
 ,
, 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 ,下列叙述的错误的是
,下列叙述的错误的是A.转移电子数为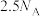 |
B.断裂的 键数为 键数为 |
| C.还原产物比氧化产物多0.5mol |
D.将生成物配制成1L水溶液,溶液中 |
您最近一年使用:0次
解题方法
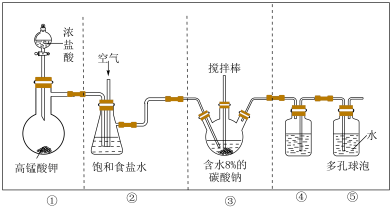
4 . 次氯酸作为消毒剂,被广泛应用于物体表面、织物等污染物品的消毒。某小组涉及如下装置(部分夹持装置略)制备 。
。 混合通入潮湿的碳酸钠中能生成
混合通入潮湿的碳酸钠中能生成 ,且反应放热;
,且反应放热;
ⅱ. 浓度过高时易爆炸,不含
浓度过高时易爆炸,不含 的
的 易与水反应生成
易与水反应生成 ;
;
ⅲ. 在
在 以上会分解。
以上会分解。
请回答下列问题:
(1)写出装置①中发生反应的化学方程式:_____ 。
(2)试从平衡角度分析装置②中试剂选择饱和食盐水的原因:_____ ;饱和食盐水也可替换为_____ 。
(3)制备 的一种产物为
的一种产物为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_____ 。
(4)装置④的作用是_____ ;装置⑤中多孔球泡的作用是_____ 。
(5)实验小组成员发现该套制备装置的设计存在一定问题并制订了修正方案:
a.将装置④的导管改为左长右短;b._____ 。
 。
。
 混合通入潮湿的碳酸钠中能生成
混合通入潮湿的碳酸钠中能生成 ,且反应放热;
,且反应放热;ⅱ.
 浓度过高时易爆炸,不含
浓度过高时易爆炸,不含 的
的 易与水反应生成
易与水反应生成 ;
;ⅲ.
 在
在 以上会分解。
以上会分解。请回答下列问题:
(1)写出装置①中发生反应的化学方程式:
(2)试从平衡角度分析装置②中试剂选择饱和食盐水的原因:
(3)制备
 的一种产物为
的一种产物为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(4)装置④的作用是
(5)实验小组成员发现该套制备装置的设计存在一定问题并制订了修正方案:
a.将装置④的导管改为左长右短;b.
您最近一年使用:0次
解题方法
5 . 一种处理废旧电池正极材料(主要成分为 ),制备三元锂电池正极材料
),制备三元锂电池正极材料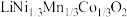 的工业流程如下:
的工业流程如下:
② 时相关物质的溶度积数据如下表。
时相关物质的溶度积数据如下表。
回答下列问题:
(1)基态 价层电子排布图是
价层电子排布图是_____ 。
(2)“酸浸”中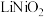 发生反应的化学方程式为
发生反应的化学方程式为_____ ;“酸浸”中 消耗量较大程度地超过理论用量,其原因可能是
消耗量较大程度地超过理论用量,其原因可能是_____ 。
(3)假设正极材料酸浸后溶液中金属阳离子浓度均为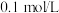 ,则“调
,则“调 ”过程中
”过程中 调控的范围是
调控的范围是_____ (溶液中某离子浓度小于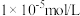 时,视为该离子沉淀完全)。
时,视为该离子沉淀完全)。
(4)“沉锂”过程发生反应的离子方程式为_____ 。
(5)产品的粒径和结晶度直接关系着三元电极的性能。为防止反应中产生的 和
和 影响晶体生长,需在“焙烧”前进行
影响晶体生长,需在“焙烧”前进行_____ (填“预烧”、“酸洗”或“搅拌”)。
(6)某三元锂电池以有机聚合物为电解质,电池放电时总反应方程式为: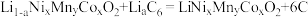 (石墨)
(石墨)
放电时工作装置简图如下,写出放电时A电极的电极反应式_____ 。
 ),制备三元锂电池正极材料
),制备三元锂电池正极材料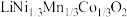 的工业流程如下:
的工业流程如下: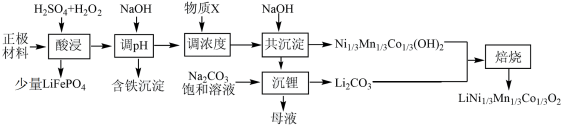

②
 时相关物质的溶度积数据如下表。
时相关物质的溶度积数据如下表。| 物质 |  |  |  |  |
 | 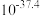 | 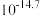 | 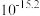 |  |
(1)基态
 价层电子排布图是
价层电子排布图是(2)“酸浸”中
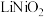 发生反应的化学方程式为
发生反应的化学方程式为 消耗量较大程度地超过理论用量,其原因可能是
消耗量较大程度地超过理论用量,其原因可能是(3)假设正极材料酸浸后溶液中金属阳离子浓度均为
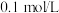 ,则“调
,则“调 ”过程中
”过程中 调控的范围是
调控的范围是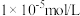 时,视为该离子沉淀完全)。
时,视为该离子沉淀完全)。(4)“沉锂”过程发生反应的离子方程式为
(5)产品的粒径和结晶度直接关系着三元电极的性能。为防止反应中产生的
 和
和 影响晶体生长,需在“焙烧”前进行
影响晶体生长,需在“焙烧”前进行(6)某三元锂电池以有机聚合物为电解质,电池放电时总反应方程式为:
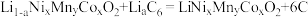 (石墨)
(石墨)放电时工作装置简图如下,写出放电时A电极的电极反应式

您最近一年使用:0次
2024-04-29更新
|
72次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
6 . 实验室用 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是___________ ,还原产物是___________ ;
(2)用单线桥标明电子转移的方向与数目___________ 。
(3)该反应中,氧化剂与还原剂的物质的量之比为___________ (前者比后者);盐酸在反应中表现出来的性质是___________ 。
(4)当生成标准状况下 时,转移的电子数目为
时,转移的电子数目为___________ ,被氧化的还原剂的物质的量为___________ 。
(5)也可以用 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:___________ 。
(6)举例说明氯气的氧化性比硫单质强,___________ 。
 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是
(2)用单线桥标明电子转移的方向与数目
(3)该反应中,氧化剂与还原剂的物质的量之比为
(4)当生成标准状况下
 时,转移的电子数目为
时,转移的电子数目为(5)也可以用
 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:(6)举例说明氯气的氧化性比硫单质强,
您最近一年使用:0次
解题方法
7 . 空气质量日报中涉及的污染物主要是 和可吸入颗粒物。
和可吸入颗粒物。
Ⅰ.汽车尾气是城市大气氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催化转化器”,使 和
和 反应生成可参与大气生态环境循环的无毒气体。
反应生成可参与大气生态环境循环的无毒气体。
(1)以 为例写出反应的化学方程式:
为例写出反应的化学方程式:_________ 。
Ⅱ.SO2的排放是造成酸雨的主要因素,形成酸雨的原理之一可简单表示为:
______________ (填“>”“<”或“=”)5.6。
(3)反应 的化学方程式为
的化学方程式为______________ 。
(4)用足量的氨水吸收 ,其离子方程式为
,其离子方程式为________ 。
(5) 溶液可以吸收含
溶液可以吸收含 的烟气,若
的烟气,若 溶液与
溶液与 恰好反应完全,检验反应后的溶液中是否含有
恰好反应完全,检验反应后的溶液中是否含有 的方法为
的方法为_____________ 。
Ⅲ.利用溶液吸收尾气(主要含 及少量
及少量 )中的氮氧化物,实验装置如图所示.已知:
)中的氮氧化物,实验装置如图所示.已知: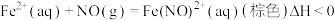
______ 时,说明 中
中 溶液需要更换。
溶液需要更换。
(7)若尾气体积为 (标准状况),用
(标准状况),用 溶液滴定a中溶液,消耗
溶液滴定a中溶液,消耗 溶液体积为
溶液体积为 ,尾气中
,尾气中 的体积分数为
的体积分数为_________ 。
 和可吸入颗粒物。
和可吸入颗粒物。Ⅰ.汽车尾气是城市大气氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催化转化器”,使
 和
和 反应生成可参与大气生态环境循环的无毒气体。
反应生成可参与大气生态环境循环的无毒气体。(1)以
 为例写出反应的化学方程式:
为例写出反应的化学方程式:Ⅱ.SO2的排放是造成酸雨的主要因素,形成酸雨的原理之一可简单表示为:


(3)反应
 的化学方程式为
的化学方程式为(4)用足量的氨水吸收
 ,其离子方程式为
,其离子方程式为(5)
 溶液可以吸收含
溶液可以吸收含 的烟气,若
的烟气,若 溶液与
溶液与 恰好反应完全,检验反应后的溶液中是否含有
恰好反应完全,检验反应后的溶液中是否含有 的方法为
的方法为Ⅲ.利用溶液吸收尾气(主要含
 及少量
及少量 )中的氮氧化物,实验装置如图所示.已知:
)中的氮氧化物,实验装置如图所示.已知: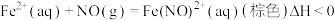

 中
中 溶液需要更换。
溶液需要更换。(7)若尾气体积为
 (标准状况),用
(标准状况),用 溶液滴定a中溶液,消耗
溶液滴定a中溶液,消耗 溶液体积为
溶液体积为 ,尾气中
,尾气中 的体积分数为
的体积分数为
您最近一年使用:0次
解题方法
8 . 氢氧化铈  是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为
是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为 ]制备氢氧化铈的流程如图。下列说法
]制备氢氧化铈的流程如图。下列说法错误 的是
 是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为
是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为 ]制备氢氧化铈的流程如图。下列说法
]制备氢氧化铈的流程如图。下列说法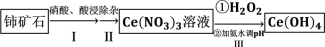
| A.铈是一种常见的稀土元素且属于金属元素 |
B.步骤Ⅰ中发生的反应为 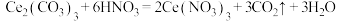 |
| C.步骤Ⅱ中用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
D.步骤Ⅲ中参加反应的氧化剂与还原剂的物质的量之比为 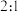 |
您最近一年使用:0次
解题方法
9 .  具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、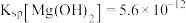 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:___________ ;加入 的目的是
的目的是___________ 。
(2)滤渣1的主要成分为___________ 、___________ 及不溶于酸、碱的杂质;加入 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
___________ 。
(3)若通入过量 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为___________ 。
(4)写出洗去固体A表面杂质的简要操作:___________ 。
(5)“煅烧”固体A反应的化学方程式为___________ 。
 具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、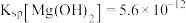 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:
 的目的是
的目的是(2)滤渣1的主要成分为
 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
(3)若通入过量
 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为(4)写出洗去固体A表面杂质的简要操作:
(5)“煅烧”固体A反应的化学方程式为
您最近一年使用:0次
2024-04-25更新
|
191次组卷
|
3卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
名校
解题方法
10 . 已知还原性: ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为
 ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为A. , , , , | B. , , , , | C. , , , , | D. , , , , |
您最近一年使用:0次



