解题方法
1 . 按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
解题方法
2 . 一种制备 的工艺路线如图所示
的工艺路线如图所示
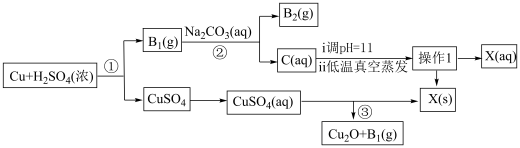
已知:ⅰ.常温下, 的电离平衡常数
的电离平衡常数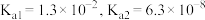
ⅱ.反应②所得C溶液 在
在 之间
之间
ⅲ.反应③需及时补加 以保持反应在
以保持反应在 条件下进行。
条件下进行。
(1)反应①中氧化剂与还原剂物质的量之比为___________ ,溶液C的溶质为___________ (填化学式)。
(2)低温真空蒸发主要目的是___________ ,操作1的名称为___________ 。
(3)写出流程中可以循环利用的物质___________ (填化学式)。
(4)写出反应③的化学反应方程式___________ 。
(5)若 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比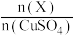 增大时,需补加
增大时,需补加 的量
的量___________ (填“减少”或“增多”或“不变”)。
 的工艺路线如图所示
的工艺路线如图所示
已知:ⅰ.常温下,
 的电离平衡常数
的电离平衡常数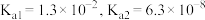
ⅱ.反应②所得C溶液
 在
在 之间
之间ⅲ.反应③需及时补加
 以保持反应在
以保持反应在 条件下进行。
条件下进行。(1)反应①中氧化剂与还原剂物质的量之比为
(2)低温真空蒸发主要目的是
(3)写出流程中可以循环利用的物质
(4)写出反应③的化学反应方程式
(5)若
 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比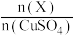 增大时,需补加
增大时,需补加 的量
的量
您最近一年使用:0次
解题方法
3 . 下列说法错误是
A.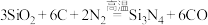 该反应中氧化剂和还原剂个数比为3∶1 该反应中氧化剂和还原剂个数比为3∶1 |
B.已知在碱性溶液中可发生反应: ,则 ,则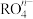 中R的化合价是+6 中R的化合价是+6 |
C.已知 , ,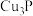 中 中 显+1价,则1个 显+1价,则1个 参与反应时,整个反应转移1个电子 参与反应时,整个反应转移1个电子 |
D.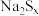 在碱性条件下可被 在碱性条件下可被 氧化为 氧化为 ,而 ,而 被还原为 被还原为 ,若反应中 ,若反应中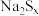 与 与 的个数比为1∶16,则x值为5 的个数比为1∶16,则x值为5 |
您最近一年使用:0次
解题方法
4 . 油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄( )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
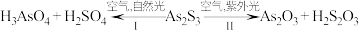
下列说法错误的是
 )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应: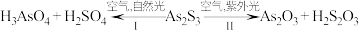
下列说法错误的是
A. 和 和 的空间构型都是正四面体形 的空间构型都是正四面体形 |
| B.反应Ⅰ和Ⅱ中均有两种氧化产物 |
C.反应Ⅰ和Ⅱ中,氧化1  转移的电子数之比为7∶3 转移的电子数之比为7∶3 |
D.反应Ⅰ和Ⅱ中,参加反应 的比值:反应Ⅰ 的比值:反应Ⅰ 反应Ⅱ 反应Ⅱ |
您最近一年使用:0次
解题方法
5 .  用于红外光谱分析以及显像管生产等。以辉锑矿(主要成分为的
用于红外光谱分析以及显像管生产等。以辉锑矿(主要成分为的 ,还含有
,还含有 、PbS、CuO和
、PbS、CuO和 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下:

已知:①浸出液主要含盐酸和 ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;
②常温下, ,
, ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)加快辉锑矿“酸浸”的措施有___________ (答出一条即可);滤渣1中除了S之外,还有___________ 。
(2)浸出液中加入适量Sb的目的是___________ 。
(3)已知浸出液中 、
、 。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是___________ (填化学式);常温下,“除铜、铅”时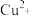 和
和 均沉淀完全,此时溶液中
均沉淀完全,此时溶液中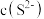 不低于
不低于___________  ,
, 也不宜过多,其原因为
也不宜过多,其原因为___________ 。
(4)在“除砷”过程中,氧化产物为 ,则该反应中氧化剂、还原剂的物质的量之比为
,则该反应中氧化剂、还原剂的物质的量之比为___________ ;已知在“电解” 溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有
溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有___________ 。
 用于红外光谱分析以及显像管生产等。以辉锑矿(主要成分为的
用于红外光谱分析以及显像管生产等。以辉锑矿(主要成分为的 ,还含有
,还含有 、PbS、CuO和
、PbS、CuO和 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①浸出液主要含盐酸和
 ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;②常温下,
 ,
, ;
;③溶液中离子浓度小于或等于
 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。回答下列问题:
(1)加快辉锑矿“酸浸”的措施有
(2)浸出液中加入适量Sb的目的是
(3)已知浸出液中
 、
、 。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是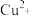 和
和 均沉淀完全,此时溶液中
均沉淀完全,此时溶液中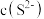 不低于
不低于 ,
, 也不宜过多,其原因为
也不宜过多,其原因为(4)在“除砷”过程中,氧化产物为
 ,则该反应中氧化剂、还原剂的物质的量之比为
,则该反应中氧化剂、还原剂的物质的量之比为 溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有
溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有
您最近一年使用:0次
名校
解题方法
6 . 海洋植物如海带、海藻中含有丰富的碘元素,其中碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如图。
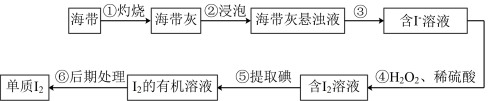
(1)步骤①所用硅酸盐仪器除酒精灯、瓷坩埚外,还有___________ 。
(2)写出步骤④中主要反应的离子方程式:___________ 。
(3)步骤⑤操作的名称为___________ ;若该步骤用的有机溶剂为苯,则得到 的有机溶液的操作为充分振荡放气后,静置分层,
的有机溶液的操作为充分振荡放气后,静置分层,___________ ,该步骤还可选择的有关试剂是___________ (填标号)。
a.酒精 b.四氯化碳 c.饱和食盐水
(4)流程中后期处理用反萃取法:
碘的有机溶液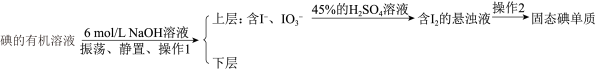
①碘单质与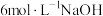 溶液(即浓溶液)发生反应的离子方程式为
溶液(即浓溶液)发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的质量之比为___________ 。
(2) 与
与 在
在 的
的 溶液中能发生反应,反应的化学方程式为
溶液中能发生反应,反应的化学方程式为___________ 。
(5)实验室常用碘量法测定某溶液中 的含量。取
的含量。取 该溶液,加入
该溶液,加入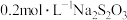 溶液,充分反应后,消耗
溶液,充分反应后,消耗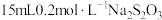 溶液。则该溶液中
溶液。则该溶液中 的含量是
的含量是___________  。(离子方程式为
。(离子方程式为 )
)

(1)步骤①所用硅酸盐仪器除酒精灯、瓷坩埚外,还有
(2)写出步骤④中主要反应的离子方程式:
(3)步骤⑤操作的名称为
 的有机溶液的操作为充分振荡放气后,静置分层,
的有机溶液的操作为充分振荡放气后,静置分层,a.酒精 b.四氯化碳 c.饱和食盐水
(4)流程中后期处理用反萃取法:
碘的有机溶液
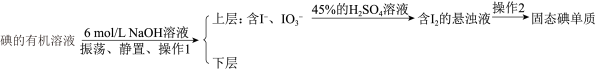
①碘单质与
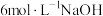 溶液(即浓溶液)发生反应的离子方程式为
溶液(即浓溶液)发生反应的离子方程式为(2)
 与
与 在
在 的
的 溶液中能发生反应,反应的化学方程式为
溶液中能发生反应,反应的化学方程式为(5)实验室常用碘量法测定某溶液中
 的含量。取
的含量。取 该溶液,加入
该溶液,加入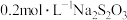 溶液,充分反应后,消耗
溶液,充分反应后,消耗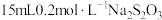 溶液。则该溶液中
溶液。则该溶液中 的含量是
的含量是 。(离子方程式为
。(离子方程式为 )
)
您最近一年使用:0次
名校
7 . 煤燃烧排放的烟气含有 和
和 ,是大气的重要污染源之一、用
,是大气的重要污染源之一、用 溶液对烟气
溶液对烟气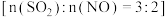 同时脱硫脱硝(分别生成
同时脱硫脱硝(分别生成 、
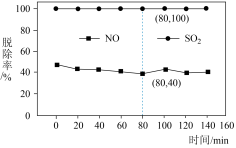
、 ),测得NO、
),测得NO、 脱除率如图,下列说法错误的是
脱除率如图,下列说法错误的是
 和
和 ,是大气的重要污染源之一、用
,是大气的重要污染源之一、用 溶液对烟气
溶液对烟气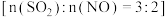 同时脱硫脱硝(分别生成
同时脱硫脱硝(分别生成 、
、 ),测得NO、
),测得NO、 脱除率如图,下列说法错误的是
脱除率如图,下列说法错误的是
A.酸性环境下脱除NO的反应: |
| B.随着脱除反应的进行,吸收溶液的pH逐渐减小 |
C. 脱除率高于NO的原因可能是 脱除率高于NO的原因可能是 在水中的溶解度大于NO 在水中的溶解度大于NO |
D.依据图中信息,在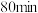 时,吸收液中 时,吸收液中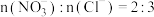 |
您最近一年使用:0次
2023-03-31更新
|
470次组卷
|
6卷引用:山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
8 . 元素的“价—类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。下图为铁元素的“价—类”二维图,图中甲~己均含铁元素。回答下列问题:

(1)下列说法正确的是____
(2)高铁酸盐( )是一种高效净水剂,请结合图像推测其净水原理
)是一种高效净水剂,请结合图像推测其净水原理_______ 。
(3)在戊的溶液中滴加烧碱溶液并放置一段时间的现象是_______ ,在放置过程时的反应化学方程式为_______ 。
(4)已知甲与稀硝酸反应的化学方程式为: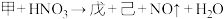 (未配平)。若产物中戊和己的物质的量之比为3:1,还原剂与氧化剂分别为
(未配平)。若产物中戊和己的物质的量之比为3:1,还原剂与氧化剂分别为_______ 和_______ ,二者的物质的量之比为_______ ,该反应的化学方程式_______ 。

(1)下列说法正确的是____
| A.铁与高温水蒸气的反应可实现上述甲到乙的转化 |
B. 是一种黑色粉末,不稳定,在空气中受热时迅速转化为红棕色粉末 是一种黑色粉末,不稳定,在空气中受热时迅速转化为红棕色粉末 |
| C.向戊的水溶液中滴加硫氰化钾溶液后溶液会变成血红色 |
| D.在空气中加热丙会生成红棕色固体 |
 )是一种高效净水剂,请结合图像推测其净水原理
)是一种高效净水剂,请结合图像推测其净水原理(3)在戊的溶液中滴加烧碱溶液并放置一段时间的现象是
(4)已知甲与稀硝酸反应的化学方程式为:
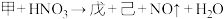 (未配平)。若产物中戊和己的物质的量之比为3:1,还原剂与氧化剂分别为
(未配平)。若产物中戊和己的物质的量之比为3:1,还原剂与氧化剂分别为
您最近一年使用:0次
2023-01-10更新
|
178次组卷
|
3卷引用:山东省曹县第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 锰酸锂离子蓄电池是第二代锂离子动力电池,性能优良。工业上用某软锰矿(主要成分为MnO2,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂(LiMn2O4)。流程如图:
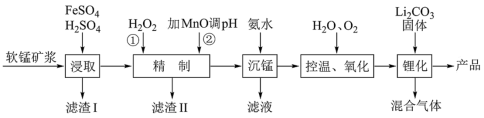
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为______ 。
(2)滤渣II的主要成分是______ ;“精制”中加入H2O2的量比理论值大得多,其主要原因是_____ 。
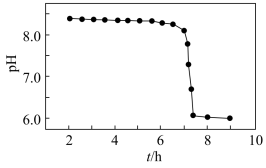
(3)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为MnO2,若控温氧化时溶液的pH随时间的变化如图,其中pH下降的原因是______ (用化学方程式表示)。
(4)工业上也可以将“精制”后的滤液加入K2S2O8来合成MnO2。K2S2O8中S的化合价为 价,加入K2S2O8溶液合成MnO2发生反应的离子方程式为
价,加入K2S2O8溶液合成MnO2发生反应的离子方程式为______ 。
(5)“锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是_____ 。
(6)为测定成品锰酸锂的纯度,实验室可通过连续滴定法测定锰酸锂中锰元素的平均价态。
进行如下实验:
步骤1:取少量成品锰酸锂(假设为LiMnxOy)分成两等份,分别置于两只锥形瓶中;
步骤2:向一只锥形瓶中加入稀硝酸和双氧水,完全反应后,LiMnxOy中Mn元素转化为Mn2+,除去过量的双氧水。调节pH,滴加指示剂,用浓度为0.300mol•L-1的EDTA标准溶液滴定,终点时消耗EDTA标准溶液20.00mL(已知:Mn2+与EDTA反应的化学计量数之比为1∶1);
步骤3:向另一锥形瓶中加入1.340gNa2C2O4和足量硫酸,充分反应后,用0.100mol•L-1KMnO4标准溶液滴定,到达滴定终点时消耗KMnO4标准溶液20.80mL。
已知:LiMnxOy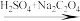 Mn2+,则此成品锰酸锂LiMnxOy中Mn元素的平均化合价为
Mn2+,则此成品锰酸锂LiMnxOy中Mn元素的平均化合价为______ 。

(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为
(2)滤渣II的主要成分是
(3)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为MnO2,若控温氧化时溶液的pH随时间的变化如图,其中pH下降的原因是

(4)工业上也可以将“精制”后的滤液加入K2S2O8来合成MnO2。K2S2O8中S的化合价为
 价,加入K2S2O8溶液合成MnO2发生反应的离子方程式为
价,加入K2S2O8溶液合成MnO2发生反应的离子方程式为(5)“锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是
(6)为测定成品锰酸锂的纯度,实验室可通过连续滴定法测定锰酸锂中锰元素的平均价态。
进行如下实验:
步骤1:取少量成品锰酸锂(假设为LiMnxOy)分成两等份,分别置于两只锥形瓶中;
步骤2:向一只锥形瓶中加入稀硝酸和双氧水,完全反应后,LiMnxOy中Mn元素转化为Mn2+,除去过量的双氧水。调节pH,滴加指示剂,用浓度为0.300mol•L-1的EDTA标准溶液滴定,终点时消耗EDTA标准溶液20.00mL(已知:Mn2+与EDTA反应的化学计量数之比为1∶1);
步骤3:向另一锥形瓶中加入1.340gNa2C2O4和足量硫酸,充分反应后,用0.100mol•L-1KMnO4标准溶液滴定,到达滴定终点时消耗KMnO4标准溶液20.80mL。
已知:LiMnxOy
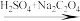 Mn2+,则此成品锰酸锂LiMnxOy中Mn元素的平均化合价为
Mn2+,则此成品锰酸锂LiMnxOy中Mn元素的平均化合价为
您最近一年使用:0次
2023-01-10更新
|
598次组卷
|
3卷引用:山东省烟台第一中学2022-2023学年高一上学期月考化学试题
名校
解题方法
10 . 将 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体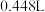 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是
 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体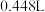 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是A.原混合物中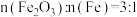 |
B.原混合物中氧化铁的质量为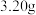 |
C.向所得溶液中滴加 溶液,溶液显红色 溶液,溶液显红色 |
D.向所得溶液中通入 ,可以将 ,可以将 完全转化为 完全转化为 |
您最近一年使用:0次
2023-01-01更新
|
586次组卷
|
5卷引用:山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题



