名校
1 . 工业上以钛铁矿(主要成分为 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: 反应。回答下列问题:
反应。回答下列问题:
(1)矿渣的主要成分是__________ ;试剂A为__________ (填化学式)。
(2)“操作Ⅱ”为__________ 、__________ 、过滤、洗涤、干燥。
(3)沸腾氯化中,氯气与矿料逆流而行,目的是__________ ,充分反应后,混合气体中CO与 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为__________ 。
(4)高温下镁与 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是__________ (填选项)。
a. b.
b. c.
c. d.Ar
d.Ar
 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: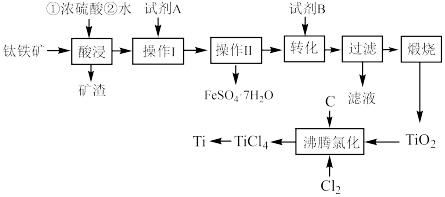
 反应。回答下列问题:
反应。回答下列问题:(1)矿渣的主要成分是
(2)“操作Ⅱ”为
(3)沸腾氯化中,氯气与矿料逆流而行,目的是
 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为(4)高温下镁与
 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是a.
 b.
b. c.
c. d.Ar
d.Ar
您最近一年使用:0次
名校
解题方法
2 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中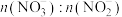 都为
都为 。下列说法错误的是
。下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中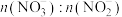 都为
都为 。下列说法错误的是
。下列说法错误的是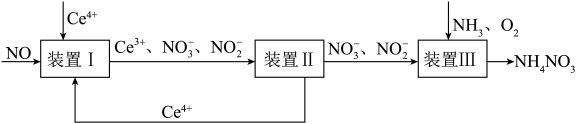
A.装置Ⅰ中若有 参与反应,则转移 参与反应,则转移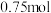 电子 电子 |
B.装置Ⅰ中反应为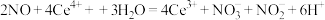 |
C.装置Ⅲ中氧化剂和还原剂的物质的量之比为 |
D.装置Ⅲ中 和 和 的体积比 的体积比 时,可实现原子利用率最大化 时,可实现原子利用率最大化 |
您最近一年使用:0次
3 . 化学与生活、生产息息相关。请回答下列问题:
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为_______ 。
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为_______ 。
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式_______ :
_______C+_______K2Cr2O7+_______H2SO4=_______K2SO4+_______CO2↑+_______Cr2(SO4)3+_______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为_______ 。
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式
_______C+_______K2Cr2O7+_______H2SO4=_______K2SO4+_______CO2↑+_______Cr2(SO4)3+_______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为
您最近一年使用:0次
名校
4 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 。
。
(1)水晶和玛瑙的主要成分均为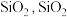 为
为___________ (填“酸性”、“碱性”或“两性”)氧化物,写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:___________ 。
(2)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。
(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;
③ 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。
Ⅰ.第②步制备 反应的化学方程式为:
反应的化学方程式为:___________ ,步骤①②③中属于氧化还原反应的是___________ (填序号)。
Ⅱ.整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:___________ 。
 。
。(1)水晶和玛瑙的主要成分均为
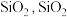 为
为 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:(2)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥
 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;③
 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。Ⅰ.第②步制备
 反应的化学方程式为:
反应的化学方程式为:Ⅱ.整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 碘化亚铜(CuI)是白色粉末,不溶于水和乙醇,溶于浓硫酸,易被氧化,常用作有机反应催化剂、阳极射线管覆盖物、动物饲料添加剂等。在实验室制备CuI的装置如图所示(部分夹持装置已省略)。
(1)装置D的作用是除去SO2中的H2SO4蒸气,盛放的溶液是___________(填选项字母)。
(2)按气流从左到右的方向,各装置的连接顺序为a→___________ (填仪器接口小写字母)。
(3)装置C中发生反应的化学方程式为___________ 。
(4)实验结束时的现象是___________ 。
(5)实验结束后,熄灭装置A中的酒精灯,打开K,向装置内鼓入N2一段时间,其目的是___________ 。
(6)先用装置B中的溶液洗涤制得的CuI,然后再用无水乙醇洗涤,可能的原因是___________ 。
(7)准确称取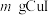 样品,加入足量
样品,加入足量 溶液,发生反应
溶液,发生反应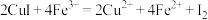 ,待样品完全反应后,用
,待样品完全反应后,用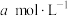 酸性
酸性 溶液滴定
溶液滴定 ,消耗
,消耗 溶液的体积为
溶液的体积为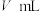 ,则样品中
,则样品中 的质量分数为
的质量分数为___________ 。(用含a、V、m的代数式表示,列出计算式即可)

(1)装置D的作用是除去SO2中的H2SO4蒸气,盛放的溶液是___________(填选项字母)。
| A.品红溶液 | B.NaOH溶液 | C.饱和NaHSO3溶液 | D.饱和Na2SO3溶液 |
(2)按气流从左到右的方向,各装置的连接顺序为a→
(3)装置C中发生反应的化学方程式为
(4)实验结束时的现象是
(5)实验结束后,熄灭装置A中的酒精灯,打开K,向装置内鼓入N2一段时间,其目的是
(6)先用装置B中的溶液洗涤制得的CuI,然后再用无水乙醇洗涤,可能的原因是
(7)准确称取
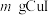 样品,加入足量
样品,加入足量 溶液,发生反应
溶液,发生反应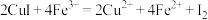 ,待样品完全反应后,用
,待样品完全反应后,用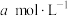 酸性
酸性 溶液滴定
溶液滴定 ,消耗
,消耗 溶液的体积为
溶液的体积为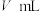 ,则样品中
,则样品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
6 . 碲( )是第ⅥA族元素,可用作合金材料的添加剂、催化剂等。一种利用含碲废料(主要成分是
)是第ⅥA族元素,可用作合金材料的添加剂、催化剂等。一种利用含碲废料(主要成分是 、
、 )制取粗碲、
)制取粗碲、 固体的工艺流程如图所示。
固体的工艺流程如图所示。 属于两性氧化物,难溶于水,易溶于强酸和强碱,分别生成
属于两性氧化物,难溶于水,易溶于强酸和强碱,分别生成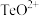 和
和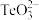 。
。
回答下列问题:
(1)“焙烧”过程在焙烧炉内完成,焙烧炉内壁材料可以为___________(填标号)。
(2)“焙烧”常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是___________ ;“焙烧”时, 转化为
转化为 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)“调 ”时控制
”时控制 为
为 ,此时生成
,此时生成 的离子方程式为
的离子方程式为___________ ;加入硫酸的量不宜过多,其原因是___________ 。
(4)“还原”时,获得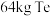 理论上需要标准状况下
理论上需要标准状况下 的体积为
的体积为___________  ;流程中可以循环利用的物质是
;流程中可以循环利用的物质是___________ (填化学式)。
(5)获得 固体“一系列操作”包含
固体“一系列操作”包含___________ 、过滤、洗涤、干燥。
 )是第ⅥA族元素,可用作合金材料的添加剂、催化剂等。一种利用含碲废料(主要成分是
)是第ⅥA族元素,可用作合金材料的添加剂、催化剂等。一种利用含碲废料(主要成分是 、
、 )制取粗碲、
)制取粗碲、 固体的工艺流程如图所示。
固体的工艺流程如图所示。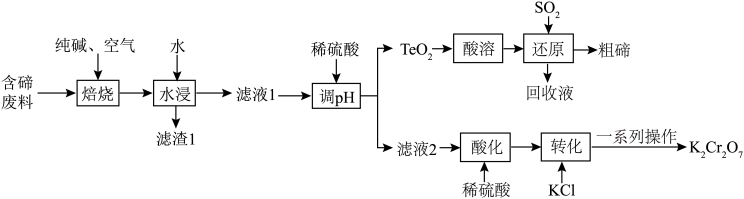
 属于两性氧化物,难溶于水,易溶于强酸和强碱,分别生成
属于两性氧化物,难溶于水,易溶于强酸和强碱,分别生成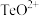 和
和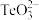 。
。回答下列问题:
(1)“焙烧”过程在焙烧炉内完成,焙烧炉内壁材料可以为___________(填标号)。
A. | B. | C. | D. |
(2)“焙烧”常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是
 转化为
转化为 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(3)“调
 ”时控制
”时控制 为
为 ,此时生成
,此时生成 的离子方程式为
的离子方程式为(4)“还原”时,获得
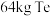 理论上需要标准状况下
理论上需要标准状况下 的体积为
的体积为 ;流程中可以循环利用的物质是
;流程中可以循环利用的物质是(5)获得
 固体“一系列操作”包含
固体“一系列操作”包含
您最近一年使用:0次
名校
7 . 含硫石油、煤、天然气的燃烧,硫化矿石的熔炼和焙烧,及各种含硫原料的加工生产过程等均能产生二氧化硫。
(1)画出硫原子的原子结构示意图_______ 。
(2)实验室常用亚硫酸钠固体和70%的浓硫酸反应制取二氧化硫,该反应的化学方程式_______ ;用该方法制备 时,能随时控制反应速率的装置是
时,能随时控制反应速率的装置是_______ (填标号),原因是_______ 。 的含量,某小组同学将空气样品经过管道通入盛有
的含量,某小组同学将空气样品经过管道通入盛有 酸性
酸性 溶液的密闭容器中,若管道中空气流量为
溶液的密闭容器中,若管道中空气流量为 ,经过
,经过 恰好使酸性
恰好使酸性 溶液完全褪色(假定样品中的
溶液完全褪色(假定样品中的 可被溶液充分吸收且样品中其他成分不与
可被溶液充分吸收且样品中其他成分不与 反应)。
反应)。
①写出上述反应的离子方程式_______ 。
②该空气样品中 的含量为
的含量为_______  。
。
(4)为了减少二氧化硫产生的危害,可以采取的措施是_______ 。
(1)画出硫原子的原子结构示意图
(2)实验室常用亚硫酸钠固体和70%的浓硫酸反应制取二氧化硫,该反应的化学方程式
 时,能随时控制反应速率的装置是
时,能随时控制反应速率的装置是A. B.
B. C.
C.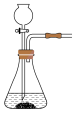 D.
D.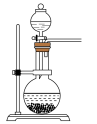
 的含量,某小组同学将空气样品经过管道通入盛有
的含量,某小组同学将空气样品经过管道通入盛有 酸性
酸性 溶液的密闭容器中,若管道中空气流量为
溶液的密闭容器中,若管道中空气流量为 ,经过
,经过 恰好使酸性
恰好使酸性 溶液完全褪色(假定样品中的
溶液完全褪色(假定样品中的 可被溶液充分吸收且样品中其他成分不与
可被溶液充分吸收且样品中其他成分不与 反应)。
反应)。①写出上述反应的离子方程式
②该空气样品中
 的含量为
的含量为 。
。(4)为了减少二氧化硫产生的危害,可以采取的措施是
您最近一年使用:0次
名校
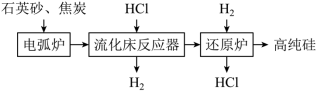
8 . 高纯硅用于制作光伏电池,如图是一种生产高纯硅的工艺流程图: ;
;
②还原炉的主反应: ;
;
③SiHCl3极易水解。回答下列问题:
(1)Si在元素周期表中的位置为________ 。石英砂的主要成分为SiO2,能溶于HF的水溶液,写出其化学方程式________ 。
(2)电弧炉中生成粗硅,反应的化学方程式为________ 。若电弧炉中焦炭过量,还会有SiC生成,石英砂和焦炭生成SiC的反应中,氧化剂和还原剂的物质的量之比为________ 。
(3)整个操作流程都需隔绝空气,原因是________ (答出两条 即可)。
(4)SiHCl3极易发生水解反应,其生成物之一是一种可燃性气体,则SiHCl3水解的化学方程式为________ 。
(5)上述操作流程中可以循环利用的物质是________ 。
 ;
;②还原炉的主反应:
 ;
;③SiHCl3极易水解。回答下列问题:
(1)Si在元素周期表中的位置为
(2)电弧炉中生成粗硅,反应的化学方程式为
(3)整个操作流程都需隔绝空气,原因是
(4)SiHCl3极易发生水解反应,其生成物之一是一种可燃性气体,则SiHCl3水解的化学方程式为
(5)上述操作流程中可以循环利用的物质是
您最近一年使用:0次
名校
9 . 在溶液中用光照射 催化剂产生光电子和空穴
催化剂产生光电子和空穴 ,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
 催化剂产生光电子和空穴
催化剂产生光电子和空穴 ,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是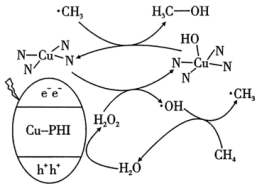
A.空穴 参与发生的反应为 参与发生的反应为 |
| B.反应过程中有非极性键的生成,没有非极性键的断裂 |
| C.生成的甲醇因能与水形成分子间氢键而易溶于水 |
D.该反应的化学方程式为 |
您最近一年使用:0次
名校
解题方法
10 . 如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ ,体现了c的_____ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是_____ (填化学式)。
(3)将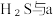 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为_____ 。
(4)配平下列反应:_____ 。
_____
(5)为防止多余的a气体污染环境,应将尾气通入_____ 溶液中;
(6)将足量的 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填字母)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀

(7)将 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为_____ 。 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:_____ 。
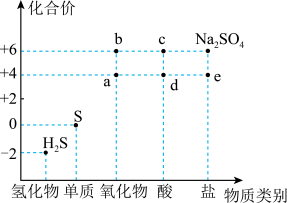
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是
(3)将
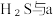 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应:
_____

(5)为防止多余的a气体污染环境,应将尾气通入
(6)将足量的
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(7)将
 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为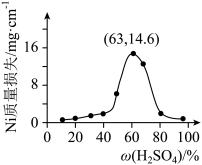
 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近一年使用:0次



