1 . (1)白色固体PCl5受热即挥发并发生分解:PCl5(g)  PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105 Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,平衡时PCl5的分解率为
PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105 Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,平衡时PCl5的分解率为________ 。
(2)下列微粒在溶液中的还原性和氧化性强弱顺序如下:还原性HSO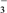 >I-,氧化性IO
>I-,氧化性IO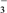 >I2>SO
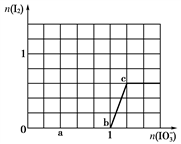
>I2>SO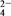 。向含有x mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示,则x为
。向含有x mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示,则x为________ mol。
(3)甲醇对水质会造成一定的污染,可细菌的作用下,用氨(NH3)处理含甲醇(CH3OH)的工业废水,使其变成无毒的CO2和N2,从而消除对环境的污染,化学方程式为:_____________________ ,该过程中被氧化的元素是 ___________ ,当产生标准状况下2.24L 时,共转移电子
时,共转移电子_______ mol。
 PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105 Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,平衡时PCl5的分解率为
PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105 Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,平衡时PCl5的分解率为(2)下列微粒在溶液中的还原性和氧化性强弱顺序如下:还原性HSO
 >I-,氧化性IO
>I-,氧化性IO >I2>SO
>I2>SO 。向含有x mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示,则x为
。向含有x mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示,则x为
(3)甲醇对水质会造成一定的污染,可细菌的作用下,用氨(NH3)处理含甲醇(CH3OH)的工业废水,使其变成无毒的CO2和N2,从而消除对环境的污染,化学方程式为:
 时,共转移电子
时,共转移电子
您最近一年使用:0次
解题方法
2 . 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
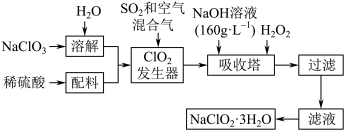
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO3•3H2O;
②纯ClO2易分解爆炸, 一般用稀有气体或空气稀释到 10% 以下较安全;
③HClO2 可看成是强酸;
④ClO2常温下为气态 。
(1)160 g•L-1 NaOH溶液的物质的量浓度为______________ mol•L-1,若要计算该溶液溶质的质量分数,还需要的一个条件是_______________________ 。
(2)在发生器中鼓入空气的作用可能是______________ (填序号)。
A. 将 SO2氧化成SO3,增强酸性
B. 稀释 ClO2以防止爆炸
C. 将 NaClO3氧化成ClO2
(3)ClO2 发生器中发生的化学反应方程式为_____ ,吸收塔内的反应的离子反应方程式为_______ ;
(4)吸收塔中为防止 NaClO2被 还原成 NaCl所用还原剂的还原性应适中。 除H2O2外,还可以选择的还原剂是_____ (填序号)。
A Na2O2 B Na2S C FeCl2 D O3

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO3•3H2O;
②纯ClO2易分解爆炸, 一般用稀有气体或空气稀释到 10% 以下较安全;
③HClO2 可看成是强酸;
④ClO2常温下为气态 。
(1)160 g•L-1 NaOH溶液的物质的量浓度为
(2)在发生器中鼓入空气的作用可能是
A. 将 SO2氧化成SO3,增强酸性
B. 稀释 ClO2以防止爆炸
C. 将 NaClO3氧化成ClO2
(3)ClO2 发生器中发生的化学反应方程式为
(4)吸收塔中为防止 NaClO2被 还原成 NaCl所用还原剂的还原性应适中。 除H2O2外,还可以选择的还原剂是
A Na2O2 B Na2S C FeCl2 D O3
您最近一年使用:0次
3 . 为探索稳定性 溶液对氮氧化物(
溶液对氮氧化物( )的处理效果,实验过程如下:
)的处理效果,实验过程如下: 具有强氧化性,且氧化性随着溶液的酸性增强而增强。
具有强氧化性,且氧化性随着溶液的酸性增强而增强。 和NaOH反应的化学方程式为:
和NaOH反应的化学方程式为: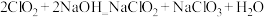 。
。 对氮氧化物具有强吸收效果。
对氮氧化物具有强吸收效果。
(1)“制气”阶段生成 、NO和
、NO和 。“制气”反应的化学方程式为
。“制气”反应的化学方程式为___________ 。
(2) 可以将NO氧化为
可以将NO氧化为 ,并进一步将
,并进一步将 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图-1所示)。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图-1所示)。 的吸收率与吸收器内碎瓷片填料的高度关系如图-2所示。
的吸收率与吸收器内碎瓷片填料的高度关系如图-2所示。 和
和 反应的离子方程式为
反应的离子方程式为___________ 。
②随着吸收器内填料高度增加, 去除率增高的原因是
去除率增高的原因是___________ 。
(3)通过加入盐酸或NaOH调节 溶液的pH,测得不同pH的
溶液的pH,测得不同pH的 溶液对
溶液对 吸收率的影响如图-3所示。
吸收率的影响如图-3所示。 吸收率随pH增大而减小的原因是
吸收率随pH增大而减小的原因是___________ 。
②当pH大于7时, 吸收率随pH增大而增大的原因是
吸收率随pH增大而增大的原因是___________ 。
 溶液对氮氧化物(
溶液对氮氧化物( )的处理效果,实验过程如下:
)的处理效果,实验过程如下: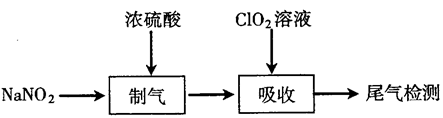
 具有强氧化性,且氧化性随着溶液的酸性增强而增强。
具有强氧化性,且氧化性随着溶液的酸性增强而增强。 和NaOH反应的化学方程式为:
和NaOH反应的化学方程式为: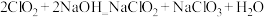 。
。 对氮氧化物具有强吸收效果。
对氮氧化物具有强吸收效果。(1)“制气”阶段生成
 、NO和
、NO和 。“制气”反应的化学方程式为
。“制气”反应的化学方程式为(2)
 可以将NO氧化为
可以将NO氧化为 ,并进一步将
,并进一步将 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图-1所示)。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图-1所示)。 的吸收率与吸收器内碎瓷片填料的高度关系如图-2所示。
的吸收率与吸收器内碎瓷片填料的高度关系如图-2所示。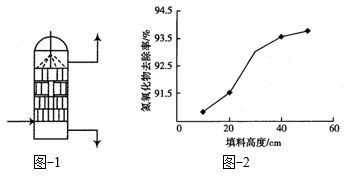
 和
和 反应的离子方程式为
反应的离子方程式为②随着吸收器内填料高度增加,
 去除率增高的原因是
去除率增高的原因是(3)通过加入盐酸或NaOH调节
 溶液的pH,测得不同pH的
溶液的pH,测得不同pH的 溶液对
溶液对 吸收率的影响如图-3所示。
吸收率的影响如图-3所示。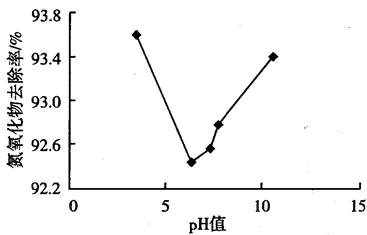
 吸收率随pH增大而减小的原因是
吸收率随pH增大而减小的原因是②当pH大于7时,
 吸收率随pH增大而增大的原因是
吸收率随pH增大而增大的原因是
您最近一年使用:0次
2021-06-27更新
|
486次组卷
|
3卷引用:辽宁省葫芦岛市普通高中2021-2022学年高一下学期期末学业质量监测化学试题
4 . 黄铁矿(FeS2)中-1价硫元素在酸性条件下可以与ClO3-发生反应,其离子方程式如下
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
| A. ClO3-是氧化剂,Fe3+是还原产物 |
| B. ClO3-的氧化性强于Fe3+ |
| C.生成l mol SO42-时,转移7mol 电子 |
| D.取反应后的溶液加KSCN溶液,可观察到有红色沉淀产生 |
您最近一年使用:0次
2020-02-20更新
|
569次组卷
|
3卷引用:辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题
辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的规律:先后律、强弱律【精编选择25题】(已下线)考点05 氧化还原反应方程式的配平与计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
5 . 超细银粉在光学、生物医疗等领域有着广阔的应用前景。由含银废催化剂制备超细银粉的过程如下:
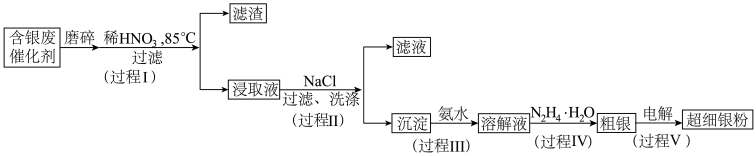
资料:
i.含银废催化剂成分:主要含Ag、 及少量MgO、
及少量MgO、 、
、 、
、 等
等
ii. 为载体,且不溶于硝酸
为载体,且不溶于硝酸
iii.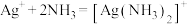
(1)预处理
过程I中,为提高银的浸取速率采取的措施有_______
(2)分离除杂
①过程Ⅱ中,检验沉淀表面的 已洗涤干净的操作是
已洗涤干净的操作是_______ 。
②过程Ⅲ中,请结合平衡移动原理解释沉淀溶解的原因_______ 。
③过程Ⅳ中, 被氧化为
被氧化为 ,同时获得粗银,该反应的离子方程式为
,同时获得粗银,该反应的离子方程式为_______ 。
(3)回收率测定
采用如下方法测定粗银中银的回收率:取m g粗银样品用硝酸溶解,以铁铵矾[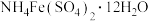 ]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
已知:i. (白色)
(白色) 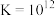
 (红色)
(红色) 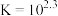
ii. 开始沉淀的pH为1.5,完全沉淀的pH为2.8
开始沉淀的pH为1.5,完全沉淀的pH为2.8
iii.AgSCN可溶于较浓硝酸判断已达滴定终点时的现象是_______ 。
(4)精炼
①精炼时粗银应连接电源_______ 极;
②电解质溶液中溶质为_______ 。

资料:
i.含银废催化剂成分:主要含Ag、
 及少量MgO、
及少量MgO、 、
、 、
、 等
等ii.
 为载体,且不溶于硝酸
为载体,且不溶于硝酸iii.
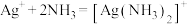
(1)预处理
过程I中,为提高银的浸取速率采取的措施有
(2)分离除杂
①过程Ⅱ中,检验沉淀表面的
 已洗涤干净的操作是
已洗涤干净的操作是②过程Ⅲ中,请结合平衡移动原理解释沉淀溶解的原因
③过程Ⅳ中,
 被氧化为
被氧化为 ,同时获得粗银,该反应的离子方程式为
,同时获得粗银,该反应的离子方程式为(3)回收率测定
采用如下方法测定粗银中银的回收率:取m g粗银样品用硝酸溶解,以铁铵矾[
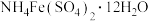 ]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。已知:i.
 (白色)
(白色) 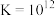
 (红色)
(红色) 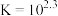
ii.
 开始沉淀的pH为1.5,完全沉淀的pH为2.8
开始沉淀的pH为1.5,完全沉淀的pH为2.8iii.AgSCN可溶于较浓硝酸判断已达滴定终点时的现象是
(4)精炼
①精炼时粗银应连接电源
②电解质溶液中溶质为
您最近一年使用:0次
2023-01-05更新
|
300次组卷
|
2卷引用:辽宁省沈阳市东北育才学校2022-2023学年高二上学期期末测试化学试题
6 . 硫酸氧钒(VOSO4)对高血糖、高血脂有治疗作用,也是钒电池不可或缺的电解质。制备 的实验流程如下:
的实验流程如下:
①向仪器a中加入 ,打开仪器b滴入一定量的浓硫酸,在85℃搅拌下充分反应,得到橙红色的
,打开仪器b滴入一定量的浓硫酸,在85℃搅拌下充分反应,得到橙红色的 溶液;
溶液;
②冷却后,向所得溶液中加入草酸(H2C2O4)充分搅拌,得到 溶液(蓝黑色);
溶液(蓝黑色);
③ 溶液经结晶、过滤得到纯蓝色的
溶液经结晶、过滤得到纯蓝色的 晶体,
晶体, 晶体脱水、干燥,得到
晶体脱水、干燥,得到 产品。
产品。
实验装置如图所示(夹持、加热装置及磁力搅拌器已省略)。回答下列问题:

(1)仪器c的名称是_______ ,用仪器b滴加浓硫酸时,_______ (填“需要”或“不需要”)打开上端的玻璃塞。
(2)反应中最适宜的加热方式为_______ ,在a中反应生成
_______ (“是”或“不是”)氧化还原反应。
(3)反应液由橙红色变为蓝黑色的化学方程式为_______ 。
(4)纯度测定:准确称取 产品m g,配成100mL溶液,用
产品m g,配成100mL溶液,用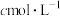 的酸性
的酸性 溶液滴定(滴定反应的产物中,V元素为+5价,Mn元素为+2价),滴定终点时,消耗酸性
溶液滴定(滴定反应的产物中,V元素为+5价,Mn元素为+2价),滴定终点时,消耗酸性 溶液的体积为V mL,
溶液的体积为V mL, 的摩尔质量为
的摩尔质量为 ,则该产品的纯度为
,则该产品的纯度为_______ %。
(5)性质探究:查阅资料后,有同学对 的热分解提出了两种猜想:
的热分解提出了两种猜想:
猜想ⅰ. ;
;
猜想ⅱ.
欲采用如下装置探究:
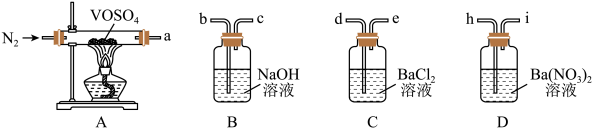
选择必要的仪器装置,按气流从左到右的流向,探究分解产物的导管接口顺序为a→_______ ;若气体流经的装置均有气泡产生,则上述所选必要装置中可观察的现象为_______ ,证明猜想ⅱ正确。
 的实验流程如下:
的实验流程如下:①向仪器a中加入
 ,打开仪器b滴入一定量的浓硫酸,在85℃搅拌下充分反应,得到橙红色的
,打开仪器b滴入一定量的浓硫酸,在85℃搅拌下充分反应,得到橙红色的 溶液;
溶液;②冷却后,向所得溶液中加入草酸(H2C2O4)充分搅拌,得到
 溶液(蓝黑色);
溶液(蓝黑色);③
 溶液经结晶、过滤得到纯蓝色的
溶液经结晶、过滤得到纯蓝色的 晶体,
晶体, 晶体脱水、干燥,得到
晶体脱水、干燥,得到 产品。
产品。实验装置如图所示(夹持、加热装置及磁力搅拌器已省略)。回答下列问题:

(1)仪器c的名称是
(2)反应中最适宜的加热方式为

(3)反应液由橙红色变为蓝黑色的化学方程式为
(4)纯度测定:准确称取
 产品m g,配成100mL溶液,用
产品m g,配成100mL溶液,用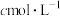 的酸性
的酸性 溶液滴定(滴定反应的产物中,V元素为+5价,Mn元素为+2价),滴定终点时,消耗酸性
溶液滴定(滴定反应的产物中,V元素为+5价,Mn元素为+2价),滴定终点时,消耗酸性 溶液的体积为V mL,
溶液的体积为V mL, 的摩尔质量为
的摩尔质量为 ,则该产品的纯度为
,则该产品的纯度为(5)性质探究:查阅资料后,有同学对
 的热分解提出了两种猜想:
的热分解提出了两种猜想:猜想ⅰ.
 ;
;猜想ⅱ.

欲采用如下装置探究:

选择必要的仪器装置,按气流从左到右的流向,探究分解产物的导管接口顺序为a→
您最近一年使用:0次
2023-02-08更新
|
321次组卷
|
2卷引用:辽宁省朝阳市2022-2023学年高三上学期1月期末化学试题
7 . 含氰废水中氰化物主要形态是HCN和CN-。氰化物浓度较低时,可在碱性条件下用H2O2将其转化为N2。浓度较高时,用Fe、K2CO3溶液与HCN反应生成 、H2和CO2。已知酸性:
、H2和CO2。已知酸性: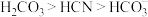 。下列化学反应表示错误的是
。下列化学反应表示错误的是
 、H2和CO2。已知酸性:
、H2和CO2。已知酸性: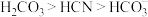 。下列化学反应表示错误的是
。下列化学反应表示错误的是A. K2CO3溶液与足量HCN溶液反应: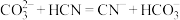 |
B.向NaCN溶液中通入少量CO2: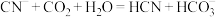 |
C.碱性条件下H2O2与CN-反应: |
D.Fe、K2CO3溶液与HCN溶液反应: |
您最近一年使用:0次
解题方法
8 . 利用锌精矿(含有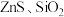 和铁、铝的氧化物等)和软锰矿(含有
和铁、铝的氧化物等)和软锰矿(含有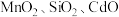 等)直接生产
等)直接生产 和
和 ,工艺流程如下:
,工艺流程如下:
①氧化性: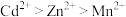 ;
;
② 稳定;
稳定;
③部分金属阳离子生成氢氧化物沉淀的 范围(开始沉淀和完全沉淀的
范围(开始沉淀和完全沉淀的 ):
): :
: :
: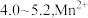 :
: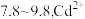 :
: :
: 。
。
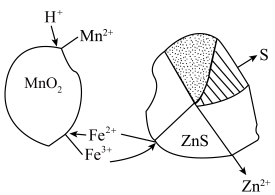
请回答下列问题: 微粒和
微粒和 微粒组成的微电池反应来实现的,如图。则该过程的总反应离子方程式为
微粒组成的微电池反应来实现的,如图。则该过程的总反应离子方程式为_______ 。
(2)“浸出渣”主要含有_______ 、_______ (填化学式),可利用物质的溶解性,选择_______ (填序号),将二者初步分离。
A.蒸馏水 B. 溶液 C.酒精 D.
溶液 C.酒精 D.
(3)“除镉”获得的“富镉渣”主要含有金属镉。若物质X为金属单质,则其原子基态价电子排布式为_______ 。
(4)“锌锰分离”时,若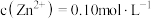 ,温度控制在常温,通过加入氨水调节
,温度控制在常温,通过加入氨水调节 控制溶液中
控制溶液中 沉淀率为99.9%(反应前后液体的体积变化忽略不计),则
沉淀率为99.9%(反应前后液体的体积变化忽略不计),则
_______ 。若氨水加入量过多,可导致_______ (至少答出1条结果)。
(5)“一系列操作”主要包括_______ 、_______ 、_______ 、_______ (按操作顺序填写)。
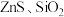 和铁、铝的氧化物等)和软锰矿(含有
和铁、铝的氧化物等)和软锰矿(含有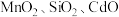 等)直接生产
等)直接生产 和
和 ,工艺流程如下:
,工艺流程如下: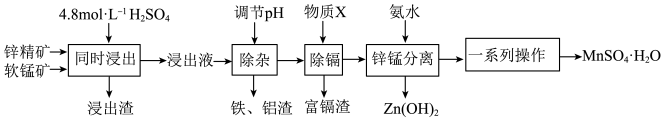
①氧化性:
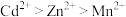 ;
;②
 稳定;
稳定;③部分金属阳离子生成氢氧化物沉淀的
 范围(开始沉淀和完全沉淀的
范围(开始沉淀和完全沉淀的 ):
): :
: :
: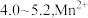 :
: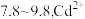 :
: :
: 。
。请回答下列问题:
 微粒和
微粒和 微粒组成的微电池反应来实现的,如图。则该过程的总反应离子方程式为
微粒组成的微电池反应来实现的,如图。则该过程的总反应离子方程式为(2)“浸出渣”主要含有
A.蒸馏水 B.
 溶液 C.酒精 D.
溶液 C.酒精 D.
(3)“除镉”获得的“富镉渣”主要含有金属镉。若物质X为金属单质,则其原子基态价电子排布式为
(4)“锌锰分离”时,若
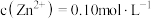 ,温度控制在常温,通过加入氨水调节
,温度控制在常温,通过加入氨水调节 控制溶液中
控制溶液中 沉淀率为99.9%(反应前后液体的体积变化忽略不计),则
沉淀率为99.9%(反应前后液体的体积变化忽略不计),则
(5)“一系列操作”主要包括
您最近一年使用:0次
解题方法
9 . 氯化碘(ICl)是红棕色液体,易挥发,熔点为 ,沸点为
,沸点为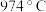 ,易与水反应,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组同学拟用下列仪器制备氯化碘。
,易与水反应,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组同学拟用下列仪器制备氯化碘。
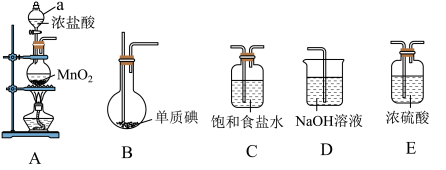
(1)a仪器名称___________ 。
(2)上述装置,按气流方向连接的顺序为___________ (装置可重复使用)。
(3)A装置中发生反应的化学方程式为___________ 。
(4)氟化氯与氯化碘都是卤素互化物,它可用于制备硝酸氯,原理为: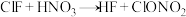 ,下列判断中正确的是___________。
,下列判断中正确的是___________。
(5)高铁酸钾 与
与 都是高效消毒剂,实验室可将氯气通入过量
都是高效消毒剂,实验室可将氯气通入过量 与
与 的混合溶液来制备
的混合溶液来制备 。向
。向 滴加盐酸可以生成氯气,说明氧化性:
滴加盐酸可以生成氯气,说明氧化性:
___________  (填“>”或“<”),而
(填“>”或“<”),而 的制备实验表明
的制备实验表明 和
和 的氧化性强弱关系相反,其原因是
的氧化性强弱关系相反,其原因是___________ 。
 ,沸点为
,沸点为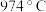 ,易与水反应,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组同学拟用下列仪器制备氯化碘。
,易与水反应,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组同学拟用下列仪器制备氯化碘。
(1)a仪器名称
(2)上述装置,按气流方向连接的顺序为
(3)A装置中发生反应的化学方程式为
(4)氟化氯与氯化碘都是卤素互化物,它可用于制备硝酸氯,原理为:
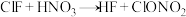 ,下列判断中正确的是___________。
,下列判断中正确的是___________。A. 和 和 熔融状态均能导电 熔融状态均能导电 |
B. 与 与 反应时,氯元素被还原 反应时,氯元素被还原 |
C.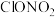 与水反应生成盐酸和硝酸 与水反应生成盐酸和硝酸 |
D. 化学性质与卤素单质相似,可以与锌反应 化学性质与卤素单质相似,可以与锌反应 |
(5)高铁酸钾
 与
与 都是高效消毒剂,实验室可将氯气通入过量
都是高效消毒剂,实验室可将氯气通入过量 与
与 的混合溶液来制备
的混合溶液来制备 。向
。向 滴加盐酸可以生成氯气,说明氧化性:
滴加盐酸可以生成氯气,说明氧化性:
 (填“>”或“<”),而
(填“>”或“<”),而 的制备实验表明
的制备实验表明 和
和 的氧化性强弱关系相反,其原因是
的氧化性强弱关系相反,其原因是
您最近一年使用:0次
10 . 高铁酸钾(K2FeO4)是一种既能杀菌 消毒、又能絮凝净水的水处理剂,工业制备高铁酸钾的离子方程式为Fe(OH)3+ClO-+OH-
 +Cl-+H2O (未配平)。下列有关说法不正确的是
+Cl-+H2O (未配平)。下列有关说法不正确的是

 +Cl-+H2O (未配平)。下列有关说法不正确的是
+Cl-+H2O (未配平)。下列有关说法不正确的是A.由上述反应可知,FeO 的氧化性强于ClO- 的氧化性强于ClO- |
| B.生成0.4molCl-时转移电子数0.8NA |
| C.上述反应中氧化剂和还原剂的物质的量之比为3∶2 |
D.K2FeO4处理水的原理可为:  |
您最近一年使用:0次
2023-11-17更新
|
379次组卷
|
3卷引用:辽宁省沈阳市重点高中五校协作体2023-2024学年高一上学期1月期末化学试题



