名校
解题方法
1 . 设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.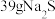 和 和 组成的混合物中,含有阴离子的数目为0.5NA 组成的混合物中,含有阴离子的数目为0.5NA |
| B.密闭容器中,1mol N2(g)与3mol H2(g)充分反应制备氨气,形成N−H键少于6NA |
C.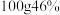 的乙醇溶液中,含 的乙醇溶液中,含 键的数目为 键的数目为 |
D.在标况下将 溶于足量 溶于足量 溶液中,转移电子数目为 溶液中,转移电子数目为 |
您最近半年使用:0次
2023-06-19更新
|
94次组卷
|
2卷引用:四川省达州市 万源中学2022-2023学年高一下学期5月期中测试化学试题
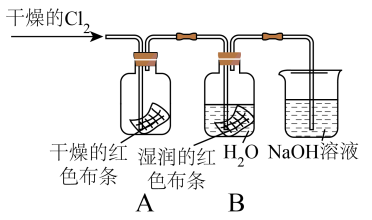
2 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为: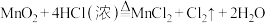 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
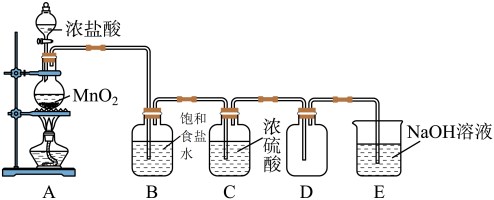
回答下列问题:
(1)装置B的目的是除去氯气中的___________ (填化学式)。
(2)在制取氯气的反应中,浓盐酸表现了酸性和___________ 性(填“氧化”或“还原”)。
(3)为了防止污染空气,在 烧杯中盛装冷的
烧杯中盛装冷的 溶液,吸收氯气后的溶液具有漂白性。
溶液,吸收氯气后的溶液具有漂白性。
①该漂白性溶液的有效成分是___________ (填名称)。
②检验该漂白性溶液中是否含有 的方法是:先取少量被检测的溶液中于试管中,滴入适量稀硝酸,使其酸化,再
的方法是:先取少量被检测的溶液中于试管中,滴入适量稀硝酸,使其酸化,再___________ ,如产生白色沉淀,则可判断该溶液中含有 。生成白色沉淀时,发生反应的离子方程式为
。生成白色沉淀时,发生反应的离子方程式为___________ 。
(4)为探究 的性质,某同学设计了如下实验:能看到红色布条褪色的装置是
的性质,某同学设计了如下实验:能看到红色布条褪色的装置是___________ (填“A”或“B”)。
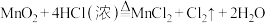 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
回答下列问题:
(1)装置B的目的是除去氯气中的
(2)在制取氯气的反应中,浓盐酸表现了酸性和
(3)为了防止污染空气,在
 烧杯中盛装冷的
烧杯中盛装冷的 溶液,吸收氯气后的溶液具有漂白性。
溶液,吸收氯气后的溶液具有漂白性。①该漂白性溶液的有效成分是
②检验该漂白性溶液中是否含有
 的方法是:先取少量被检测的溶液中于试管中,滴入适量稀硝酸,使其酸化,再
的方法是:先取少量被检测的溶液中于试管中,滴入适量稀硝酸,使其酸化,再 。生成白色沉淀时,发生反应的离子方程式为
。生成白色沉淀时,发生反应的离子方程式为(4)为探究
 的性质,某同学设计了如下实验:能看到红色布条褪色的装置是
的性质,某同学设计了如下实验:能看到红色布条褪色的装置是
您最近半年使用:0次
名校
解题方法
3 . 世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,亚氯酸钠在3类致癌物清单中,但其在工业上可用作漂白剂、脱色剂、清毒剂、拔染剂等, 的一种生产工艺如下:
的一种生产工艺如下:
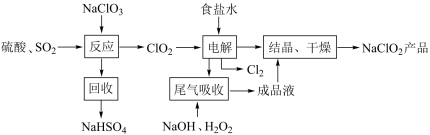
(1)写出“反应”步骤中生成 的化学反应方程式:
的化学反应方程式:_______ 。
(2)“电解所用食盐水由粗盐水精制而成,精制时为除去 ,加入的除杂试剂依次为
,加入的除杂试剂依次为_______ ,过滤后为得到纯净的 溶液还需加入
溶液还需加入_______ (以上填写相应物质的化学式)。设计除杂的实验方案时,除了要考虑所加试剂的种类,还要考虑_______ 。
(3)“电解”过程产生的 可用于工业制漂白液,写出工业制漂白液的化学方程式:
可用于工业制漂白液,写出工业制漂白液的化学方程式:_______ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中氧化产物是_______ 。
(5)新冠流行期间,一种名叫“VB空气防护卡”成为了网红。商品介绍卡片中含有的主要活性成分—— 。在接触空气时可以释放安全可靠的低浓度
。在接触空气时可以释放安全可靠的低浓度 ,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。
,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到
,同时得到 和钠的另一种正盐,试写出相应的化学反应方程式:
和钠的另一种正盐,试写出相应的化学反应方程式:_______ 。
 的一种生产工艺如下:
的一种生产工艺如下:
(1)写出“反应”步骤中生成
 的化学反应方程式:
的化学反应方程式:(2)“电解所用食盐水由粗盐水精制而成,精制时为除去
 ,加入的除杂试剂依次为
,加入的除杂试剂依次为 溶液还需加入
溶液还需加入(3)“电解”过程产生的
 可用于工业制漂白液,写出工业制漂白液的化学方程式:
可用于工业制漂白液,写出工业制漂白液的化学方程式:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(5)新冠流行期间,一种名叫“VB空气防护卡”成为了网红。商品介绍卡片中含有的主要活性成分——
 。在接触空气时可以释放安全可靠的低浓度
。在接触空气时可以释放安全可靠的低浓度 ,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。
,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到
,同时得到 和钠的另一种正盐,试写出相应的化学反应方程式:
和钠的另一种正盐,试写出相应的化学反应方程式:
您最近半年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
A. 通入冷的NaOH溶液: 通入冷的NaOH溶液: |
B.用醋酸和淀粉-KI溶液检验加碘盐中的 : : |
C.硫酸酸化的 溶液中加入 溶液中加入 : :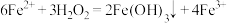 |
D. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
您最近半年使用:0次
名校
解题方法
5 . 以工业废渣[主要成分为 ,杂质为
,杂质为 ]为原料制备
]为原料制备 的流程如图:
的流程如图:

氯化时控制温度在75℃左右进行,充分反应后过滤所得滤液为 、
、 的混合溶液。下列有关说法正确的是
的混合溶液。下列有关说法正确的是
 ,杂质为
,杂质为 ]为原料制备
]为原料制备 的流程如图:
的流程如图:
氯化时控制温度在75℃左右进行,充分反应后过滤所得滤液为
 、
、 的混合溶液。下列有关说法正确的是
的混合溶液。下列有关说法正确的是A.氯化过程中通入 的速率越快越好 的速率越快越好 |
B.氯化后过滤,测定滤液中 与 与 的个数之比为2:3 的个数之比为2:3 |
C.滤渣的主要成分为 |
D.转化过程可能发生反应的化学方程式为 |
您最近半年使用:0次
2023-05-14更新
|
153次组卷
|
2卷引用:四川师范大学附属中学2022-2023学年高一下学期半期考试化学试题
名校
6 . 高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
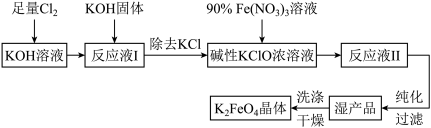
回答下列问题:
(1)写出Cl2与KOH溶液反应的化学方程式___________ 。
(2)在“反应液I”中加入KOH固体的目的是___________ 。
(3)写出Fe(NO3)3溶液与碱性KClO溶液反应的离子方程式___________ 。
(4)K2FeO4可作为新型多功能水处理剂的原因是___________ 。
(5)从“反应液II”中分离出K2FeO4后,副产品有___________ (写化学式)。实验室模拟工业流程中“过滤”操作用到的主要玻璃仪器有___________ 。
(6)该工艺每得到1.98kg K2FeO4,理论上消耗Cl2的物质的量为___________ mol。

回答下列问题:
(1)写出Cl2与KOH溶液反应的化学方程式
(2)在“反应液I”中加入KOH固体的目的是
(3)写出Fe(NO3)3溶液与碱性KClO溶液反应的离子方程式
(4)K2FeO4可作为新型多功能水处理剂的原因是
(5)从“反应液II”中分离出K2FeO4后,副产品有
(6)该工艺每得到1.98kg K2FeO4,理论上消耗Cl2的物质的量为
您最近半年使用:0次
2023-04-06更新
|
227次组卷
|
3卷引用:四川省眉山市2022-2023学年高二上学期期末教学质量检测理综化学试题
解题方法
7 . 下列离子方程式书写正确的是
A.用 溶液腐蚀覆铜板: 溶液腐蚀覆铜板: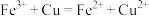 |
B.向稀硫酸中加入氢氧化镁: |
C.向冷的石灰乳中通入 制漂白粉: 制漂白粉: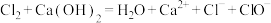 |
D. 溶液中通入过量的氯气: 溶液中通入过量的氯气: |
您最近半年使用:0次
8 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。下图是实验室制取纯净、干燥氯气装置图。
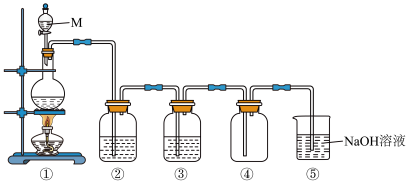
(1)M仪器的名称是___________ ,①中反应的反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。
(3)⑤中反应的离子方程式是___________ 。
【实验2】研究氯水性质。实验操作及现象如下表。
资料:淀粉的特征反应——遇 变蓝色
变蓝色
(4)实验2-1可证明氧化性
___________  (填“>”或“<”);实验2-2中使溶液褪色的粒子是
(填“>”或“<”);实验2-2中使溶液褪色的粒子是___________ 。
(5)证明氯水中含有氯离子的方案是___________ 。
(6)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。
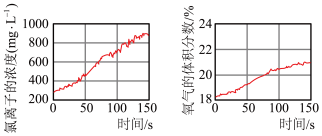
上两图中曲线变化的原因是___________ 。
【实验1】制备氯气。下图是实验室制取纯净、干燥氯气装置图。

(1)M仪器的名称是
(2)③中存放的试剂是
(3)⑤中反应的离子方程式是
【实验2】研究氯水性质。实验操作及现象如下表。
资料:淀粉的特征反应——遇
 变蓝色
变蓝色| 实验2-1 | 实验2-2 | |
| 实验操作(氯水均为新制) | 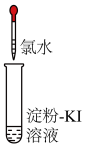 | 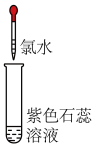 |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |

 (填“>”或“<”);实验2-2中使溶液褪色的粒子是
(填“>”或“<”);实验2-2中使溶液褪色的粒子是(5)证明氯水中含有氯离子的方案是
(6)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。

上两图中曲线变化的原因是
您最近半年使用:0次
名校
解题方法
9 . 下图是一种检验某气体化学性质的实验装置,图中B为开关。如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C中红色布条颜色褪去。则D瓶中盛有的溶液是
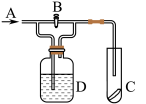

| A.浓H2SO4 | B.饱和Na2SO4 | C.浓NaOH溶液 | D.KI溶液 |
您最近半年使用:0次
2023-03-28更新
|
154次组卷
|
4卷引用:四川省成都市双流棠湖中学2023-2024学年高三上学期11月期中考试化学试题
四川省成都市双流棠湖中学2023-2024学年高三上学期11月期中考试化学试题四川省达州市万源中学2023-2024学年高一上学期12月月考化学试题(已下线)【2022】【高一上】【期中考】【杭十一中】【高中化学】【李雪收集】广东省普宁市华侨中学2022-2023学年高一上学期(11月)期中考试化学试题
解题方法
10 . 化学小组同学为研究氯气制备进行了如图实验。如图是实验室制取纯净、干燥氯气装置图。
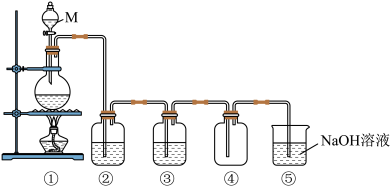
(1)M仪器的名称是_______ ,①中反应的反应的化学方程式是_______
(2)③中存放的试剂是_______
(3)⑤中反应的离子方程式是_______

(1)M仪器的名称是
(2)③中存放的试剂是
(3)⑤中反应的离子方程式是
您最近半年使用:0次



